Clear Sky Science · ru
Обзор данных о влиянии аполипопротеинов на атеросклеротические коронарные бляшки
Почему жиры в вашей крови по‑прежнему имеют значение
Инфаркты и инсульты часто начинаются с бесшумных изменений в сосудах, питающих сердце. Эта статья смотрит дальше привычных «хороших» и «плохих» холестеринов — на белковые оболочки, переносящие жиры по кровотоку, называемые аполипопротеинами. Прослеживая, как четыре таких белка влияют на рост, состав и лечение коронарных бляшек — жировых отложений, закупоривающих сосуды сердца — авторы показывают, почему некоторые люди остаются в зоне высокого риска сердечно‑сосудистых заболеваний, даже если их показатели холестерина кажутся идеальными.
Скрытые участники, «ездящие» на холестерине
Большинство из нас слышало о холестерине ЛПНП и ЛПВП, но каждая такая частица окружена одним или несколькими аполипопротеинами, которые во многом определяют, куда частица направится и насколько она опасна. В обзоре рассматриваются четыре ключевых типа: аполипопротеин(а), аполипопротеин A‑I, аполипопротеин B и аполипопротеин C‑III. Вместе они управляют сборкой жировых частиц, временем их циркуляции и способностью проникать в стенку артерии и повреждать её. Современные инструменты визуализации — ультразвук внутри сосуда, высокоразрешающие оптические методы и КТ‑ангиография — позволяют врачам видеть не только степень сужения сосуда, но и то, являются ли бляшки мягкими и склонными к разрыву или плотными и кальцифицированными. 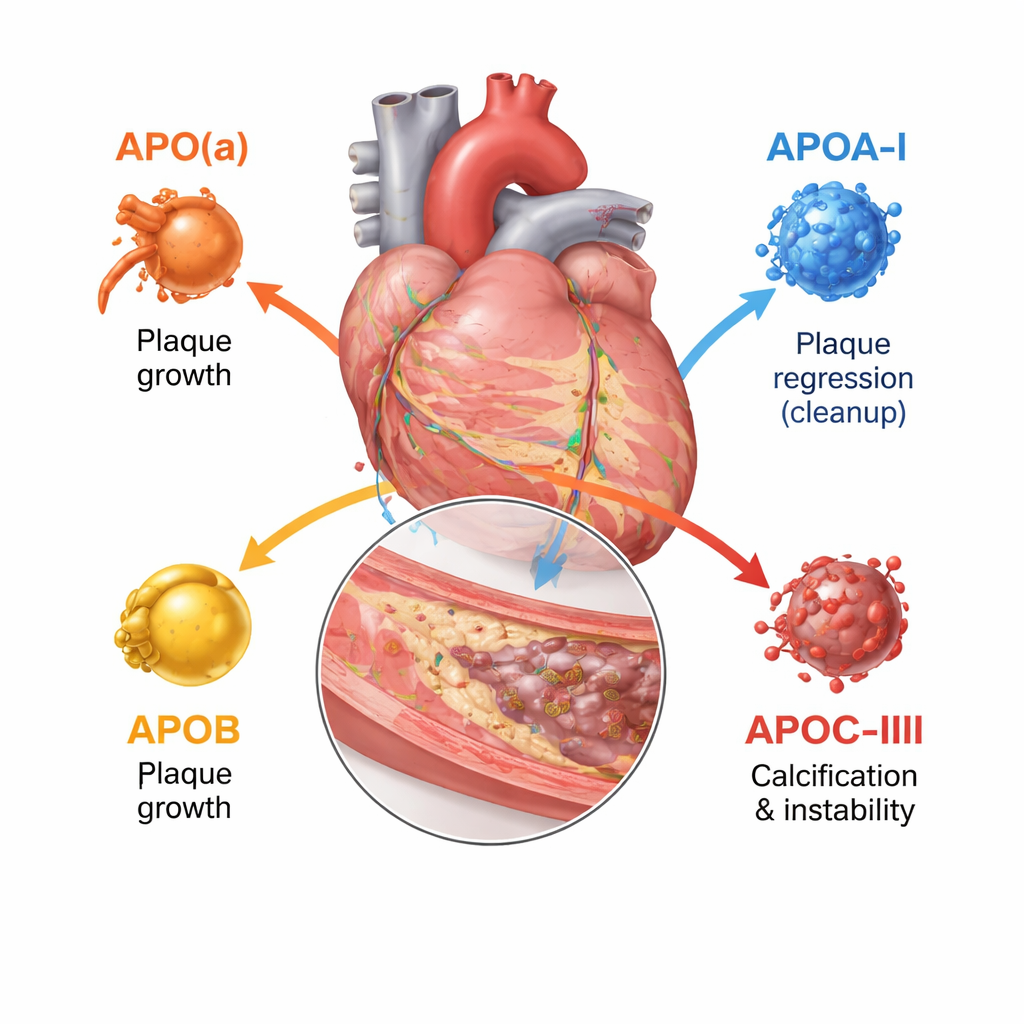
Как четыре белка формируют опасные бляшки
Аполипопротеин B присутствует на каждой частице ЛПНП и сходных частицах и фактически учитывает, сколько атерогенных — закупоривающих артерии — частиц содержится в крови. Чем больше частиц, несущих ApoB, и чем дольше они циркулируют, тем выше общий объём бляшек в коронарных артериях. Исследования с визуализацией внутри коронар показывают, что повышенные уровни ApoB сочетаются с большими по объёму бляшками, большей длиной поражений, большим числом мягких некротических ядер и меньшим количеством стабилизирующих отложений кальция. Напротив, аполипопротеин A‑I, основной белок на ЛПВП, способствует удалению холестерина из клеток бляшки и его обратному транспорту в печень. Более высокая функциональная активность ApoA‑I и благоприятное соотношение холестерина ЛПВП к ApoA‑I связаны с замедленным ростом бляшек и более фиброзной, стабильной тканью, хотя простое повышение уровня холестерина ЛПВП в крови не привело к снижению числа клинических событий.
Особый белок риска и фактор «уплотнения»
Аполипопротеин(а) образует частицу, называемую липопротеином(а) или Лп(а), когда присоединяется к ЛПНП‑подобному ядру. Уровень Лп(а) в основном определяется генетикой и, как правило, не изменяется диетой. Исследования визуализации у тысяч пациентов показывают, что люди с высоким Лп(а) имеют больше общей площади бляшек, больше участков с низкой плотностью и богатых липидами областей, а также больше очаговых «высокорискованных» бляшек, склонных к разрыву, даже при агрессивной терапии ЛПНП. Авторы обзора делают вывод, что Лп(а) представляет собой значительный «остаточный риск», который стандартные средства снижения холестерина не полностью устраняют. Аполипопротеин C‑III, в основном находящийся на частицах, богатых триглицеридами, замедляет их элиминацию и усиливает воспаление. У людей с более высоким уровнем ApoC‑III чаще выявляют коронарный кальциноз и более сложные, кальцифицированные узелки внутри бляшек — признаки продвинутой болезни и упрочнения артерий.
Новые лекарства, нацеленные на нужные мишени
Поскольку эти белки точнее, чем один только холестерин, отражают риск, они становятся прямыми мишенями для лекарств. Для Лп(а) несколько инъекционных генетических препаратов — антисмысловые олигонуклеотиды и препараты малых интерферирующих РНК — в ранних испытаниях снижают уровни на 80–95%, а также экспериментальная пероральная таблетка, блокирующая сборку частицы, демонстрирует крупные сокращения. Для ApoC‑III недавно одобренные терапии существенно снижают триглицериды и сам ApoC‑III, и первые данные указывают на возможное уменьшение частоты панкреатита и изменение кальцификации бляшек. 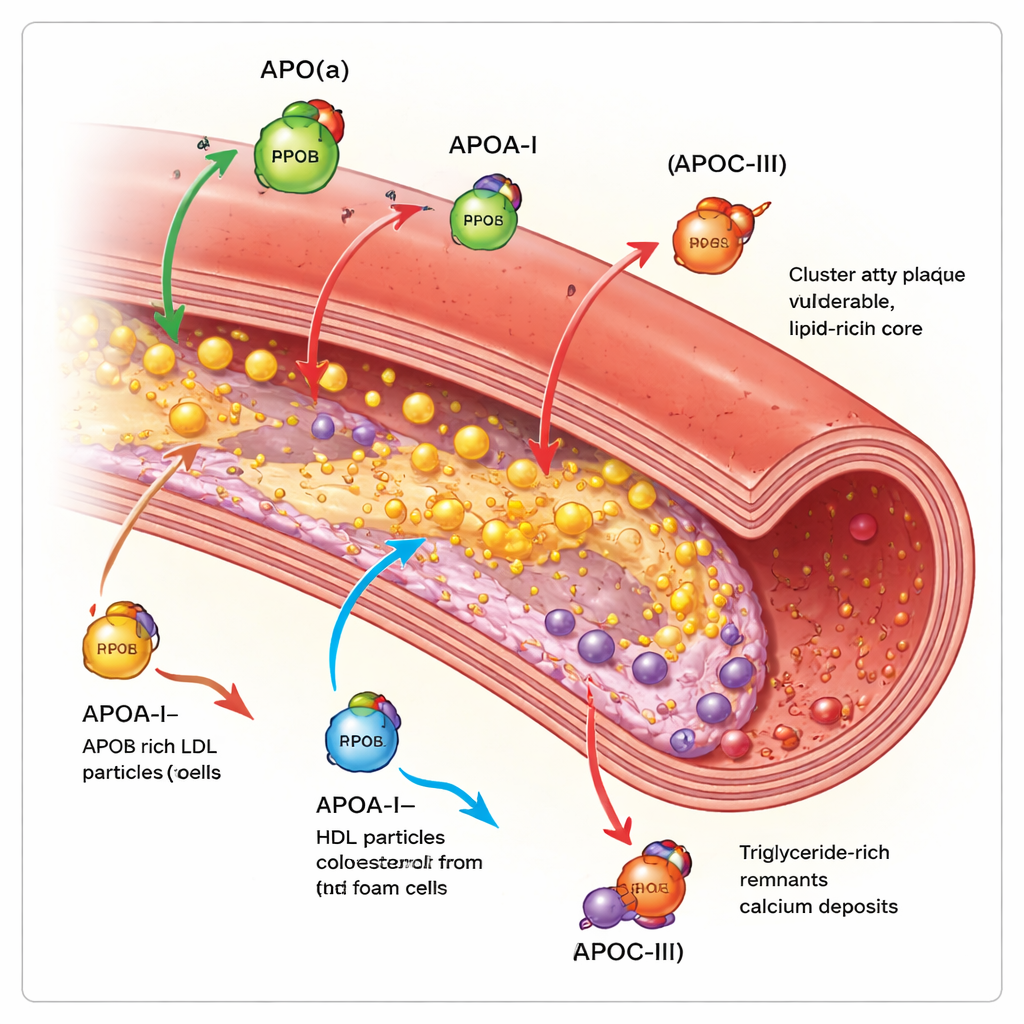
Что это значит для защиты вашего сердца
Проще говоря, в обзоре утверждается, что решение о том, у кого произойдёт инфаркт, не принимается только уровнями холестерина, а определяется смесью и поведением белково‑покрытых частиц, переносивших этот холестерин. ApoB отражает, сколько «вредных» частиц атакуют стенку артерии, ApoA‑I отражает систему, увозящую холестерин, Лп(а) добавляет дополнительный генетически обусловленный риск, а ApoC‑III способствует формированию уплотнённых, воспалённых бляшек. Новые препараты, направленные на снижение Лп(а) и ApoC‑III, а также более точное использование тестов на ApoB и ApoA‑I в повседневной практике могут позволить врачам индивидуализировать профилактику в соответствии с биологией бляшки каждого пациента и обнаруживать скрытый риск, который пропускают стандартные липидные панели.
Цитирование: Fukase, T., Dohi, T. A narrative review of impacts of apolipoproteins on atherosclerotic coronary plaques. npj Cardiovasc Health 3, 4 (2026). https://doi.org/10.1038/s44325-026-00104-x
Ключевые слова: липопротеин(а), аполипопротеин B, аполипопротеин A‑I, аполипопротеин C‑III, визуализация коронарных бляшек