Clear Sky Science · ru
Максимизация использования фотонов в спектроскопической микроскопии одиночных молекул с локализацией с помощью симметрично диспергирующих двойных клиньевых призм
Более чёткие взгляды на крошечный мир
Многие из важнейших действующих лиц в биологии — отдельные молекулы внутри наших клеток — слишком малы, чтобы увидеть их обычным микроскопом. За последнее десятилетие новые методы «сверхразрешения» изменили эту ситуацию, но они часто заставляют учёных жертвовать чёткостью изображения ради цветовой информации или требовать длинных и сложных экспериментов. В этой статье представлен изящный оптический модуль‑дополнение, который позволяет исследователям одновременно видеть разные типы молекул в 3D с лучшей детализацией и меньшими сложностями.
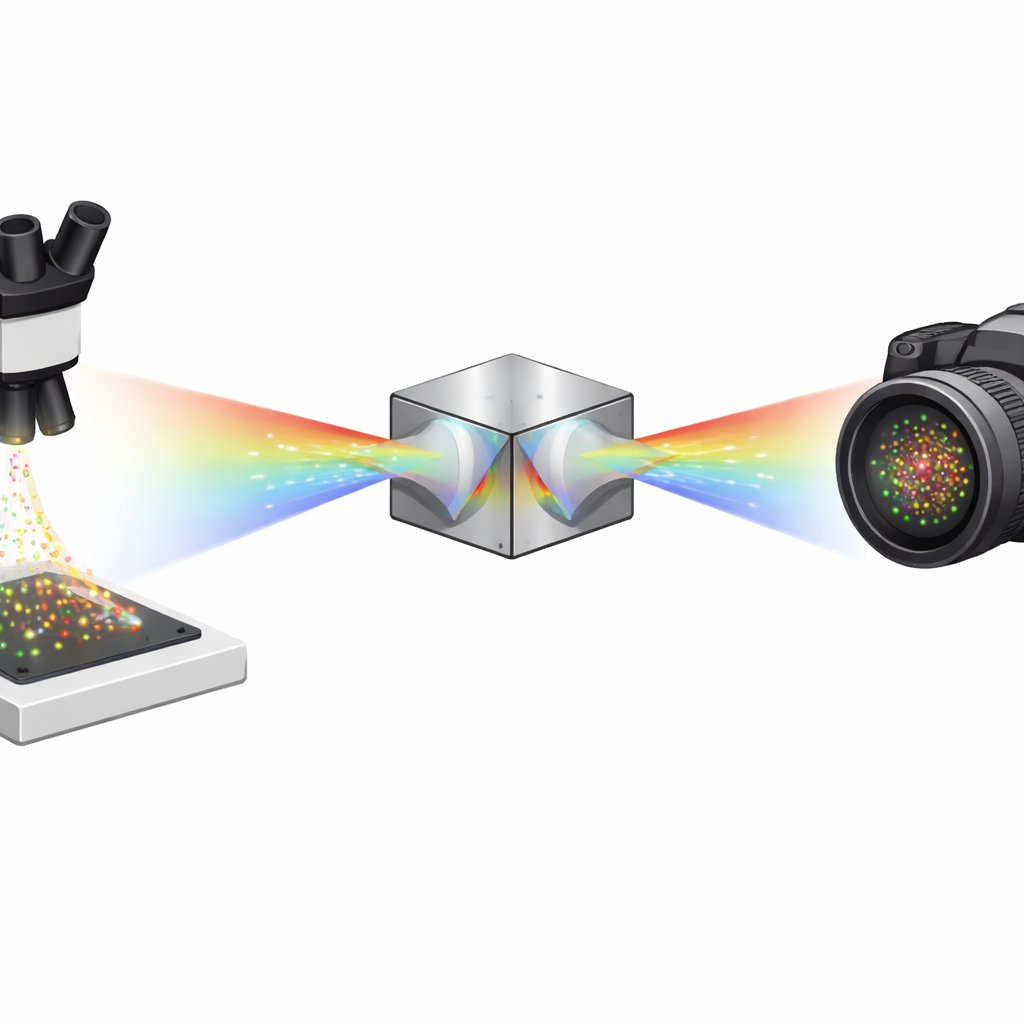
Наблюдение одиночных молекул по одной
Методы сверхразрешения, такие как STORM и PALM, работают, заставляя одновременно мигать лишь несколько флуоресцентных молекул, затем с высокой точностью определяют положение каждого вспышки и объединяют тысячи таких кадров в детализированное изображение. Спектроскопическая микроскопия одиночных молекул с локализацией (sSMLM) идёт дальше: она не только определяет, где находится каждая молекула, но и измеряет её спектр. Дополнительная спектральная информация особенно ценна, поскольку позволяет использовать несколько красителей с перекрывающимися спектрами и всё же различать их. Но традиционная sSMLM обычно вынуждена разделять драгоценные фотоны между изображением положения и спектральным изображением, что размазывает итоговую картину и затрудняет обнаружение слабых молекул.
Использование каждого фотона по двойному назначению
Авторы решают эту проблему с помощью компактного оптического модуля на основе двух одинаковых двойных клиньевых призм и делителя луча. Вместо того чтобы направлять фотоны в «положенческую» и отдельную «цветовую» ветви, их конструкция с симметрично диспергирующими двойными клиньями (SDDWP) создаёт на одной и той же камере два зеркально‑симметричных, спектрально растянутых изображения каждой мигающей молекулы. Поскольку эти два изображения идеально симметричны, простая вычислительная обработка позволяет восстановить и истинное положение молекулы (по средней точке между двумя пятнами), и её спектр (по расстоянию между пятнами). Фактически все собранные фотоны вносят вклад и в пространственную, и в спектральную информацию, что существенно повышает точность локализации и идентификации каждой молекулы.
Более чёткие, яркие цвета в трёх измерениях
С помощью аналитических моделей и тщательно калиброванных тестовых образцов команда показывает, что SDDWP повышает поперечную (в‑плоскости) точность примерно на 27% и спектральную точность примерно на 48% по сравнению с их прежней системой на основе призм. Далее они расширяют эту конструкцию до трёхмерной визуализации с использованием «биплэн» подхода, когда два спектральных изображения находятся немного вне фокуса в противоположных направлениях. Анализируя, как меняется размер каждого пятна между двумя плоскостями, система может определить, насколько далеко выше или ниже фокусной плоскости расположена молекула, достигая аксиальной точности порядка 18 нанометров в полезном диапазоне глубины примерно полмикрометра. Несмотря на добавленную сложность 3D‑визуализации, новая конструкция сохраняет почти двумерный уровень спектральной чёткости, позволяя тонко различать красители с сильно перекрывающимися спектрами.
Разделение структур клетки по цвету и отслеживание движущихся частиц
Чтобы показать практическое значение метода, исследователи сняли фиксированные клетки HeLa в 3D, используя один красный лазер и три далёко‑красных красителя, которые обычно имеют перекрывающиеся спектры. Они меченили пероксисомы, микротрубочки и митохондрии и показали, что система надёжно разделяет эти структуры на основе тонких спектральных различий, сохраняя высокую пространственную детализацию по глубине. Также они использовали спектрально различимые квантовые точки как крошечные метки для одновременного отслеживания множества частиц в вязком растворе. Рассматривая спектр каждой частицы как уникальный «отпечаток», установка SDDWP смогла корректно проследить сотни плотно упакованных траекторий, которые в противном случае запутались бы при пересечениях путей, снизив ошибки отслеживания до всего нескольких процентов даже при плотностях частиц, близких к теоретическим пределам.
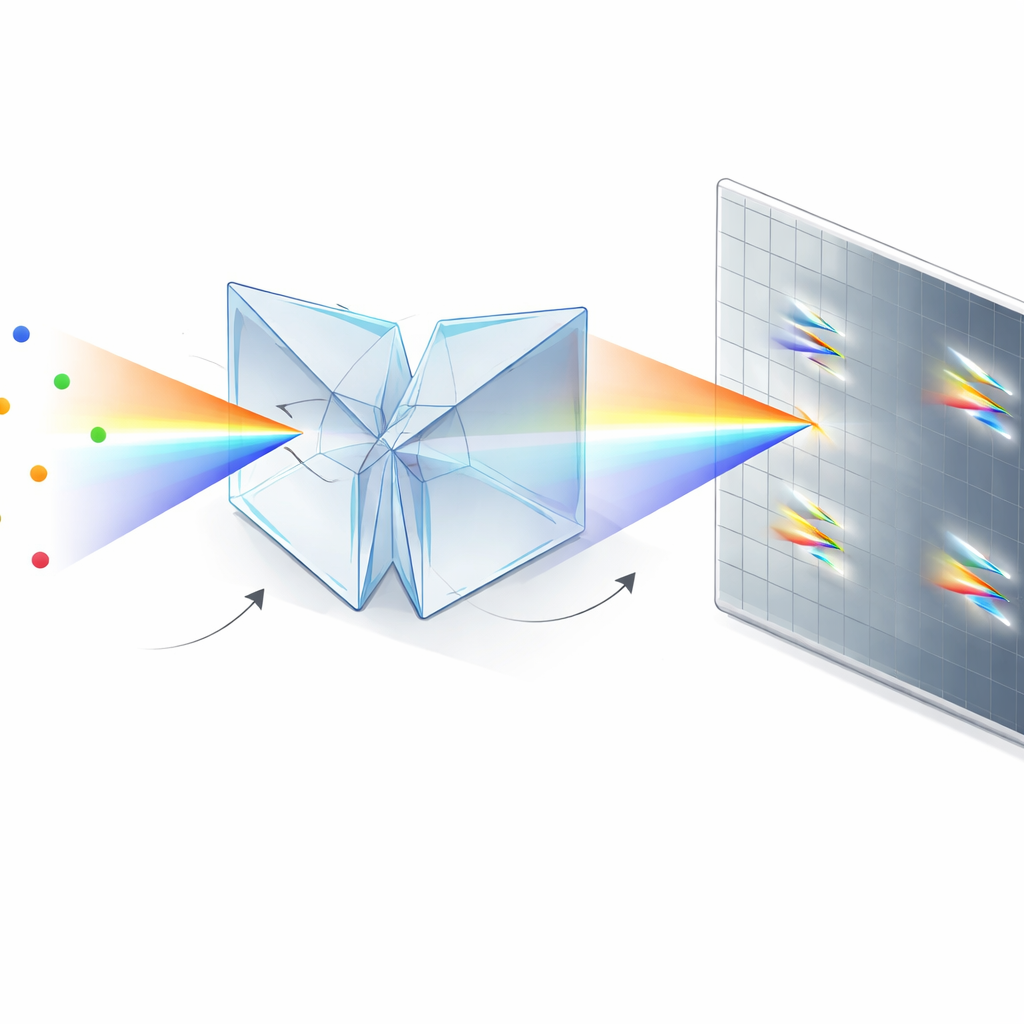
От сложной оптики к простому дополнению
Помимо производительности, ключевым преимуществом подхода является практичность. Блок SDDWP — небольшая, в основном монолитная сборка, которая крепится к боковому порту стандартного инвертированного флуоресцентного микроскопа и требует лишь умеренной юстировки. Его призменная конструкция тратит гораздо меньше фотонов, чем дифракционные решётки, и обладает достаточной механической стабильностью, чтобы оставаться откалиброванной в течение длительного времени при регулярных проверках. Это делает его реалистичным вариантом модернизации для многих существующих лабораторий, работающих с одиночными молекулами.
Что это означает для будущей микроскопии
Переосмыслив способы разделения и повторного комбинирования света, эта работа показывает, что можно получить и более точные положения, и более чёткую цветовую информацию из того же ограниченного набора фотонов. Проще говоря, это позволяет учёным различать больше типов молекул в плотных трёхмерных средах и одновременно отслеживать множество меченых частиц, не жертвуя качеством изображения. По мере того как техника будет применяться и адаптироваться — возможно, даже для съёмки живых клеток с мягким красным светом — она может стать универсальным инструментом для изучения того, как организованы сложные молекулярные ансамбли и органеллы и как они перемещаются внутри живых клеток на нанометрических масштабах.
Цитирование: Yeo, WH., Brenner, B., Shi, M. et al. Maximizing photon utilization in spectroscopic single-molecule localization microscopy using symmetrically dispersed dual-wedge prisms. npj Imaging 4, 20 (2026). https://doi.org/10.1038/s44303-026-00152-z
Ключевые слова: микроскопия одиночных молекул, сверхразрешающая визуализация, спектральная визуализация, 3D‑визуализация клеток, отслеживание отдельных частиц