Clear Sky Science · ru
Передовые методы визуализации для навигации при интраоперационной визуализации опухолей
Лучше видеть рак в операционной
Хирургия при раке часто сводится к деликатному компромиссу: удалить каждую раковую клетку и при этом сохранить как можно больше здоровых тканей. Это обзорное эссе объясняет, как новое поколение инструментов визуализации помогает хирургам видеть опухоли и их границы в реальном времени во время операции. Для неспециалиста привлекательность очевидна — эти технологии обещают меньше повторных операций, более точное удаление опухолей и лучшие шансы на долгосрочное выживание, потому что дают хирургу понятную «карту» прямо в процессе работы.
Почему важно лучше видеть во время операции
Рак сейчас — одна из ведущих причин смертности в мире, и операция по-прежнему остается краеугольным камнем лечения. Однако даже самый опытный хирург долгое время ограничивался тем, что можно увидеть и прощупать вручную, а также предоперационными снимками, сделанными за дни или недели до вмешательства. Традиционные инструменты, такие как ультразвук, КТ, МРТ и ПЭТ, помогают планировать операцию, но часто они громоздки, медленны или плохо подходят для непрерывного использования в ходе операции. В результате бывает трудно точно определить, где заканчивается опухоль и начинается здоровая ткань, что повышает риск оставить раковые очаги или удалить слишком много нормальной ткани. В обзоре показано, как «интраоперационная визуализация» — живая визуализация, используемая прямо в операционной — меняет эту картину.
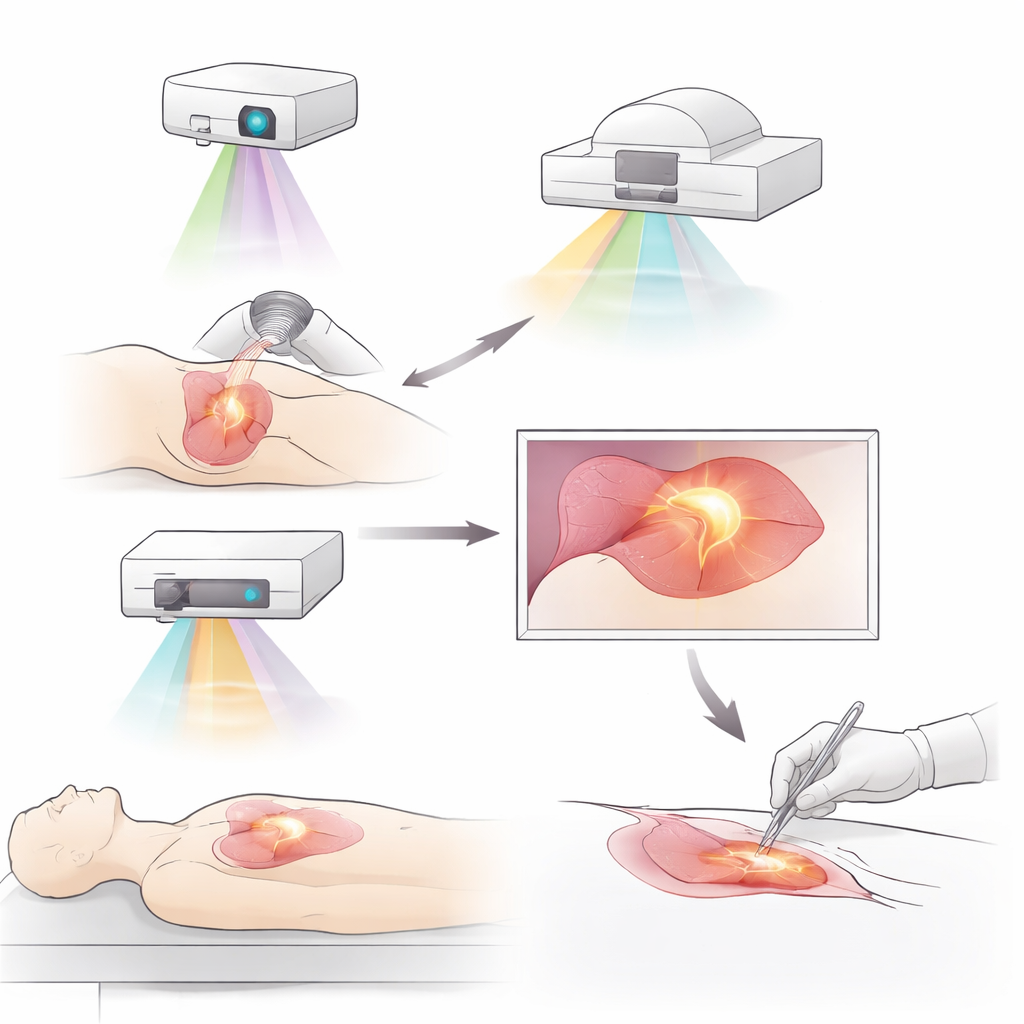
Светящиеся опухоли и новые способы их подсветки
Одним из ключевых достижений является флуоресцентная визуализация, при которой специальные красители или молекулярные зонды заставляют опухоли светиться под ближним инфракрасным светом. Старые, нетаргетированные красители, такие как индоцианиновый зеленый, уже помогают хирургам очерчивать опухоли, отслеживать лимфатические сосуды и находить важные лимфатические узлы при раке молочной железы, печени, легких и желудка. Новые таргетированные зонды идут дальше: они направляются на молекулы, которые избыточно экспрессируются опухолевыми клетками или в их микроокружении. Примеры включают зонды, которые связываются с рецепторами факторов роста, иммунными контрольными точками или белками, обильными в строме опухоли или в гипоксических зонах. Некоторые из этих агентoв могут быть связаны с противораковыми препаратами, сочетая точную визуализацию и терапию в одной молекуле. Ранние клинические испытания показывают, что такие трассеры способны обнаруживать скрытые очаги опухоли и снижать потребность в повторных операциях после органосохраняющих вмешательств при раке молочной железы.
Вне свечения: звук, свет и множество спектров
Хотя флуоресценция центральна, обзор выделяет несколько дополнительных подходов, которые фиксируют разные аспекты опухоли. Фотоакустическая визуализация использует импульсы света для генерации звуковых волн внутри ткани, сочетая детализацию оптических методов с глубиной проникновения ультразвука, и способна выявлять очень мелкие метастазы, которые пропускают другие сканы. Мультиспектральная и гиперспектральная визуализация разбивают свет на многочисленные полосы, улавливая тонкие различия в поглощении и отражении света тканями; это позволяет с высокой точностью отличать рак от нормальной ткани при опухолях молочной железы, шейки матки и желудочно-кишечного тракта. Достижения в ультразвуке — включая методы измерения жесткости ткани — добавляют информацию о глубине и помогают показать, насколько глубоко проник рак. Рамановская спектроскопия, которая считывает химический «отпечаток» ткани на основе того, как молекулы рассеивают свет, предлагает маркировку без контрастных агентов и высокую специфичность распознавания рака во время операции, особенно в комбинации с другими модальностями.
Построение 3D-карт и объединение нескольких видов изображений
Еще одна тема статьи — объединение изображений в трехмерные и мультимодальные представления, удобные для использования хирургом. Трехмерные реконструкции сосудов, лимфатических каналов и органов, наложенные на флуоресцентные сигналы, помогают планировать точные сегментарные резекции печени и легкого и направляют при сложных лимфаденэктомиях. Гибридные системы, которые совмещают ПЭТ с оптической визуализацией или соединяют нуклидные трассеры с флуоресценцией, позволяют использовать один и тот же зонд для предоперационного сканирования всего тела и интраоперационной навигации. Появляющиеся платформы интегрируют лазерную абляцию, оптическую когерентную томографию и робототехнику, чтобы автоматически локализовать и лечить поражения с высокой точностью. Такие подходы стремятся дать хирургу и «общую картину» распространения опухоли, и тонкие детали, необходимые для рассечения по безопасным, чистым границам.
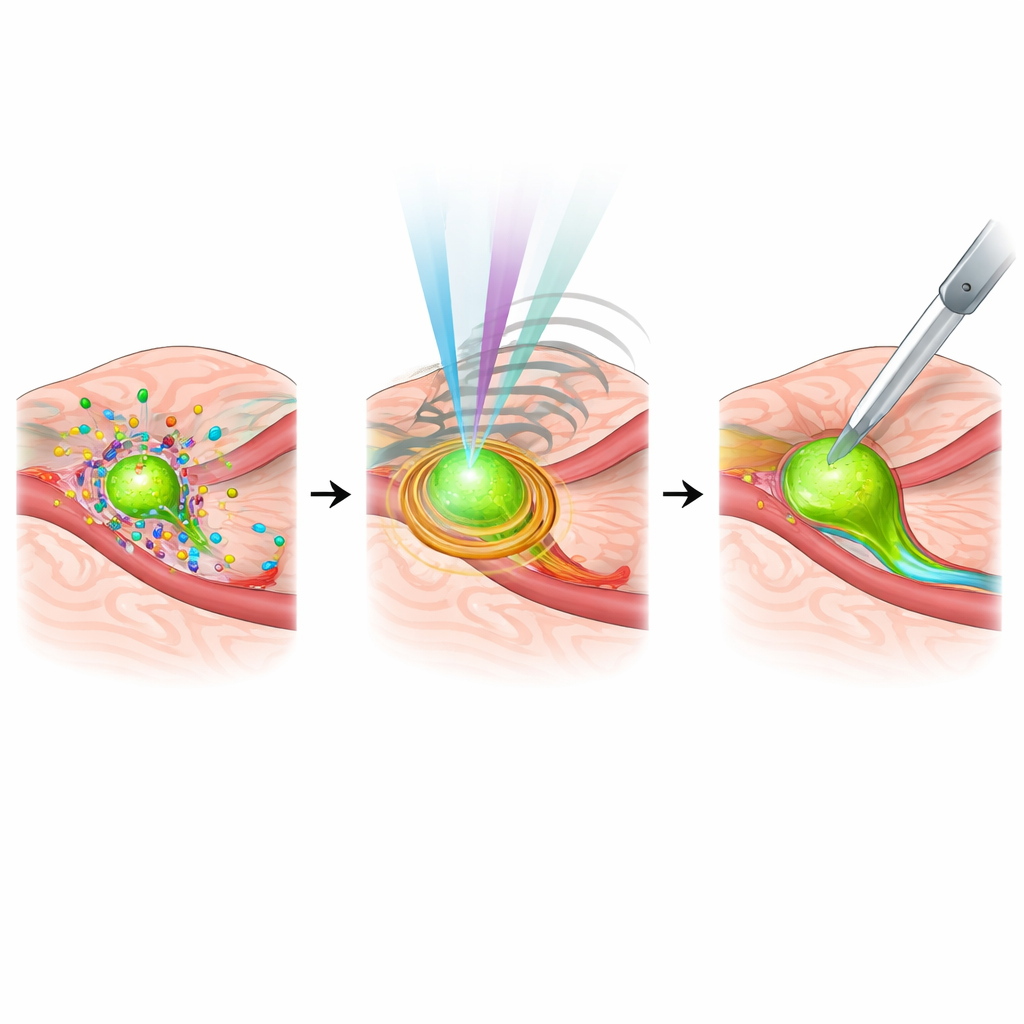
Более умные системы, персонализированные мишени и оставшиеся препятствия
Обзор также заглядывает в будущее роли искусственного интеллекта и персонализированной медицины. Модели машинного обучения уже помогают в реальном времени отличать раковую ткань от нормальной, распознавать критические анатомические структуры и даже прогнозировать распространение в лимфатические узлы при операциях на поджелудочной железе, что потенциально снижает зависимость от срочной патологии. Одновременно зонды для визуализации перерабатываются так, чтобы соответствовать уникальным молекулярным подписьям опухоли каждого пациента, связывая интраоперационные изображения с генетическими и молекулярными профилями. Тем не менее остаются препятствия: многие системы дорогие, сложные и трудно вписываются в рутинные рабочие процессы; некоторым требуется специализированные контрастные агенты с тщательно контролируемыми профилями безопасности; а стандарты интеграции всех этих данных в навигационные системы все еще формируются.
Что это значит для пациентов
Доступным языком заключение статьи таково: хирурги получают то, чего у них раньше не было в полной мере — способность видеть живую опухоль с высокой четкостью во время операции. Подсвечивая опухоли, читая их химию, картируя в 3D и комбинируя несколько типов изображений — часто с поддержкой ИИ — эти инструменты могут помочь удалить больше опухоли и сохранить больше здоровой ткани. Хотя стоимость, обучение и технологические разрывы нужно преодолеть до широкого внедрения таких систем, направление развития очевидно. Передовая интраоперационная визуализация готовится стать ключевой частью стандартной онкологической хирургии, предлагая пациентам более точные операции, меньше рецидивов и лучшие шансы на долгосрочный контроль заболевания.
Цитирование: Li, K., Zhang, Y., Yang, H. et al. Advanced imaging techniques for tumor intraoperative navigation imaging. npj Imaging 4, 18 (2026). https://doi.org/10.1038/s44303-026-00150-1
Ключевые слова: интраоперационная визуализация, хирургия с наведением по флуоресценции, обнаружение границ опухоли, мультимодальная визуализация рака, фотоакустическая визуализация