Clear Sky Science · ru
Одноступенчатая стратегия радиомаркировки для ПЭТ, СКЭТ и терапевтических радионуклидов с использованием наночастиц в роли универсального хелатора
Почему важны крошечные радиоактивные частицы
Современная онкология всё чаще опирается на препараты с радиоактивностью, которые одновременно помогают визуализировать опухоли в сканах и, в некоторых случаях, уничтожать их изнутри. Однако создание каждого нового радиофармацевтического препарата остаётся медленным и требовательным процессом, потому что большинство конструкций приходится адаптировать под конкретный радиоактивный металл. В этом исследовании рассматривается принципиально иной подход: использовать один тип наночастиц на основе железа как «универсальный разъём», способный удерживать различные медицинские изотопы для диагностики и терапии, что может ускорить разработку и тонкую настройку таких препаратов.
От множества ключей к одному замку
Современные радиопрепараты обычно опираются на химические «хватки» — хелаторы, которые захватывают атомы металлов и присоединяют их к антителам или другим молекулам-мишеням. Для каждого радиоактивного металла, как правило, нужен свой хелатор и своя рецептура — условия реакции, такие как температура, кислотность и время, меняются. Для некоторых важных в медицине металлов, особенно используемых в мощной альфа-частичной терапии, до сих пор нет идеального хелатора. Авторы утверждают, что такой подход «металл за металлом» стал узким местом: число полезных изотопов растёт, а химия для безопасной работы с ними не поспевает.
Наночастицы как универсальный разъём
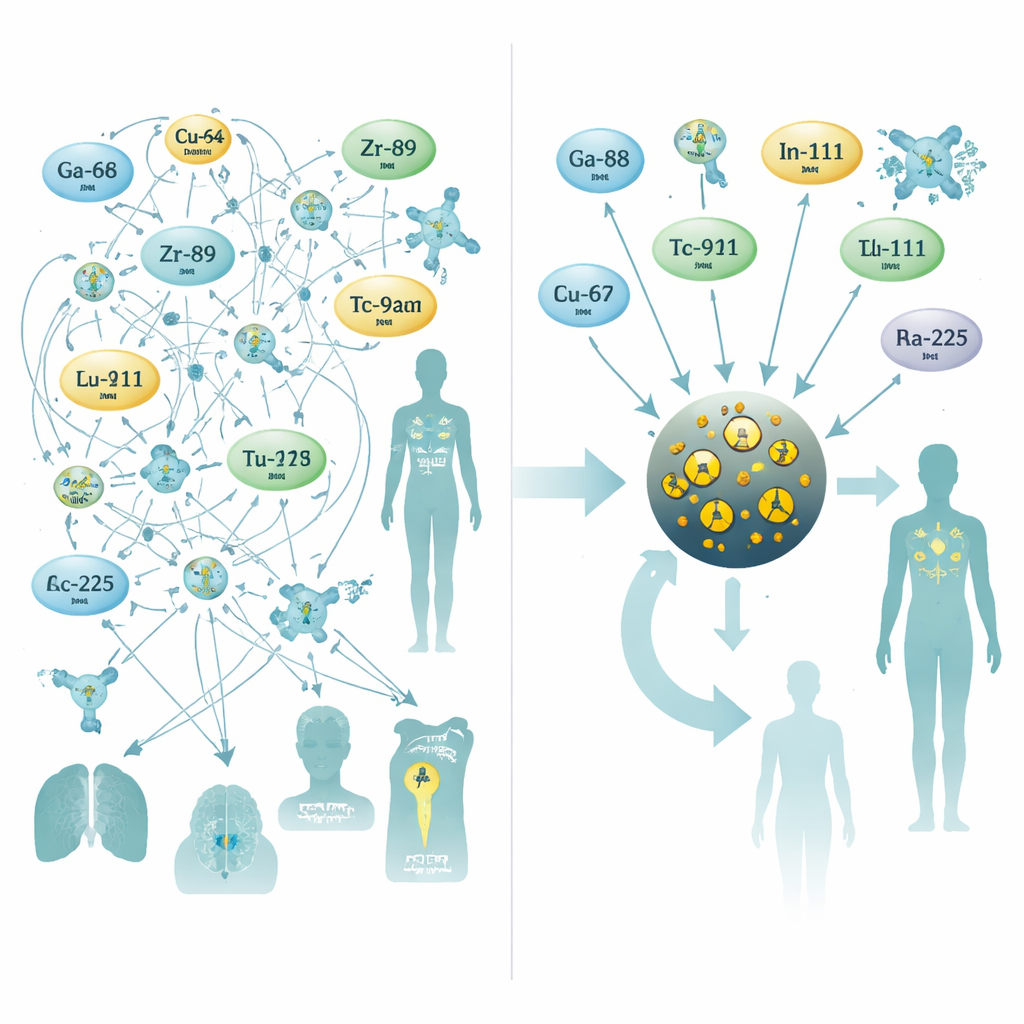
Чтобы решить эту задачу, исследователи обратились к очень маленьким наночастицам оксида железа — материалу, уже изучаемому в качестве контраста для МРТ. Они разработали частицы с ядром из оксида железа диаметром около трёх нанометров, покрытые цитратной оболочкой, которая обеспечивает стабильность в крови. В ходе единственного 10-минутного шага микроволнового синтеза они допировали ядро одним из десяти различных радиоактивных металлов, обычно используемых для ПЭТ, СКЭТ или внутренней радиотерапии. Этот одноконтейнерный процесс давал частицы одинакового размера с высокими выходами и, что важно, с отличной стабильностью в сыворотке человека — даже для сложных терапевтических изотопов, таких как радий-223 и актиний-225, дочерние продукты распада которых часто ускользают от традиционных хелаторов.
Визуализация тромбов и опухолей мозга
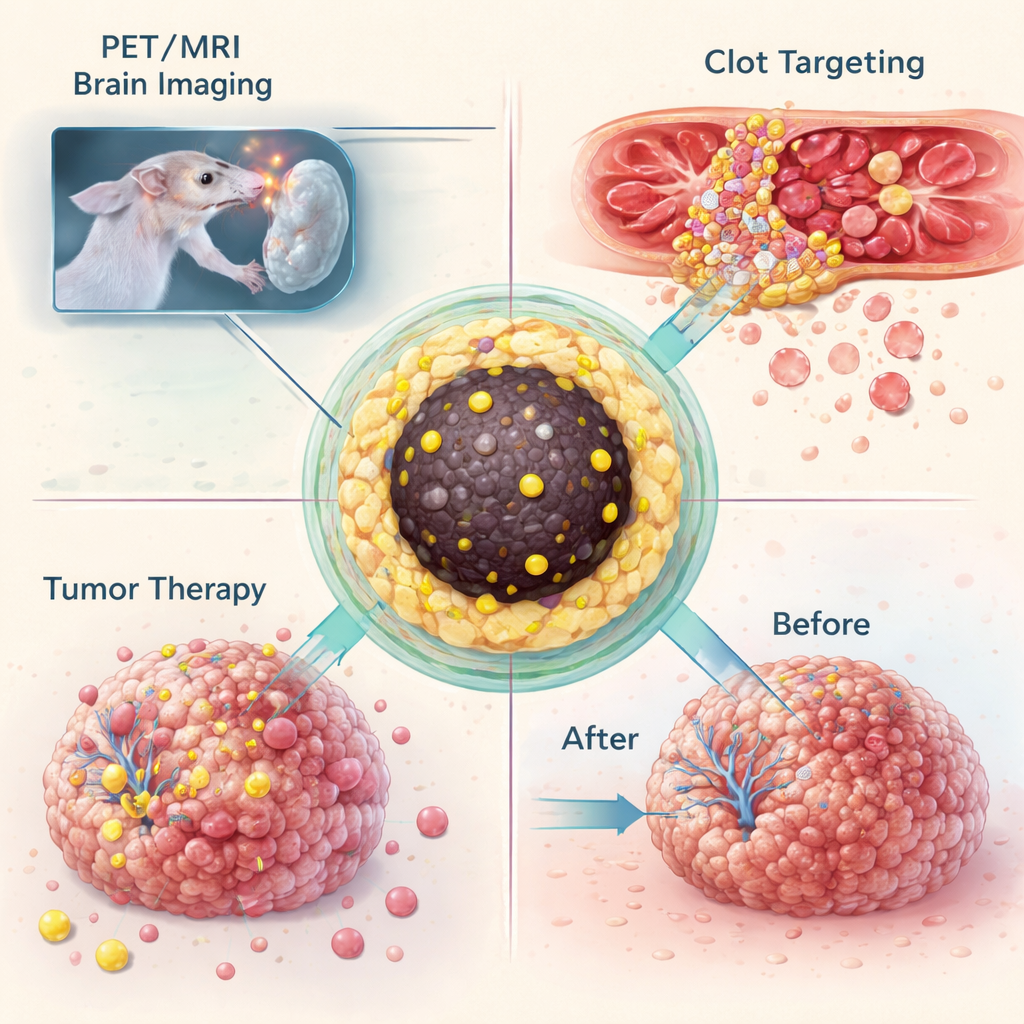
Показав способность задерживать разные изотопы в одной конструкции наночастиц, команда протестировала эти «нанотрассеры» на живых животных. В модели глиобластомы у мышей частицы, меченные галлием-68, вводили в кровь и визуализировали с помощью комбинации ПЭТ и МРТ. Частицы накапливались в опухолях, достаточно больших, чтобы нарушить гематоэнцефалический барьер, что позволило одной и той же формуле обеспечивать как яркий МРТ-контраст, так и чувствительный ПЭТ-сигнал. В отдельном эксперименте частицы химически модифицировали так, чтобы они могли соединяться посредством высокоселективной «щелочной» реакции click с антителом, ориентирующимся на активированные тромбоциты внутри кровяных сгустков. У мышей с повреждённой сонной артерией эта двухшаговая стратегия «предтаргетирования» дала чёткие ПЭТ-сигналы в месте тромба, тогда как в контрольных животных такого горячего пятна не наблюдалось.
От диагностики к лечению и более безопасному выведению
Ту же платформу использовали и для доставки терапии. При прямой инъекции наночастиц, нагруженных лютецией-177, в опухоли глиобластомы у мышей частицы в основном оставались в пределах опухолевой массы как минимум в течение двух недель. За это время нелечёные опухоли увеличивались в несколько раз, тогда как лечёные прекращали рост, что говорит о том, что локальная доза радиации была достаточной для остановки прогрессирования. Понимая, что многократные введения могут перегружать печень и селезёнку железом, команда затем изменила условия синтеза, чтобы получить ещё меньшие частицы — около четырёх–пяти нанометров — которые достаточно малы, чтобы фильтроваться почками. Эти уменьшенные частицы по-прежнему надёжно удерживали свой радиоактивный груз, но быстро выводились в мочевой пузырь, уменьшая долгосрочное накопление в основных органах.
Что это может значить для будущей онкологической помощи
Для неспециалистов ключевое сообщение в том, что исследователи создали одну гибкую платформу наночастиц, которую можно сочетать с множеством разных радиоактивных металлов, не изобретая заново химию каждый раз. В моделях на животных одна и та же базовая частица может помогать обнаруживать опухоли мозга, выделять тромбы, доставлять радиацию непосредственно в опухоли и даже быть настроенной на выведение через почки. Хотя прежде чем этот подход дойдёт до пациентов, потребуется ещё много работы, он предлагает перспективный путь к созданию семейств диагностических и терапевтических агентов, которые ведут себя одинаково в организме, различаясь лишь видом переносимого излучения. Такая согласованность может упростить разработку, улучшить тестирование безопасности и в конечном итоге сделать передовые инструменты ядерной медицины более доступными.
Цитирование: Herraiz, A., Rodríguez-San-Pedro, A., Casquero-Veiga, M. et al. A single-step radiolabeling strategy for PET, SPECT, and therapeutic radionuclides using nanoparticles as a universal chelator. npj Imaging 4, 8 (2026). https://doi.org/10.1038/s44303-026-00142-1
Ключевые слова: радиотерапевтика, наночастицы, ПЭТ-визуализация, глиобластома, таргетная радиотерапия