Clear Sky Science · ru
Ускоренная и локализованная синуклеинопатия в гибридной мышиной модели: последствия для исследований с позитронно-эмиссионной томографией
Почему это исследование важно
Болезнь Паркинсона наиболее известна тремором и нарушениями движения, но в глубине мозга она начинается с крошечных изменений, которые трудно заметить. Врачи остро нуждаются в методах для раннего выявления этих изменений и для быстрой проверки новых препаратов. В этом исследовании описана усовершенствованная мышиная модель, которая воспроизводит ключевые признаки повреждения мозга, похожие на болезнь Паркинсона, всего за несколько недель и в очень ограниченной области мозга, специально адаптированной для использования с продвинутой визуализацией мозга — позитронно-эмиссионной томографией (PET). 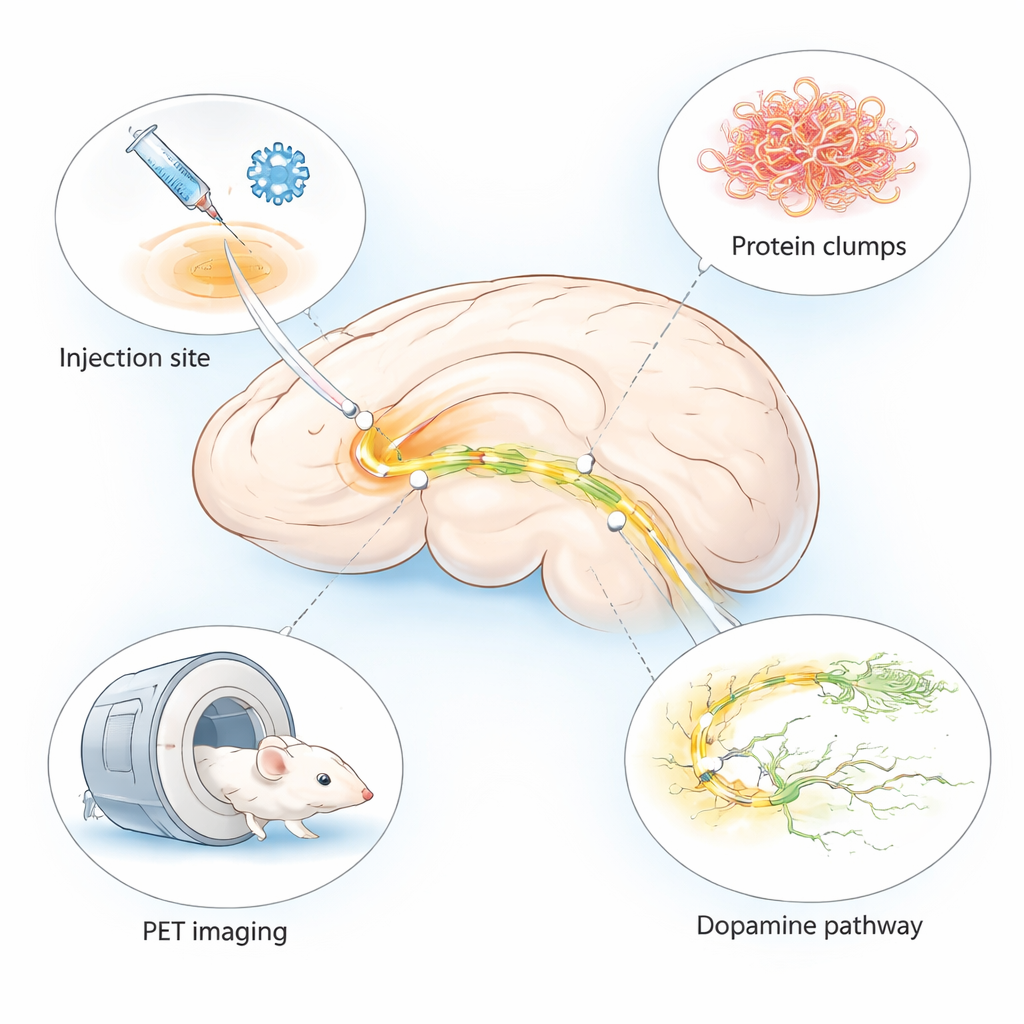
Создание более быстрой и сфокусированной модели болезни
Многие существующие модели болезни Паркинсона у животных требуют месяцев для развития симптомов или не демонстрируют полного набора изменений мозга, наблюдаемых у пациентов. Авторы объединили два уже известных подхода в одну «гибридную» модель. Они ввели безвредный вирус, заставляющий клетки мозга производить человеческий альфа‑синуклеин — белок, который образует сгустки при болезни Паркинсона, — вместе с предварительно сформированными фибриллами, действующими как семена, запускающие дальнейшее агрегацию. Оба компонента были доставлены в небольшую, связанную с движением область — субстанцию нигру — с одной стороны мозга мыши. Такая схема вызывает локальные, но интенсивные изменения, похожие на болезнь, на стороне инъекции, в то время как противоположная сторона остается относительно здоровой для сравнения.
Отслеживание белковых сгустков и гибнущих нейронов
Всего через две недели после инъекции у мышей обнаружили высокий уровень человеческого альфа‑синуклеина и его аномальной, фосфорилированной формы в целевой области мозга. Под микроскопом исследователи увидели структуры, напоминающие тельца Леви и лиевые нейриты — характерные признаки болезни Паркинсона. В течение следующих нескольких недель эти аномальные отложения увеличивались. В то же время начали исчезать нейроны, продуцирующие дофамин — нейромедиатор, жизненно важный для плавности движений. Маркеры этих клеток уменьшились примерно до 60 процентов от уровня на неповрежденной стороне к пятой неделе, что подтверждает явную прогрессирующую потерю дофаминовой системы.
Воспаление, ослабевающие синапсы и усталые «энергетические станции»
Иммунные клетки мозга, называемые микроглией, также перешли в высокоактивное, воспалительное состояние вокруг поврежденной области. Окраски для нескольких белков, связанных с воспалением, были значительно сильнее рядом с отложениями альфа‑синуклеина, чем на противоположной стороне мозга. На более поздних этапах команда обнаружила утрату синапсов — крошечных контактных точек, через которые нейроны общаются, — и признаки нарушения работы митохондрий, «энергетических фабрик» клеток. В совокупности эти наблюдения показывают, что модель воспроизводит не только образование белковых сгустков, но и цепную реакцию воспаления, утраты связей и энергетических проблем, которые способствуют гибели нейронов при болезни Паркинсона. 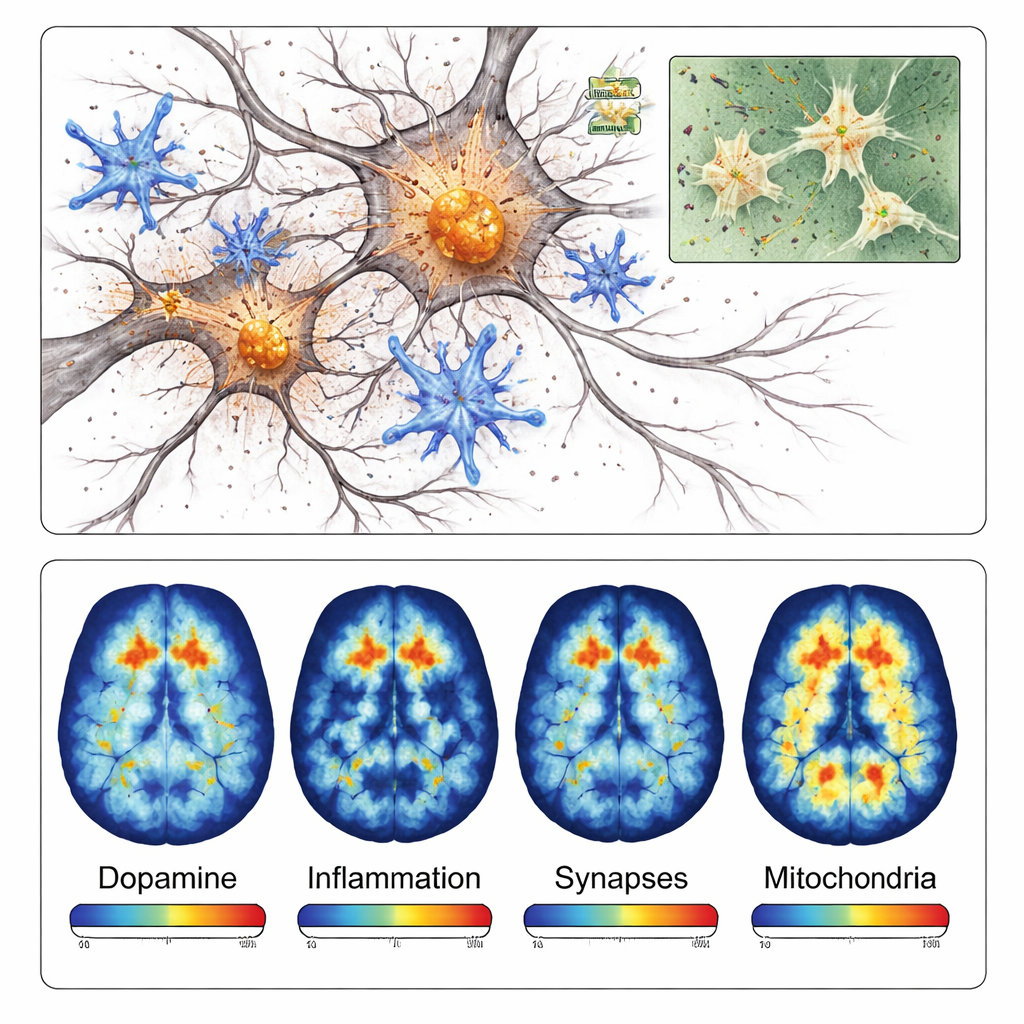
Применение ПЭТ-сканеров
Поскольку эта модель локализована и развивается быстро, она особенно пригодна для позитронно-эмиссионной томографии (PET) — метода сканирования, позволяющего измерять специфические молекулы в живом мозге. Исследователи протестировали четыре разных ПЭТ-трейсера, связывающихся с дофаминергическими окончаниями, воспалительной микроглией, синаптическими белками и митохондриальными ферментами. В каждом случае ПЭТ-снимки показали более низкие или более высокие сигналы на стороне инъекции таким образом, что это соответствовало результатам микроскопии. Например, трейсер, нацеленный на дофаминовые пути, показал примерно на 40 процентов меньший сигнал на поврежденной стороне, тогда как маркер воспаления продемонстрировал более чем на 40 процентов больший сигнал в пораженной области.
Что это значит для пациентов и будущих терапий
Эта новая мышиная модель объединяет в короткие сроки многие ключевые изменения, которые у людей с болезнью Паркинсона развиваются в течение лет. Поскольку повреждение ограничено небольшой, четко определенной областью и может отслеживаться с помощью ПЭТ, исследователи могут эффективнее тестировать новые визуализационные трейсеры и потенциальные терапии. Хотя ни одна мышиная модель не способна полностью воспроизвести человеческое состояние, такой подход предоставляет мощный практичный инструмент для сокращения дистанции между лабораторными исследованиями и клиническими испытаниями, в конечном счете помогая уточнить диагностику и ускорить поиск более эффективных методов лечения.
Цитирование: Xia, C.A., Tsai, HM., Diaz Garcia, S. et al. Accelerated and localized synucleinopathy in a hybrid mouse model: implications for positron emission tomography studies. npj Imaging 4, 7 (2026). https://doi.org/10.1038/s44303-026-00138-x
Ключевые слова: Болезнь Паркинсона, альфа-синуклеин, синуклеинопатия, PET-сканирование, мышиная модель