Clear Sky Science · ru
Разные роли шаперонов Hsp70 в секреции белков ортофлавивирусов и формировании вирионов
Почему крошечные «помощники при тепловом шоке» важны для вирусов, поражающих мозг
Вирусы, переносимые клещами и комарами, такие как вирус клещевого энцефалита и вирус Западного Нила, могут проникать в головной мозг и вызывать тяжёлые заболевания, однако специфических лекарств против них до сих пор нет. В этом исследовании изучают, как эти вирусы захватывают набор собственных клеточных «помощников» — шаперонов Hsp70 — чтобы собирать и выпускать новые вирусные частицы. Поскольку белки Hsp70 уже рассматриваются как мишени для лекарств при раке, понимание этой связи может открыть новые подходы к лечению опасных вирусных инфекций, не атакуя вирусы напрямую.
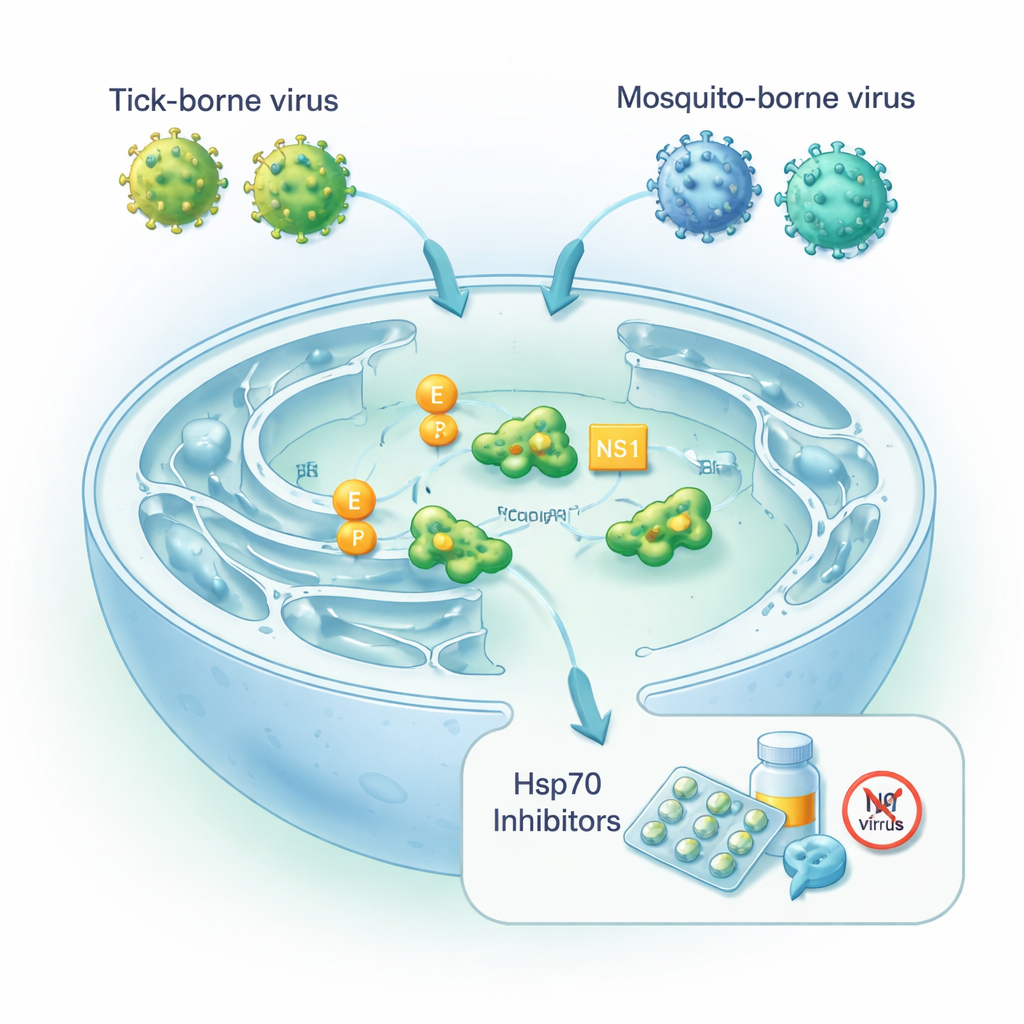
Вирусы, опирающиеся на клеточный аппарат свёртывания белков
Ортофлавивирусы — это мелкие РНК‑вирусы, генетический материал которых кодирует длинный полипротеин, требующий расщепления и свёртывания в несколько функциональных частей. Два ключевых вирусных компонента — оболочный белок E, покрывающий вирусную частицу и позволяющий ей входить в новые клетки, и нестуктурный белок NS1, который помогает вирусу копировать геном и может секретироваться для манипуляции иммунной системой. Всё это происходит в эндоплазматическом ретикулуме — отделе клетки, где многие белки свёртываются и готовятся к экспорту. Там клетка полагается на шапероны Hsp70, включая местную форму BiP, чтобы защищать новосинтезированные белки от неправильного свёртывания при стрессе. Авторы задали вопрос, насколько сильно нейротропные клещевые и комариные ортофлавивирусы зависят от этих шаперонов при сборке инфекционных частиц.
Прямые «рукопожатия» между вирусными белками и Hsp70
Используя клетки, генетически модифицированные для перепроизводства отдельных вирусных белков, а также клетки, инфицированные аутентичными вирусами, исследователи выделяли BiP или Hsp70 и проверяли, какие вирусные партнёры с ними шли. Они обнаружили, что BiP и Hsp70 последовательно образовывали комплексы с оболочным белком E у нескольких ортофлавивирусов, переносимых как клещами, так и комарами. Это указывает на то, что свёртывание E в эндоплазматическом ретикулуме направляется этими шаперонами. Картина для NS1 оказалась более избирательной: BiP и Hsp70 прочно связывались с NS1 у клещевых вирусов (вируса клещевого энцефалита и вируса Langat), но не с NS1 у комариных вирусов (вирусы Западного Нила и Usutu). Эти различия, вероятно, отражают вариации в гликозилировании и свёртывании NS1, намекая, что не все родственные вирусы используют одни и те же клеточные пути.
Блокирование шаперонов резко снижает продукцию вируса
Поскольку белки Hsp70 являются доступными для воздействия препаратами, команда протестировала два малых молекулы, вмешивающиеся в разные участки шаперонного механизма. YM‑1 нацелен на нуклеотидсвязывающий домен, замораживая Hsp70 в неактивном состоянии, тогда как PES‑Cl блокирует карман, связывающий субстрат, который обычно захватывает клиентские белки. При дозах, сохранявших большинство клеток живыми, YM‑1 резко уменьшал количество высвобождаемого инфекционного вируса для всех четырёх протестированных ортофлавивирусов и снижал количество оболочного белка, обнаруженного в культуральной среде, указывая на общий блок в формировании или выходе частиц. PES‑Cl, напротив, мало влиял на титры инфекционного вируса или на уровни оболочного белка, хотя в тестах связывания он ослаблял физическое взаимодействие между Hsp70/BiP и оболочным белком. Это предполагает, что кратковременное вмешательство в «захватывающий» карман недостаточно, чтобы нарушить сборку вируса, тогда как остановка энерго‑зависимого цикла шаперона — да.
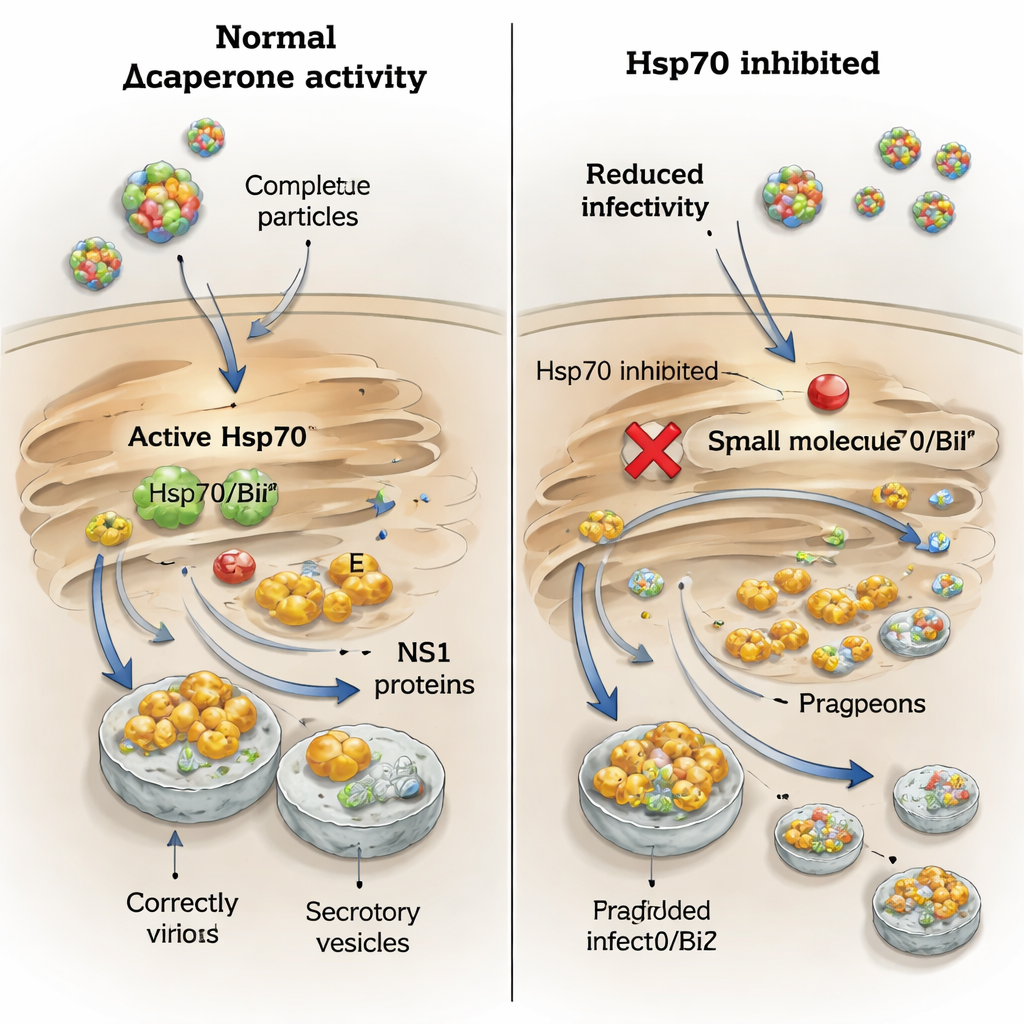
Особая зависимость клещевых вирусов от BiP в отношении NS1
История с NS1 оказалась более тонкой. При обработке инфицированных клеток PES‑Cl секреция NS1 у вирусов клещевого энцефалита и Langat резко падала, тогда как NS1 у вирусов Западного Нила и Usutu не изменялась. Это отражает предыдущее наблюдение, что только клещевые NS1 прочно связываются с BiP и Hsp70. Чтобы более детально изучить роль BiP, авторы использовали малые интерферирующие РНК для избирательного снижения уровня BiP. Это уменьшало количество как оболочного белка, так и NS1 внутри клеток и в окружающей среде для вирусов клещевого энцефалита и Западного Нила, однако титры инфекционных частиц падали лишь умеренно. Когда в клетках с дефицитом BiP применяли препараты, блокирующие деградацию белков, уровни NS1 внутри клетки восстанавливались, но его секреция не возвращалась, что показывает: BiP нужен не только чтобы защитить NS1 от разрушения, но и чтобы направлять его по секреторному пути.
Что это значит для будущих противовирусных стратегий
Для неспециалиста главный вывод в том, что эти вирусы, поражающие мозг, в значительной степени полагаются на собственные клеточные «помощники свёртывания» для формирования своей внешней оболочки и, для некоторых видов, для вывода NS1 в качестве секретируемого оружия. Широко действующий ингибитор шаперонов, такой как YM‑1, может поэтому сократить производство инфекционных частиц у нескольких родственных вирусов одновременно, хотя его мощные эффекты, вероятно, выходят за рамки одного шаперона и могут нарушать работу здоровых клеток. Более прицельные подходы, возможно, сосредоточенные на том, как BiP и Hsp70 обрабатывают конкретные вирусные клиенты вроде NS1, могут однажды помочь разработать лечения, которым труднее будет сопротивляться вирусам и которые при этом пощадят большую часть нормального свёртывания белков у хозяина.
Цитирование: Blank, L., Lorenz, C. & Steffen, I. Divergent roles of Hsp70 chaperones in orthoflavivirus protein secretion and virion formation. npj Viruses 4, 8 (2026). https://doi.org/10.1038/s44298-026-00175-8
Ключевые слова: ортофлавивирус, шаперон Hsp70, клещевой энцефалит, вирус Западного Нила, мишени для противовирусных препаратов