Clear Sky Science · ru
Растворимый G-белок респираторного синцитиального вируса способствует распространению вируса через активацию NLRP3 посредством TLR2 и пироптоз
Почему этот респираторный вирус важен для всех
Респираторный синцитиальный вирус, или РСВ, наиболее известен как зимняя угроза для младенцев, но он также отправляет в больницу многих пожилых людей и людей с ослабленным иммунитетом. Даже при наличии новых вакцин и защитных антител РСВ продолжает реинфицировановать людей снова и снова и может вызывать тяжёлое повреждение лёгких. В этом исследовании изучается малоизвестный вирусный белок — растворимая форма G-белка РСВ — и раскрывается, как он может незаметно подготавливать клетки лёгких к взрывному воспалению и помогать вирусу более эффективно распространяться по дыхательным путям.
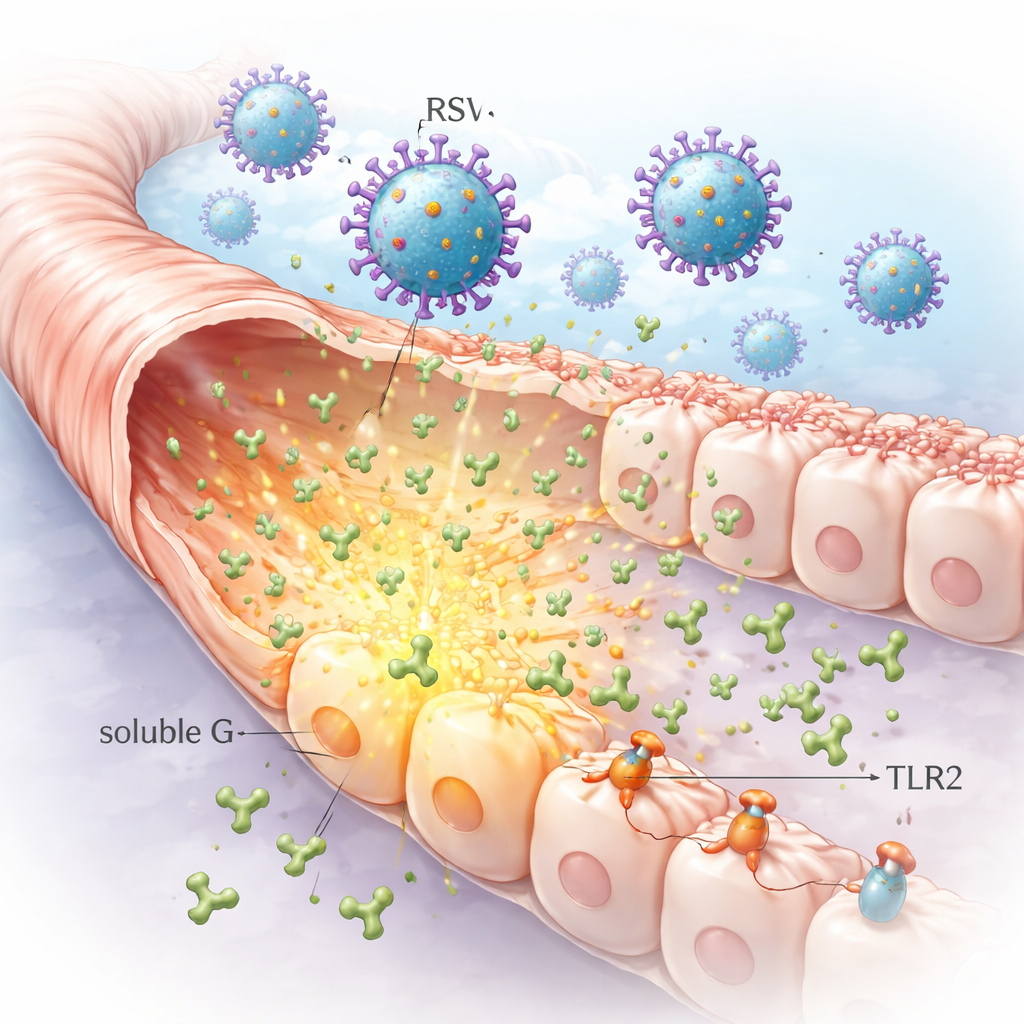
Секретируемый вирусный белок, который продвигается вперёд инфекции
РСВ несёт на своей поверхности прикрепляющий белок G, который помогает ему закрепляться на клетках дыхательных путей. Необычно то, что инфицированные клетки также выделяют в больших количествах свободную версию этого белка, известную как растворимый G. Исследователи показали, что инфицированные в лабораторных условиях клетки лёгких могут сбрасывать очень высокие уровни растворимого G в окружающую среду. Поскольку эта форма может диффундировать от исходного очага инфекции, она может достигать соседних клеток, ещё не инфицированных, создавая предпосылки для более широких изменений в эпителии лёгких, чем мог бы вызвать только сам вирус.
Растворимый G как двуадресный ключ к клеточной поверхности
Комбинируя микроскопию, биохимические тесты с вытягиванием взаимодействующих белков и ферментативную обработку, группа проследила, как растворимый G прикрепляется к клеткам. Они обнаружили, что он может связываться с углеводными цепями, называемыми гликозаминогликанами, а также с известным рецептором РСВ — CX3CR1. Критически важно, что растворимый G также связывается с распознающим паттерны молекулой на иммунных и дыхательных клетках — TLR2. Маленький мотив в белке G, известный как CX3C, оказался важным для прочного связывания с CX3CR1 и для эффективного привлечения TLR2. Это означает, что растворимый G сначала может слабо удерживаться на поверхности клетки, а затем взаимодействовать с более специфическими рецепторами, которые контролируют реакцию клетки на угрозы.
Подготовка клеток лёгких к воспалительному виду гибели
Вовлечение TLR2 растворимым G оказалось далеко не безвредным. В репортерных иммунных клетках и клеточных линиях человеческих лёгких растворимый G активировал сигнализацию MyD88–NF-κB, идущую за TLR2, что приводило к выделению провоспалительных медиаторов, таких как IL-6 и IL-8. Одновременно он усиливал синтез компонентов молекулярной «сигнальной системы» NLRP3-инфламмасомы и ферментов, генерирующих реактивные молекулы вроде оксида азота и кислородных радикалов. Само по себе это вызывало лишь небольшие повреждения. Но когда подготовленные клетки позже инфицировали РСВ, второе воздействие запускало полную сборку инфламмасомы, активацию каспазы‑1, образование пор в клеточной мембране и огневой тип гибели клетки, известный как пироптоз. Этот процесс пробивал дыры в клетках, вызывал выброс провоспалительного содержимого и сопровождался повышенным выпуском инфекционного вируса в культуральную среду.
Как эта цепная реакция может усугублять заболевания лёгких
Эффект, направленный на гибель, растворимого G был наиболее выражен в эпителиальных клетках дыхательных путей — тех самых клетках, которые РСВ предпочитает инфицировать — и зависел от NLRP3-инфламмасомы, поскольку специфический ингибитор NLRP3 в значительной степени восстанавливал жизнеспособность клеток. Напротив, некоторые иммунные клетки, богатые TLR2, но бедные по содержанию рецептора CX3CR1, не подвергались сильной лизисной гибели при тех же условиях. Этот паттерн указывает на то, что РСВ использует растворимый G, чтобы избирательно ослаблять и уничтожать защитный слой дыхательных путей, сохраняя при этом отдельные иммунные клетки, которые продолжают продуцировать сигналы. В результате создаётся среда в лёгких с большим количеством воспаления, клеточного детрита и возможностей для новых вирусных частиц уйти и заразить соседние клетки.
Что это значит для будущих терапий
Для неспециалиста главный вывод таков: РСВ опирается не только на прямое повреждение при вторжении вируса. Выделяя большие количества растворимого G-белка, он может «размягчать» соседние клетки через TLR2, делая их более склонными к воспалительной гибели и к разгулу вируса. Эта работа выделяет несколько звеньев в этой цепочке — сам растворимый G, его мотив CX3C, TLR2 и NLRP3-инфламмасому — как потенциальные мишени для лекарств. В принципе, терапии, блокирующие взаимодействие растворимого G с TLR2 или подавляющие активность NLRP3, могли бы снизить и повреждение лёгких, и распространение вируса. Такие подходы могли бы со временем дополнить существующие вакцины и антитела против РСВ, обеспечив лучшую защиту для самых молодых и наиболее уязвимых пациентов.
Цитирование: Meineke, R., Agac, A., Knittler, MC. et al. The soluble G protein of respiratory syncytial virus promotes viral dissemination via TLR2-mediated NLRP3 priming and pyroptosis. npj Viruses 4, 6 (2026). https://doi.org/10.1038/s44298-026-00172-x
Ключевые слова: респираторный синцитиальный вирус, растворимый G-белок, TLR2 инфламмасома, пироптоз, воспаление лёгких