Clear Sky Science · ru
Гормональная терапия в период менопаузы и риск нейропсихиатрических заболеваний: исследование методом менделевской рандомизации, направленное на лекарственные мишени
Почему это исследование важно
Многие женщины задаются вопросом, защищают ли гормоны, принимаемые вокруг менопаузы, их мозг или, наоборот, повышают риск проблем, таких как потеря памяти, депрессия или тревога. Врачи тоже не пришли к единому мнению, потому что прошлые исследования дали противоречивые результаты. В этой статье использован генетический подход, сходный по идее с долгосрочным рандомизированным испытанием, чтобы задать простой вопрос: когда эстрогеновые рецепторы мозга смещаются так, как это может происходить при гормональной терапии в менопаузе, меняется ли риск болезни Альцгеймера или распространённых психических расстройств?
Загадка вокруг гормонов и мозга
Женщины чаще, чем мужчины, испытывают депрессию, тревогу и болезнь Альцгеймера. Одна из основных гипотез заключается в том, что эстроген, ключевой женский половой гормон, формирует мозг на протяжении жизни и может его защищать — до тех пор, пока уровни не колеблются или не падают в середине жизни. В период менопаузального перехода многие женщины используют гормональную терапию (MHT), чтобы облегчить симптомы, такие как приливы и нарушения сна. Однако исследования о том, помогает ли MHT или вредит мозгу, расходятся: некоторые обнаружили повышенный риск деменции, другие — защитный эффект, а многие не показали явного влияния. Эти несоответствия могут быть связаны с короткой продолжительностью испытаний, разными препаратами и тем, что женщинам с более тяжёлыми симптомами гормоны назначают чаще.
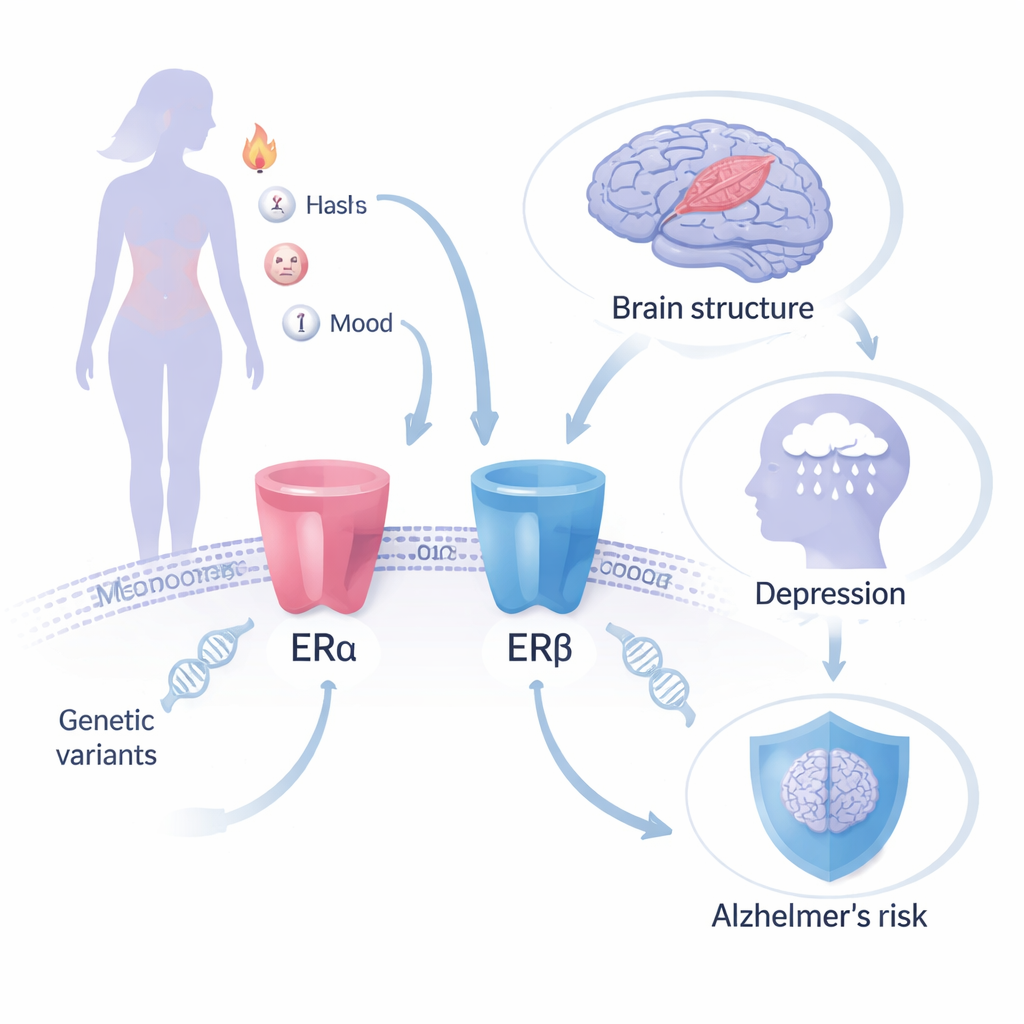
Использование генов как естественного эксперимента
Вместо того чтобы наблюдать женщин, принимающих гормоны, исследователи применили менделевскую рандомизацию — метод, использующий естественно встречающиеся генетические различия как замену пожизненному случайно присвоенному «лечению». Они сосредоточились на двух белках — эстрогеновых рецепторах ERα и ERβ — которые направлены активацией при MHT. Конкретные генетические варианты в генах, кодирующих эти рецепторы (ESR1 и ESR2), известны своими эффектами на «вторичные» признаки, которые изменяются при действии эстрогена, например плотность костной ткани, уровень белка крови, переносящего половые гормоны, и уровень гемоглобина. Отслеживая, как эти варианты, связанные с рецепторами, соотносятся с крупными генетическими наборами данных по болезни Альцгеймера, структуре мозга, депрессии и тревоге, команда смогла оценить, как изменение активности каждого рецептора может влиять на долгосрочный риск для мозга и психического здоровья.
Что показали генетические данные
Авторы построили три генетических инструмента: два, отражающих активность ERα (через варианты, связанные с плотностью костей и с глобулином, связывающим половые гормоны), и один, отражающий активность ERβ (через вариант, связанный с гемоглобином). Затем они сопоставили эти инструменты с одними из крупнейших доступных исследований ассоциаций по всему геному (GWAS) по болезни Альцгеймера, показателям МРТ мозга (общая серая масса, объём гиппокампа и «пятна» в белом веществе, связанные со старением), депрессии и тревоге. В целом они не нашли убедительных доказательств того, что генетически смоделированные изменения в любом из эстрогеновых рецепторов существенно меняют риск болезни Альцгеймера или влияют на перечисленные меры структуры мозга. Несколько слабых сигналов об изменениях в сером веществе или объёме гиппокампа не выдержали статистической коррекции, что указывает на то, что они, вероятно, случайны, а не отражают истинный биологический эффект.
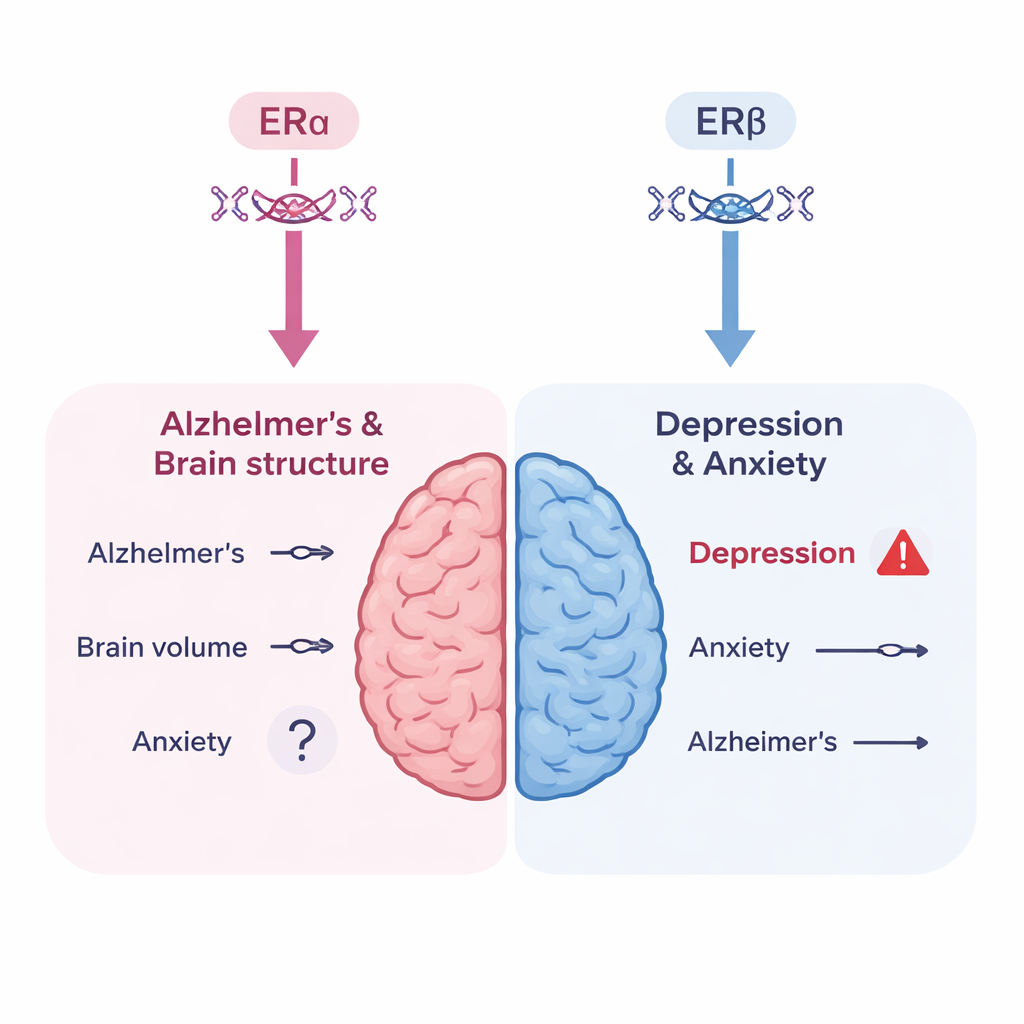
Тревожный знак для риска депрессии
Ситуация оказалась иной для настроения. При рассмотрении активности ERβ, захваченной генетическим прокси на основе гемоглобина, наблюдалась статистически значимая связь с повышенным риском депрессии. Это соответствует известному распределению активности ERβ в мозге — в таких областях, как гиппокамп и таламус, которые существенно участвуют в регуляции настроения. Авторы, однако, предупреждают, что прокси на основе гемоглобина не идеален: низкий уровень гемоглобина сам по себе может вызывать усталость и пониженное настроение, что может запутывать интерпретацию. Они не обнаружили сильных генетических доказательств того, что активность ERα сама по себе повышает риск депрессии, и нашли лишь предположительный, недоказательный намёк на связь ERα с тревогой. Важно отметить, что генетические эффекты, действующие постоянно с рождения, не идентичны началу гормональной терапии в среднем возрасте, поэтому эти результаты не следует рассматривать как прямой прогноз для какой‑либо конкретной схемы MHT.
Что это означает для женщин и их врачей
Если перевести результаты на практические решения, это исследование указывает, что воздействие на эстрогеновые рецепторы способом, сходным с MHT, явно не увеличивает и не уменьшает пожизненный риск болезни Альцгеймера и не вызывает крупных изменений в структуре мозга, по крайней мере в популяциях европейского происхождения. Одновременно вывод о связи ERβ с депрессией подчёркивает, что гормонозависимые мозговые цепи связаны с настроением, и что разные эстрогеновые рецепторы могут иметь разные последствия для психического здоровья. Эта работа не заменяет клинические испытания, но служит мощной генетической «проверкой реальности», которая может помочь уточнить будущие гормональные терапии и направить исследования в сторону более безопасных и персонализированных подходов для женщин в период менопаузы.
Цитирование: Schindler, L.S., Gill, D., Oppenheimer, H. et al. Menopausal hormone therapy and risk of neuropsychiatric disease: a drug target Mendelian randomisation study. npj Womens Health 4, 10 (2026). https://doi.org/10.1038/s44294-026-00130-1
Ключевые слова: гормональная терапия в период менопаузы, эстрогеновые рецепторы, болезнь Альцгеймера, риск депрессии, менделевская рандомизация