Clear Sky Science · ru
Всеобъемлющая геномная структура для выявления генов, предрасполагающих к раку молочной железы или яичников с дефектом гомологичной рекомбинации
Почему в некоторых семьях выше риск рака
У многих женщин с раком молочной железы или яичников в семейном анамнезе отмечается повышенный риск заболевания, однако генетическое тестирование нередко не дает ясного объяснения. Этот пробел, иногда называемый «пропавшей наследственностью», лишает семьи ответов и может ограничивать доступ к персонализированным скринингу или лечениям, таким как таргетные препараты. В этом исследовании авторы поставили цель разработать новый, более мощный способ поиска скрытых генов риска рака в нашей ДНК — путем объединения нескольких типов геномных и клинических данных вместо их разрозненного анализа. 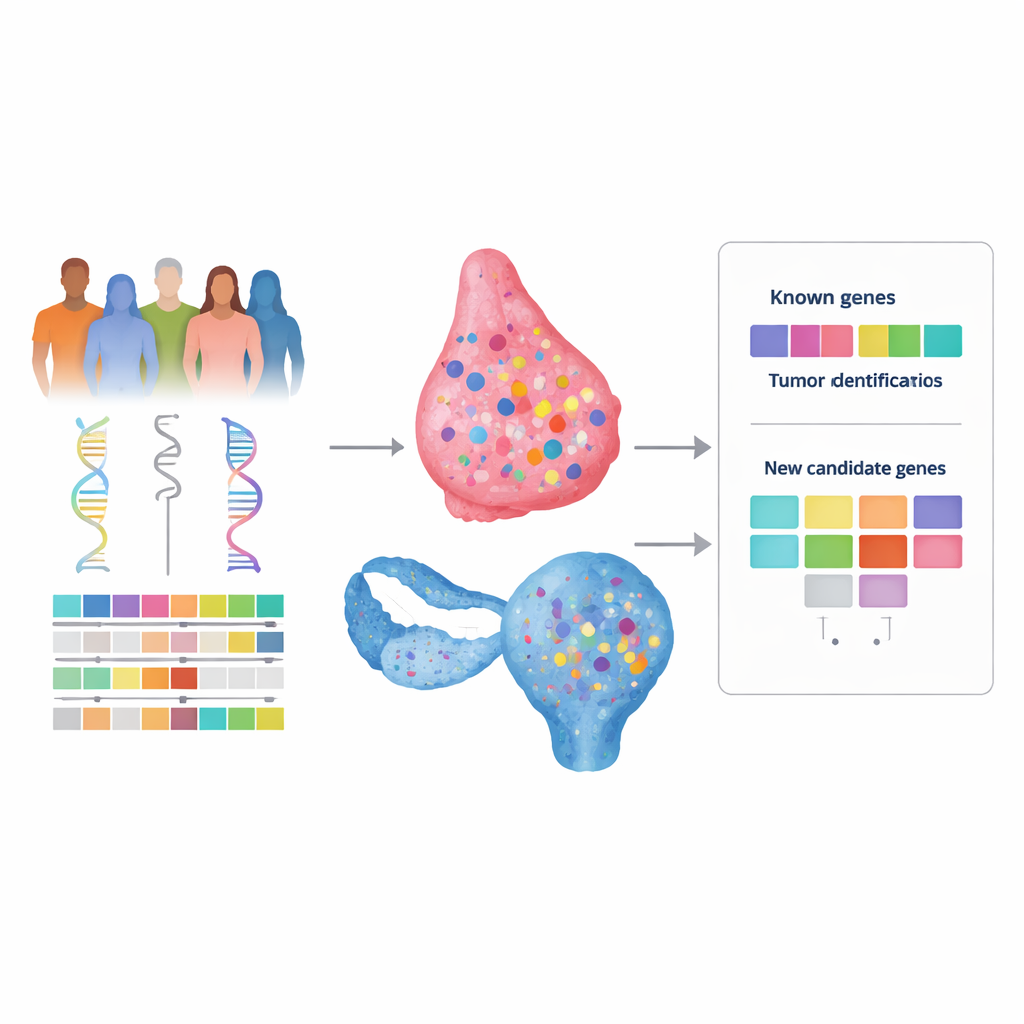
Поиск «отпечатка» дефектной репарации ДНК
Исследователи сосредоточились на конкретном механизме репарации повреждений ДНК, известном как гомологичная рекомбинация, который обычно исправляет опасные разрывы в генетическом материале. Когда эта система дает сбой, в клетках накапливается характерный «мутативный сигнатур» — специфический рисунок изменений в ДНК опухоли, действующий как молекулярный отпечаток. Этот профиль особенно часто встречается при некоторых трудноизлечимых формах рака молочной железы и яичников. Авторы предположили, что если опухоль демонстрирует такой отпечаток, то, вероятно, потеряны обе рабочие копии какого‑то гена репарации ДНК, известного или неизвестного, и это может быть прослежено до наследственной мутации в этом гене.
Создание объединенной генетико‑клинической структуры
Чтобы проверить эту идею, авторы проанализировали ДНК сотен пациентов с раком молочной железы и яичников из The Cancer Genome Atlas, который содержит как кровь (унаследованные варианты), так и опухолевую (приобретенные) генетическую информацию вместе с клиническими данными. Они обследовали весь экзом — белоккодирующую часть генома — в поисках редких наследственных вариантов, выглядящих вредоносными, которые также сопровождались «вторым ударом» в опухоли, например потерей оставшейся здоровой копии. Для каждого гена затем оценивали, встречаются ли такие двухударные события чаще в опухолях с сигнатурой дефекта репарации, чем в опухолях без нее. Важно, что они не ограничивались заранее заданной панелью генов, что позволило выявиться неожиданным кандидатам.
Проверка работоспособности метода и поиск новых подозреваемых
В качестве проверки концепции предложенная структура правильно выделила хорошо известные гены BRCA1 и BRCA2 как тесно связанные с сигнатурой дефекта репарации в обоих типах рака, подтвердив ожидаемое поведение подхода. В случае рака молочной железы она также указала на дополнительный ген THBS4 и предположила возможную роль генов KIF13B и TESPA1. Однако детальный разбор отдельных случаев показал, что изменения в THBS4 часто сосуществовали с другими, более установленными событиями, связанными с репарацией, что делает его менее убедительным драйвером. 
Фокус на не объясненных опухолях с высоким риском
Чтобы выйти за рамки статистики, исследователи включили клинические детали, такие как подтип опухоли, возраст при диагнозе и происхождение пациента. Они сосредоточились на пациентах, чьи опухоли явно демонстрировали сигнатуру дефекта репарации и принадлежали к клиническим группам, уже ассоциированным с этой биологией — базальноподобный рак молочной железы и высокодифференцированный серозный рак яичников — но при этом не имели известных событий типа BRCA. У этих пациентов повторно искали наследственные варианты с «вторым ударом», на этот раз в пределах широкой кураторской подборки генов, связанных с раком и ремонтом ДНК. Такой «клинико‑геномный» подход выделил несколько генов, участвующих в репарации двунитевых разрывов ДНК и в тесносвязанном пути фанconiанемии, включая RAD51B, RAD54B, RAD54L, FANCD2 и другие, которые выглядят правдоподобными новыми участниками наследственного риска.
Что это значит для пациентов и будущих исследований
Авторы не утверждают, что окончательно доказали новые гены риска рака; число затронутых пациентов для каждого кандидатного гена пока невелико, и потребуются более крупные и разнообразные когорты, чтобы подтвердить их роль. Вместо этого они предлагают повторно используемый план действий: способ объединять унаследованную и опухолевую ДНК, характерные мутативные отпечатки и клинические признаки для систематической приоритизации генов, которые могут лежать в основе не объясненной семейной предрасположенности. Со временем применение этой структуры к большим наборам данных и к другим типам рака может сократить разрыв «пропавшей наследственности», уточнить панели генетического тестирования и помочь большему числу пациентов понять их личный риск и варианты профилактики и таргетной терапии.
Цитирование: Camacho-Valenzuela, J., Matis, T., Roca, C. et al. A comprehensive genomic framework for identifying genes predisposing to homologous recombination repair-deficient breast or ovarian cancer. BJC Rep 4, 15 (2026). https://doi.org/10.1038/s44276-026-00218-w
Ключевые слова: дефицит гомологичной рекомбинации, генетика рака молочной железы, рак яичников, гены репарации ДНК, склонность к раку