Clear Sky Science · ru
Оценка STAR (stroma–tumor AI risk): связь доли стромы, определённой ИИ, с выживаемостью пациентов добавляет прогностическую ценность сверх KELIM при эпителиальном раке яичников
Почему «окружение» вокруг опухоли имеет значение
Когда мы думаем о раке, обычно представляем себе массой «бунтующих» клеток. Но опухоли существуют в загруженном окружении из поддерживающей ткани, кровеносных сосудов и иммунных клеток, называемом стромой. В этом исследовании поставлен простой, но мощный вопрос: можно ли с помощью баланса между опухолевыми клетками и окружающей их тканью — измеренного искусственным интеллектом (ИИ) на обычных микроскопических срезах — предсказать, у каких пациенток с раком яичников прогноз будет лучше или хуже ещё до начала лечения?
Новый способ чтения стандартных биопсийных срезов
У женщин с эпителиальным раком яичников материал обычно удаляют во время операции или получают при биопсии. Эти образцы окрашивают и изучают под микроскопом в каждой больнице. Исследователи сосредоточились на показателе, называемом соотношением опухоли и стромы (TSP): какая часть изображения занята поддерживающей тканью по сравнению с раковыми клетками. В ранних работах патологи оценивали это соотношение визуально и обнаружили, что опухоли с большим количеством стромы чаще ведут себя более агрессивно и устойчивы к стандартной платиновой химиотерапии. В настоящем исследовании команда использовала глубокую обучающуюся ИИ‑систему для автоматического измерения TSP на оцифрованных срезах, стремясь превратить ручную, отчасти субъективную задачу в быстрый и воспроизводимый показатель, доступный уже при постановке диагноза.
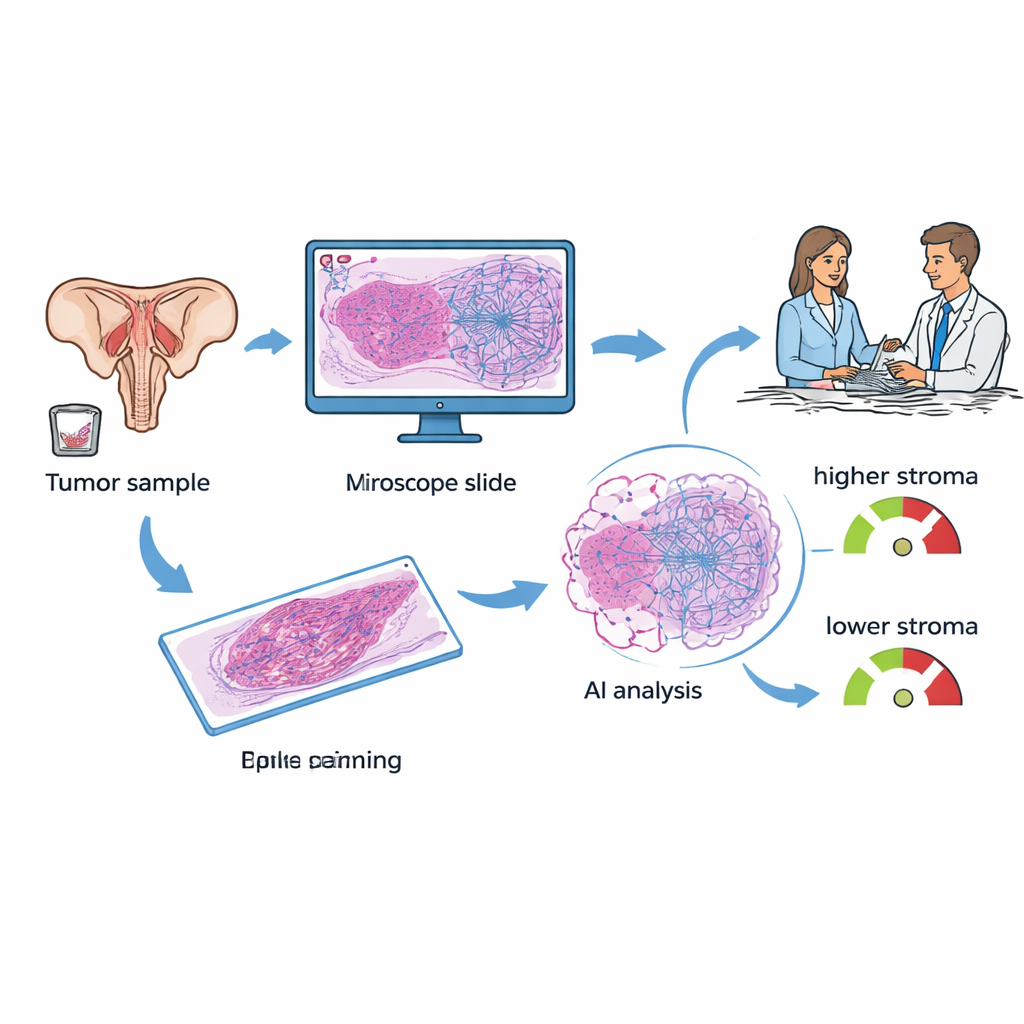
Сравнение анализа тканей ИИ с оценкой по крови
Сегодня одним из широко обсуждаемых инструментов при раке яичников является KELIM — показатель, основанный на скорости снижения в крови маркера CA‑125 в первые 100 дней химиотерапии. KELIM недорог и полезен, но его можно вычислить только после нескольких недель лечения, и не у всех пациентов есть достаточное число ранних анализов крови для расчёта. Исследователи собрали данные 89 женщин, пролеченных в одном онкологическом центре, у которых имелись и срезы ткани, и по крайней мере три измерения CA‑125. Для каждой пациентки рассчитали KELIM, патолог маркировал области опухоли на срезах, а затем модель ИИ оценивала TSP, классифицируя каждое исследование как «низкая строма» (менее 50% стромы) или «высокая строма» (50% и более).
ИИ сопоставим с экспертами и выявляет опухоли с более высоким риском
Оценка ИИ тесно согласовывалась с выводами опытных патологов: в 94% случаев автоматическая классификация TSP совпадала с ручной, что считается отличным уровнем согласия. При анализе исходов пациенток выяснилось, что у женщин с опухолями, признанными ИИ «высокая строма», общей выживаемости была существенно хуже, чем у пациенток с «низкой стромой». В статистическом выражении высокий TSP почти вдвое увеличивал риск смерти в период наблюдения, и этот эффект сохранялся даже после учёта показателя KELIM. Напротив, в этой реальной когорте пациентов KELIM был связан с резистентностью опухолей к платиновым препаратам, но явно не коррелировал с продолжительностью жизни пациенток.
Что это может значить для принятия лечебных решений
Поскольку TSP можно измерить по обычным срезам, взятым при постановке диагноза, ИИ‑оценка TSP даёт возможность оценить риск до начала химиотерапии, потенциально на месяцы раньше, чем KELIM. Результат «высокая строма» может предупредить клиницистов о более агрессивном и труднолечимом характере опухоли, побуждая к более частому наблюдению, более раннему рассмотрению дополнительных терапий или иным хирургическим стратегиям. Метод также относительно недорог: он опирается на существующие изображения патологии и программную модель, а не на новые лабораторные тесты. Авторы утверждают, что автоматизированный TSP может дополнять другие маркеры, такие как генетические тесты и динамика CA‑125, уточняя прогноз без значительного лишнего бремени для пациенток или лабораторий патологии.
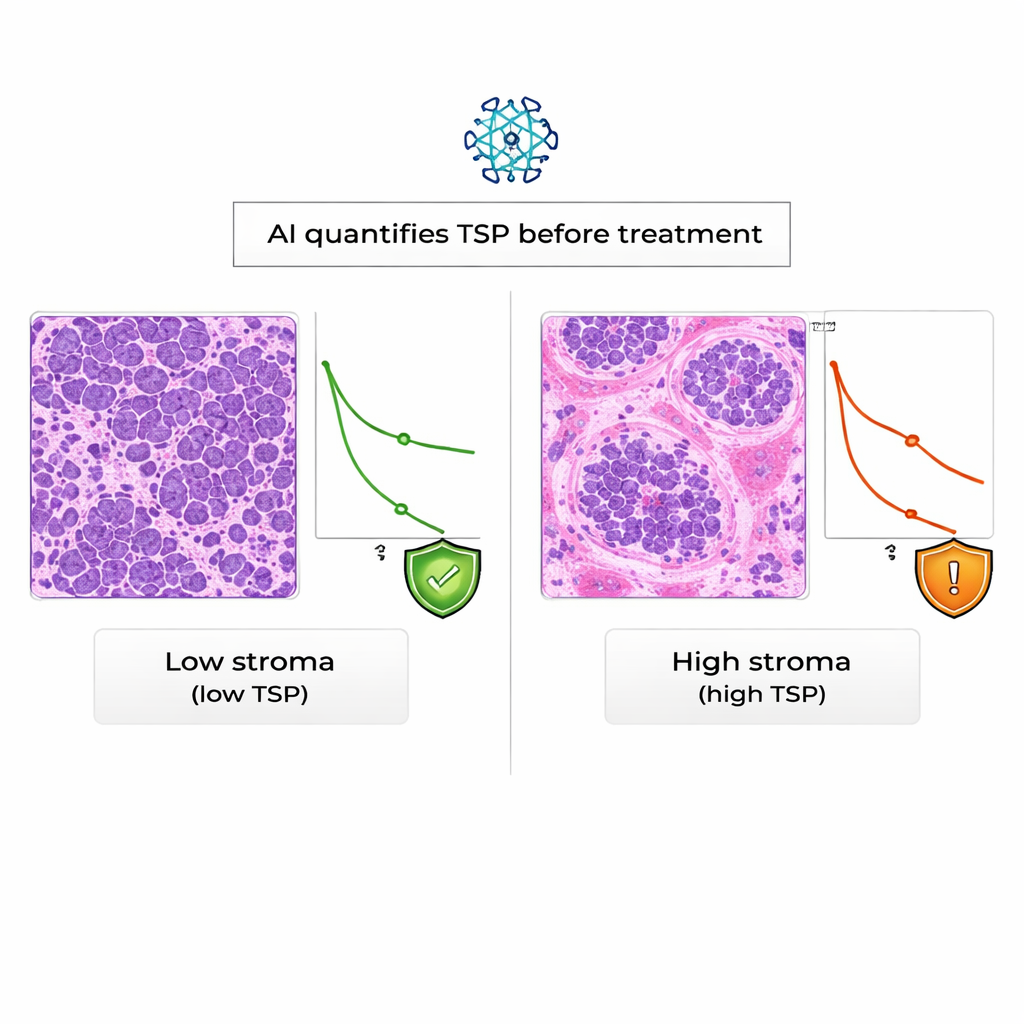
Взгляд в будущее: более умное и раннее руководство для пациенток
Для неспециалиста главный вывод таков: не все раки яичников одинаковы, и поддерживающая ткань вокруг опухоли несёт важные подсказки о том, как будет развиваться заболевание. Это исследование показывает, что ИИ надёжно считывает эти подсказки на стандартных биопсийных срезах и что опухоль с большим содержанием стромы, как правило, связана с худшей выживаемостью, независимо от существующих показателей по крови. Хотя нужны более крупные и разнообразные исследования, прежде чем подход станет частью рутинной практики, TSP, полученный с помощью ИИ, выглядит многообещающим как ранний предвестник, который может помочь врачам более точно подбирать лечение и дать пациенткам более ясные ожидания с самого начала.
Цитирование: Aggarwal, A., Madill, M., Jana, M. et al. STAR (stroma-tumor AI risk) assessment: association of AI-derived tumor-stroma proportion with patient survival provides added prognostic value beyond KELIM in epithelial ovarian cancer. BJC Rep 4, 4 (2026). https://doi.org/10.1038/s44276-026-00205-1
Ключевые слова: рак яичников, искусственный интеллект, опухолевая микроокружение, прогностический биомаркер, цифровая патология