Clear Sky Science · ru
Синергия бактериофага и меропенема против клинических изолятов Klebsiella pneumoniae, продуцирующих OXA-48
Почему крошечные вирусы могут спасти умирающие антибиотики
Больницы по всему миру сталкиваются с инфекциями, которые больше не поддаются нашим сильнейшим антибиотикам. Одним из худших преступников является бактерия Klebsiella pneumoniae, способная вызывать пневмонию, инфекции крови и мочевыводящих путей. В этом исследовании изучают, могут ли тщательно подобранные вирусы, атакующие бактерии — так называемые фаги — объединиться с мощным антибиотиком меропенемом, чтобы уничтожить высокорезистентные штаммы, угрожающие жизни пациентов.
Скрытный госпитальный возбудитель на подъеме
Klebsiella pneumoniae стала важным госпитальным супермикробом, поскольку многие штаммы научились противостоять карбапенемам — семейству антибиотиков, используемых в качестве последней линии защиты. Эти бактерии часто несут гены резистентности на крошечных кольцах ДНК, называемых плазмидами, которыми они могут обмениваться друг с другом, словно коллекционными карточками. Одна из таких плазмид, известная как pOXA-48, кодирует фермент, разрушающий карбапенемы, из-за чего лекарства вроде меропенема становятся в значительной степени бесполезными. По мере распространения этих плазмид по высоко‑рисковым бактериальным клонам в Европе и за её пределами стандартные схемы лечения становятся менее надёжными, делая даже рутинные медицинские процедуры более опасными.
Привлечение фагов как прицельных убийц
Поскольку новые антибиотики появляются медленно, исследователи обращаются к фаговой терапии — использованию вирусов, которые специфически инфицируют и убивают бактерии. В этом исследовании команда сосредоточилась на лизогенном фаге vB_Kpn_2-P4, который может инфицировать широкий набор клинических изолятов Klebsiella, собранных в испанских больницах. В лабораторных тестах этот фаг атаковал бактерии с несколькими различными механизмами резистентности к карбапенемам. Однако, как часто бывает и с антибиотиками, и с фагами, некоторые бактериальные клетки в конечном итоге выживали и снова размножались, что подчёркивает необходимость комбинированных стратегий, а не полагаться на одно единственное средство.
Когда лекарство и вирус работают лучше вместе
Затем исследователи проверили поведение меропенема и фага при совместном применении. Они культивировали двенадцать резистентных изолятов и подвергали их воздействию меропенема в одиночку, фага в одиночку или обоих одновременно, отслеживая рост в течение многих часов. Хотя при тестовых условиях все изоляты могли переносить меропенем, возникла поразительная закономерность: у штаммов, несущих плазмиду OXA‑48, комбинация фага и высоких доз меропенема вызвала резкий обвал численности бактерий с последующим отсутствием обнаруживаемого регрова. При более низких уровнях меропенема эти OXA‑48 штаммы всё равно демонстрировали сильное падение бактериальной нагрузки. Напротив, штаммы с другими ферментами резистентности не показали такого мощного совместного эффекта, что указывает на то, что некая особая черта плазмиды OXA‑48 делает бактерии особенно уязвимыми при одновременном воздействии обоих факторов.
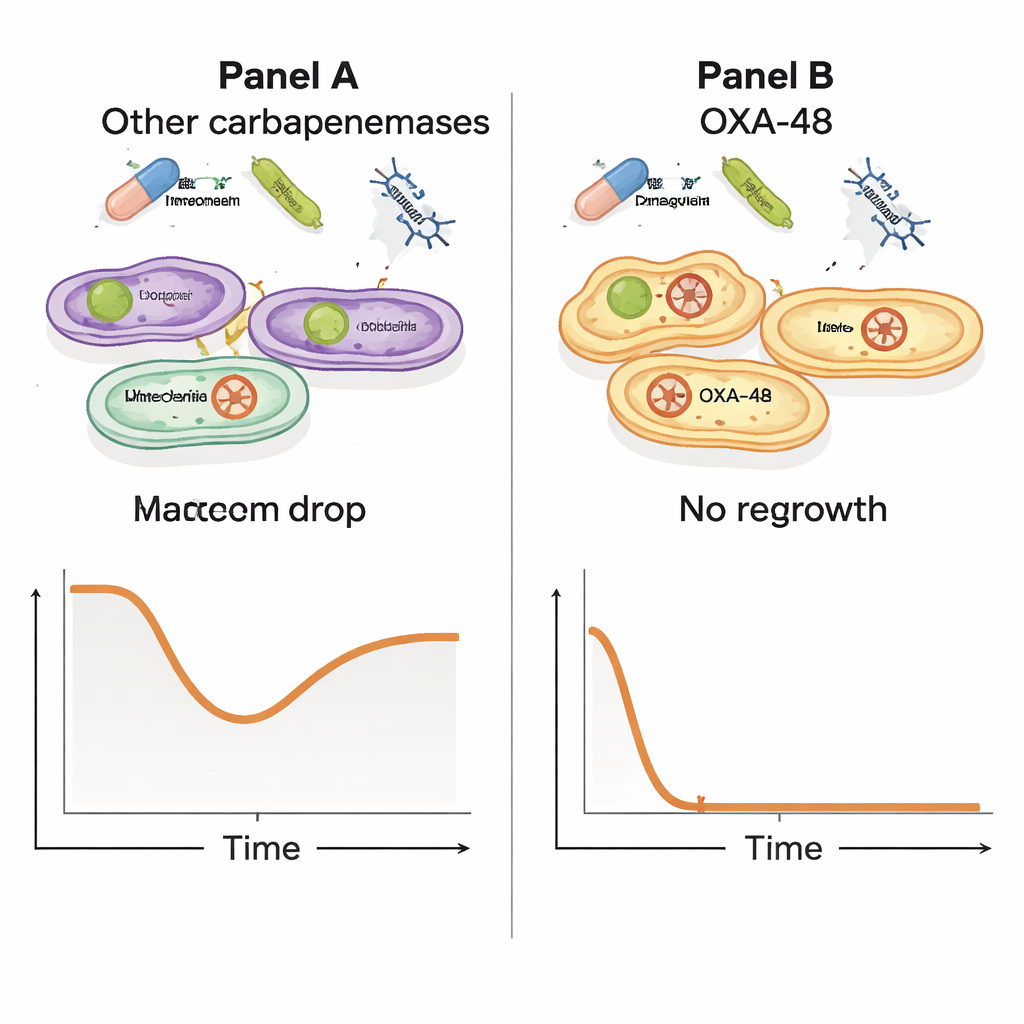
Отслеживание скрытого генетического помощника
Чтобы понять, почему синергия наблюдалась только у продуцентов OXA‑48, команда сравнила геномы различных бактериальных изолятов. Они выявили десятки генов, ассоциированных с синергетическим откликом, почти все из которых были сгруппированы на плазмиде pOXA‑48. Важно, что когда они выделили бактерии, эволюционировавшие к сопротивляемости фагу, эти выжившие всё ещё несли целый ген OXA‑48; они не просто избавились от плазмиды, чтобы уйти от угрозы. Это указывает на более тонкую картину, в которой плазмида, предоставляющая лекарственную резистентность, также налагает скрытые издержки на биологию бактерий — издержки, ставшие летальными, когда фаг и антибиотик атакуют вместе, перевешивая баланс в пользу уничтожения патогена.
Что это может означать для будущих лечений
Для неспециалистов главный вывод заключается в том, что те самые генетические уловки, которые бактерии используют, чтобы избегать наших лекарств, порой можно повернуть против них. В данном случае специфическая плазмида резистентности, по-видимому, делает некоторые штаммы Klebsiella исключительно чувствительными к комбинированной атаке подобранного фага и меропенема. Хотя эта работа проведена в лабораторных условиях и требуется больше исследований на животных моделях и у пациентов, она предполагает, что подбор правильного фага под конкретный профиль резистентности может вернуть к жизни антибиотики, казавшиеся бессильными. Вместо того чтобы заменять антибиотики, фаги могут стать умными союзниками, помогающими опередить супермикробы, которые когда‑то казались непобедимыми.
Цитирование: Cantallops, I., Ferriol-González, C., Barcos-Rodríguez, T. et al. Phage-meropenem synergy against OXA-48-producing Klebsiella pneumoniae clinical isolates. npj Antimicrob Resist 4, 12 (2026). https://doi.org/10.1038/s44259-026-00186-8
Ключевые слова: терапия бактериофагами, антибиотикорезистентность, Klebsiella pneumoniae, плазмида OXA-48, синергия с меропенемом