Clear Sky Science · ru
Глобальная реакция на воздействие антибиотиков выявляет ключевую роль нуклеотидного обмена в высокой толерантности к β-лактамам
Почему некоторые бактерии игнорируют наши сильнейшие антибиотики
Антибиотики должны уничтожать вредные бактерии, но многие инфекции упрямо сохраняются или возвращаются после лечения. В этой работе рассматривается одна недооценённая причина: некоторые бактерии умеют «зарываться» и временно переживать даже очень высокие дозы сильных препаратов, таких как пенициллин. Раскрывая, как эти микроорганизмы перестраивают свою внутриклеточную химию, чтобы выдержать атаку, исследователи указывают на новые пути восстановления эффективности существующих антибиотиков.
Скрытый приём выживания внутри инфекции
При воздействии β‑лактамных антибиотиков, например пенициллина, многие опасные грамотрицательные бактерии не умирают немедленно. Вместо этого они могут сбросить жёсткую клеточную стенку и превратиться в хрупкие округлые формы, называемые сферопластами. В этой форме они перестают размножаться, но остаются живыми и метаболически активными. После исчезновения препарата они восстанавливают стенку, возвращаются к обычной продолговатой форме и могут вновь вызвать инфекцию. Поскольку такая «толерантность» является ступенью на пути к полноценной антибиотикорезистентности и неудаче лечения, понимание механизмов выживания сферопластов важно для медицины будущего.
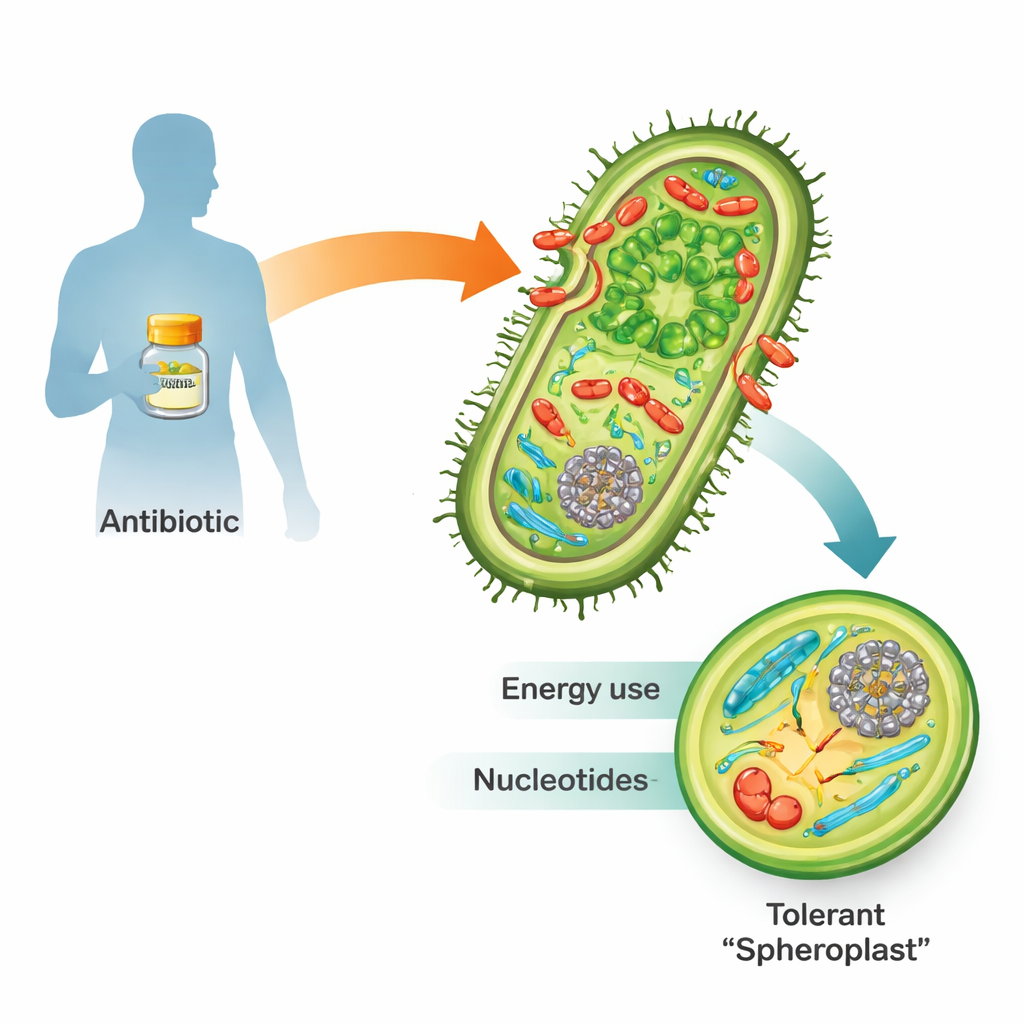
Подслушивая экстренные сигналы клетки
Авторы использовали Vibrio cholerae, бактерию, вызывающую холеру, в качестве модели, поскольку она исключительно терпима к β‑лактамам и легко поддаётся генетическим манипуляциям. Они подвергли бактерии воздействию пенициллина в десятикратной минимальной убивающей дозе и отслеживали ответ во времени с помощью двух мощных методов. Транскриптомика показала, какие гены включаются или выключаются, а метаболомика измеряла сотни малых молекул, обеспечивающих энергией и строительными блоками клетку. Вместе эти «мульти‑омные» подходы создали временную карту того, как толерантная клетка перестраивает внутреннюю работу во время атаки лекарством.
Перенаправление метаболизма и скрытая уязвимость
Данные выявили масштабные изменения в ключевых путях. Гены, отвечающие за строительство клеточной стенки, сильно активировались, что согласуется с попытками клетки ремонтировать повреждения и подготовиться к восстановлению. Также активировались системы теплового шока и стресс‑ответа, вероятно справляясь с неправильно свернутыми и окисленными белками, возникающими при стрессовом воздействии антибиотика. Одновременно центральный углеродный метаболизм сместился: некоторые звенья цикла ТCA (главного генератора энергии в клетке) усилились, тогда как ключевые промежуточные продукты гликолиза, такие как глюкозо‑6‑фосфат и фруктозо‑6‑фосфат, оказались резко истощены. Эти промежуточные соединения обычно питают и выработку энергии, и синтез клеточной стенки, что указывает на то, что непрерывный, расточительный «бесполезный цикл» материалов стенки истощает ресурсы.
Нуклеотиды под давлением
Самое заметное изменение касалось нуклеотидов — строительных блоков ДНК, РНК и многих энергетических молекул. Уровни многих нуклеотидов и их предшественников упали в клетках, обработанных пенициллином, хотя гены, ответственные за их синтез «с нуля», были сильно активированы. Одновременно гены, участвующие в «утилизации» или рециркуляции нуклеотидов, были подавлены, словно клетка пыталась сберечь оставшееся. Эти паттерны указывали на сильный нуклеотидный стресс у сферопластов. Когда исследователи намеренно нарушали пути поставки предшественников нуклеотидов — например пентозофосфатный путь — или блокировали синтез нуклеотидов другим препаратом, триметопримом, сочетание с β‑лактамами убивало значительно больше бактерий, чем любой из препаратов по отдельности. Такая сильная синергия наблюдалась не только у Vibrio cholerae, но и у высоко толерантных клинических штаммов Klebsiella pneumoniae и Escherichia coli.
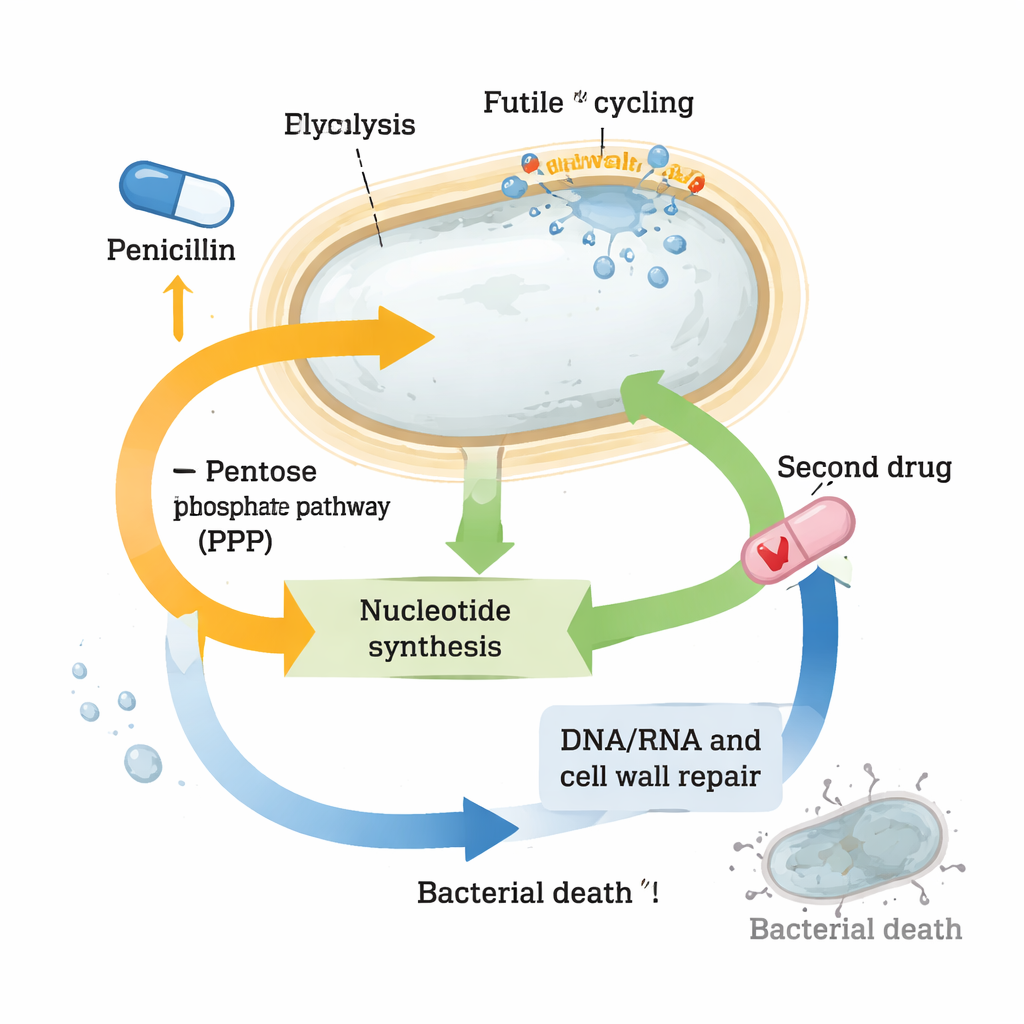
Преобразование химии выживания в терапевтическое преимущество
Несмотря на сильную перестройку метаболизма, толерантные сферопласты умудряются сохранять свой энергетический «валют» ATP относительно стабильным и избегать катастрофических повреждений, что помогает им переживать длительное воздействие антибиотиков. Но работа показывает, что при этом они доводят запасы нуклеотидов до предела. Это шаткое равновесие создаёт уязвимость: незначительное вмешательство в нуклеотидный обмен вторым препаратом рушит их защиту и возвращает мощное бактерицидное действие. Для неспециалистов главный вывод таков: некоторые бактерии выживают при приёме антибиотиков не потому, что препараты не поражают цели, а потому, что клетки быстро перенастраивают свою биохимию, чтобы переждать удар. Нахождение и использование слабых звеньев этой схемы выживания — здесь это нуклеотидный обмен — может позволить превратить старые антибиотики в эффективные комбинированные терапии, способные перехитрить даже высоко толерантные патогены.
Цитирование: Keller, M.R., Kazi, M.I., Saleh, A. et al. Global response to antibiotic exposure reveals a critical role for nucleotide metabolism in high-level β-lactam tolerance. npj Antimicrob Resist 4, 11 (2026). https://doi.org/10.1038/s44259-026-00183-x
Ключевые слова: толерантность к антибиотикам, β-лактамные антибиотики, нуклеотидный обмен, бактериальная персистенция, комбинации лекарств