Clear Sky Science · ru
Ослабление активации эпикарда и числа миофибробластов через ось Fbln2–Nupr1b стимулирует регенерацию сердца у данио-рерио
Почему некоторые сердца могут заживать сами
Когда у человека случается инфаркт, повреждённая мышца обычно покрывается жёстким рубцом, который фактически не восстанавливает ткань. Данио‑рерио, маленькие полосатые аквариумные рыбки, поступают иначе: они регенерируют сердечную ткань и со временем удаляют большую часть рубца. В этом исследовании поставлен на вид простоватый, но важный для медицины вопрос: как заживающее сердце «решает», когда нарастить рубец, а когда его убрать, чтобы могла снова вырасти мышца? Расшифровывая этот баланс у данио‑рерио, работа указывает на подходы, которые однажды могут помочь пострадавшим человеческим сердцам исправлять повреждение вместо развития сердечной недостаточности.
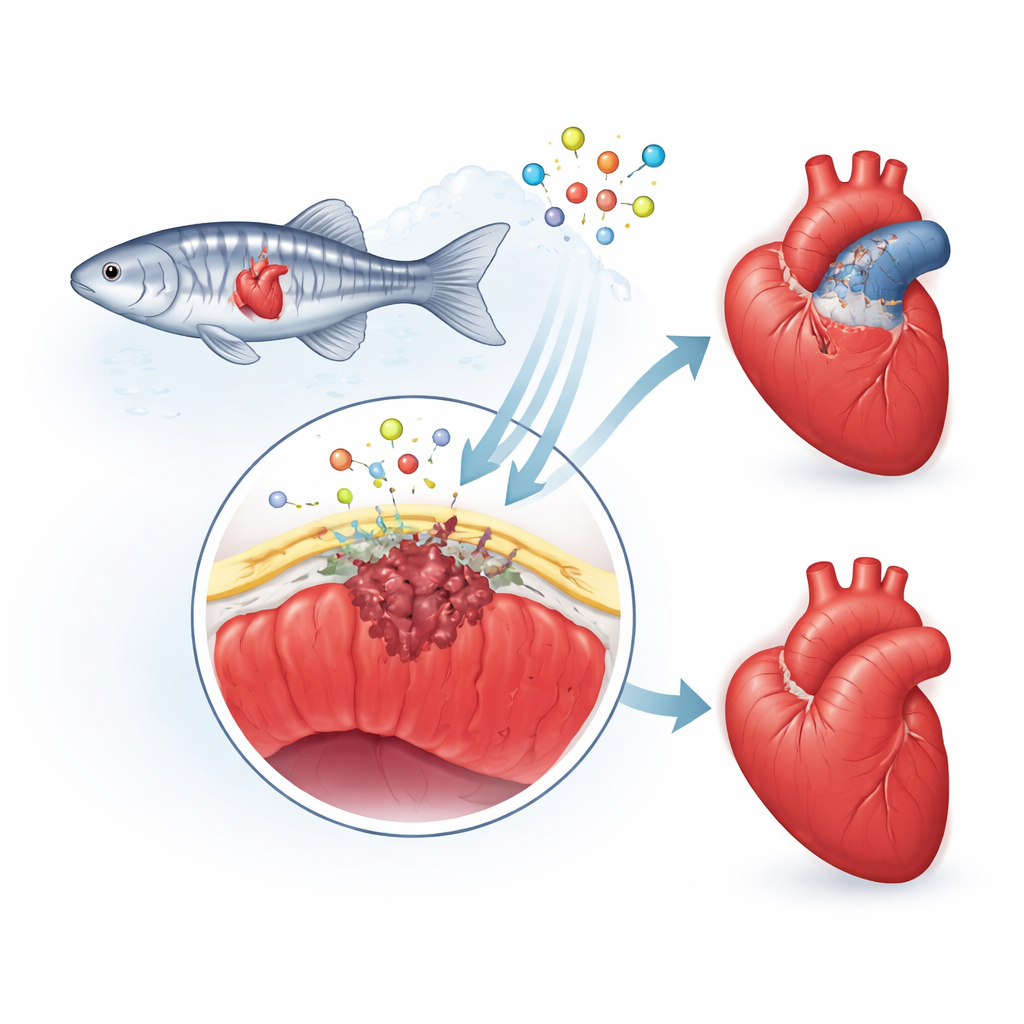
Защитная внешняя «кожа» сердца
Исследователи сосредоточились на эпикарде, тонком «слое‑коже», покрывающем сердце. После повреждения этот слой «пробуждается», клетки изменяют идентичность и часть из них мигрирует в область ранения. Там они становятся поддерживающими и рубцеобразующими клетками и выделяют химические сигналы, которые направляют рост новых кровеносных сосудов и сердечной мышцы. У людей ответ на повреждение часто чрезмерен и оставляет толстый постоянный рубец. У данио‑рерио, напротив, рубец временный и постепенно разрушается по мере возвращения здоровой мышцы. Команда предположила, что белок фибулин‑2 (Fbln2), присутствующий в внеклеточном каркасе сердца, помогает задавать скорость и силу этой эпикардиальной реакции.
Молекулярный регулятор степени рубцевания
С помощью генного редактирования у данио‑рерио учёные получили две разновидности животных с разным уровнем Fbln2: одну линию с пониженным Fbln2 и другую с полным отсутствием белка. Они травмировали сердца рыб при помощи зондов с замораживанием, моделируя инфаркт, и наблюдали за заживлением в течение недель и месяцев. При сниженных уровнях Fbln2 раннее деление клеток сердечной мышцы и выстилки сосудов ослабевало, но образовавшийся фиброзный рубец был меньше и легче поддавался ремоделированию. К трём месяцам такие сердца хорошо регенерировали и содержали мало коллагена — основного материала рубца. Напротив, у рыб с полным отсутствием Fbln2 наблюдалось более сильное подавление ключевого пути роста и рубцевания, связанного с семейством сигналов TGFβ, и значительно меньше рубцеобразующих клеток прямо под эпикардом. Их ранние рубцы тоже были меньше — но позже такие сердца не смогли удалить коллаген и в итоге сохраняли большие стойкие рубцы и демонстрировали слабую регенерацию.
Вглядываясь в изменения состояния эпикарда
Чтобы понять поведение эпикардиальных клеток на уровне отдельных клеток, команда использовала одноклеточное секвенирование РНК вскоре после травмы. Были идентифицированы несколько «состояний» эпикардных клеток: тихие клетки, недавно активированные, клетки в состоянии стресса, адаптирующиеся к низкому содержанию кислорода, и активно делящиеся клетки. У рыб с нормальным Fbln2 эпикардиальные клетки плавно переходили от тихого состояния через активацию к зрелым состояниям. У рыб с пониженным или отсутствующим Fbln2 этот прогресс тормозился: клетки задерживались на ранних стадиях, а более зрелые активированные популяции были недопредставлены, особенно у животных с полным дефицитом. Множество генов, которые обычно включаются при активации эпикарда и в ответ на сигналы TGFβ, были понижены, указывая на роль Fbln2 как «регулятора громкости» этого пути, определяющего, насколько эпикард склонен к формированию и ремоделированию рубца.
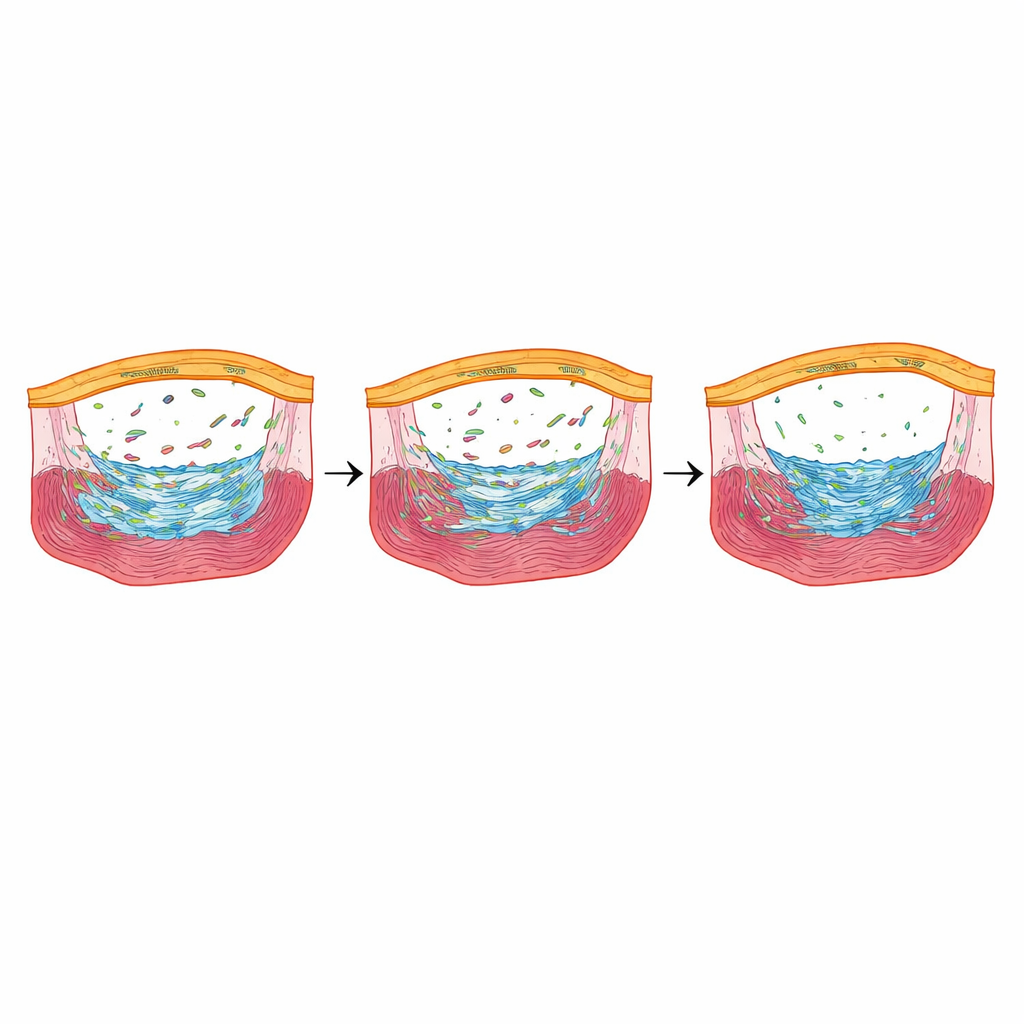
Ответчик на стресс, который тонко настраивает ремонт
Среди генов, наиболее существенно сниженных при понижении Fbln2, выделялся один: nupr1b, чувствительный к стрессу регулятор, активный в эпикардиальных клетках на ранних этапах заживления. Когда исследователи удалили nupr1b, данио‑рерио показали меньше эпикардиальных рубцеобразующих клеток и сниженное деление кардиомиоцитов, а через месяцы после травмы сохранялись крупные отложения коллагена — очень похоже на картину у рыб с полным отсутствием Fbln2. Поразительно, что при кратковременной индукции nupr1b только в эпикардиальных клетках рыб с пониженным Fbln2 количество рубцеобразующих клеток и пролиферация кардиомиоцитов восстановились, а поздний фиброз увеличился. Химическое блокирование рецепторов TGFβ снижало уровни nupr1b, что ставит nupr1b ниже по потоку в сигнальном каскаде Fbln2–TGFβ.
Что это значит для лечения человеческого сердца
В совокупности эти данные выявляют «эпикардиальную ось Fbln2–Nupr1b», которая помогает сердцам данио‑рерио балансировать между недостаточным и избыточным фиброзом. Слабое ослабление этой оси смягчает ранний взрыв рубцеобразования и способствует эффективному удалению рубца, тогда как полное её выключение нарушает регенерацию и оставляет жёсткий рубец. Для человеческой медицины важный урок таков: цель не в том, чтобы полностью подавить рубцевание, а в том, чтобы его настроить — сохранить достаточную структуру, чтобы предотвратить разрыв, но обеспечить, чтобы рубцовая ткань была временной и могла быть заменена здоровой мышцей. Понимание и, в конечном счёте, использование этой системы контроля у данио‑рерио может лечь в основу будущих терапий, которые подтолкнут повреждённое человеческое сердце к настоящей регенерации, а не к хроническому рубцеванию.
Цитирование: Kayman Kürekçi, G., Kaur Bajwa, G., Zhang, S. et al. Attenuation of epicardial activation and myofibroblast abundance via the Fbln2–Nupr1b axis stimulates cardiac regeneration in zebrafish. Nat Cardiovasc Res 5, 218–233 (2026). https://doi.org/10.1038/s44161-026-00785-8
Ключевые слова: регенерация сердца, фиброз, данио-рерио, эпикард, сигнальный путь TGF-бета