Clear Sky Science · ru
Селективная блокада активации латентного TGF-β1 подавляет тканевый фиброз при хорошей безопасности
Почему скрытая рубцевость имеет значение
Многие хронические заболевания незаметно повреждают органы, откладывая плотную рубцовую ткань — процесс, называемый фиброзом. Эти рубцы со временем могут подавлять нормальную функцию печени, почек, лёгких и даже окружать опухоли, где они также снижают эффективность современных противораковых иммунотерапий. Белок TGF-β1 стоит в центре этого процесса, но его повсеместное блокирование оказалось опасным. В этом исследовании описывается новое антитело под названием SOF10, созданное для блокировки только вредной активации TGF-β1 при сохранении его жизненно важных функций, и показавшее обнадёживающие результаты в моделях заболевания печени, почечной недостаточности и рака у животных.
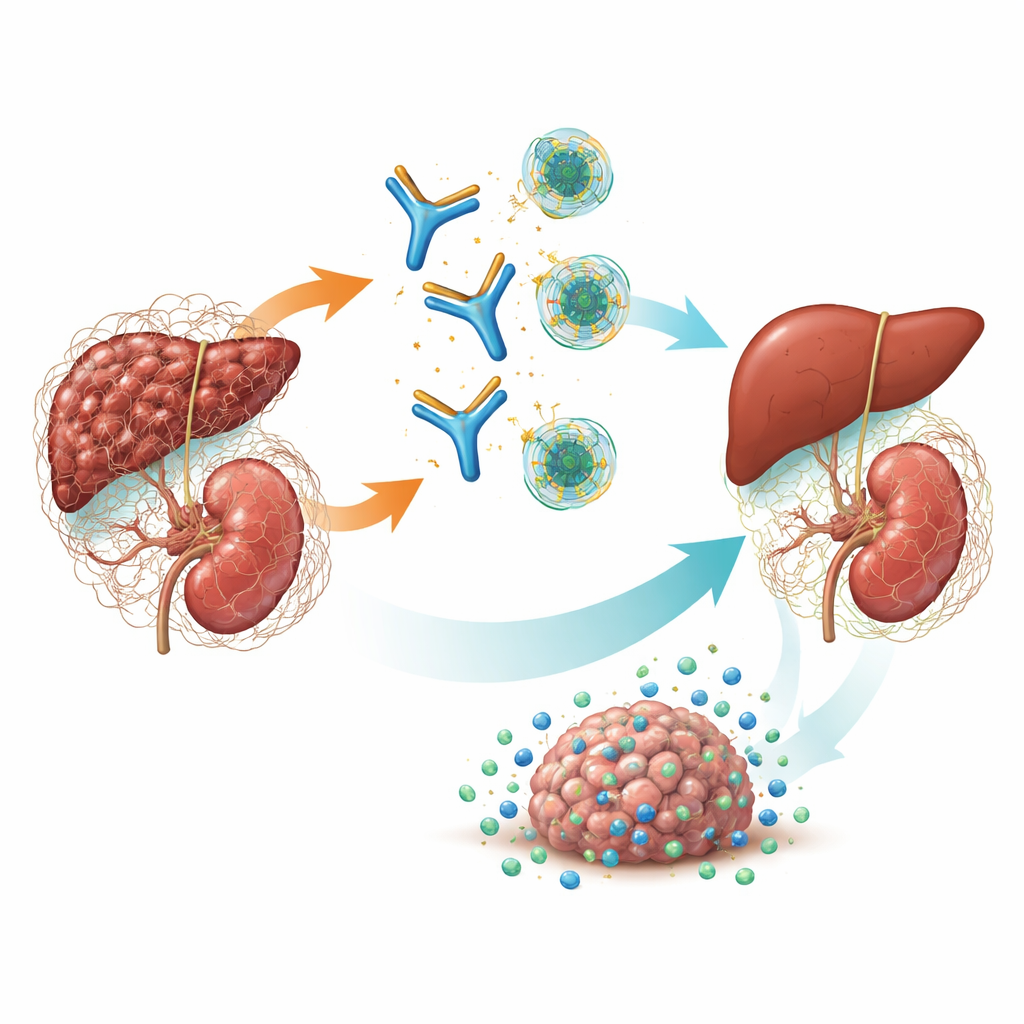
Главный переключатель рубцевания и рака
TGF-β — мощная сигнальная молекула, управляющая ростом клеток, заживлением и взаимодействием с иммунной системой. При хронических заболеваниях одна из форм — TGF-β1 — стимулирует фибробласты синтезировать избыточную соединительную ткань, что приводит к уплотнению и отказу органов. Она также формирует иммунносупрессивную фибротическую «скорлупу» вокруг опухолей, препятствуя доступу иммунных клеток и препаратов к раковым клеткам. Ранние препараты пытались подавить все три формы TGF-β одновременно, но такая «пан-блокада» вызывала серьёзные побочные эффекты — повреждение сердечных клапанов, кровотечения и кожные опухоли. Генетические исследования и предшествующие модели указывали на то, что именно TGF-β1 является главным виновником в фиброзе почек и во многих солидных опухолях, что даёт надежду, что прицельная блокада только этого изоформы может быть эффективной и безопаснее.
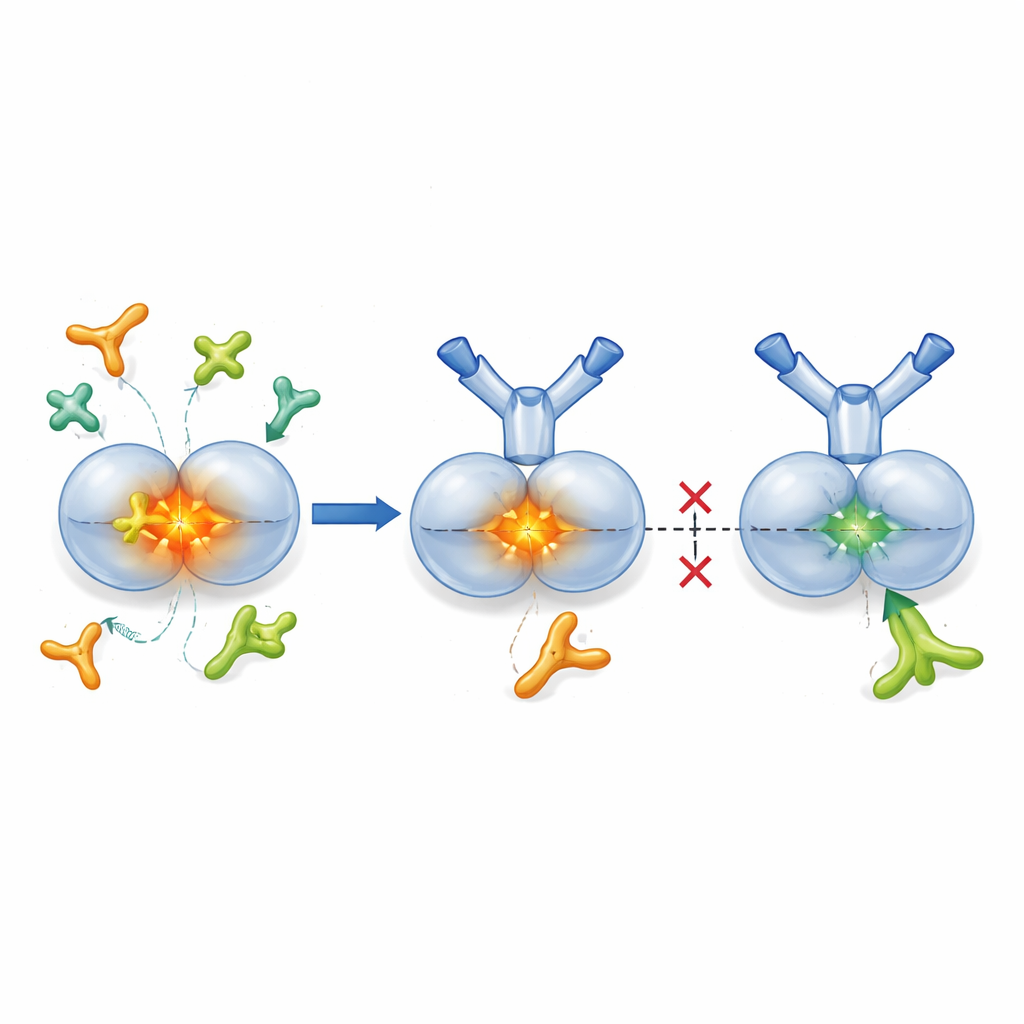
Закрепляя TGF-β1 в неактивной форме
TGF-β1 обычно синтезируется в «латентном» комплексе, где активное ядро обёрнуто партнёрным белком, удерживающим его в неактивном состоянии до необходимости. Протеазы и некоторые клеточные рецепторы — интегрины — могут открыть этот «пакет», выпуская активный TGF-β1 в окружающие ткани. Исследователи создали SOF10, гуманизированное антитело, которое связывает только латентную форму TGF-β1, а не активный гормон или другие изоформы. Структурные исследования методом рентгеновской кристаллографии показали, что SOF10 вклинивается в интерфейс между двумя половинами латентного комплекса, стабилизируя его подобно зажиму. В лабораторных тестах это препятствовало действию протеаз и одного интегрина (αvβ8) по высвобождению активного TGF-β1, оставаясь при этом в значительной степени неактивным в отношении другого интегрина (αvβ6), важного для поддержания иммунного баланса в здоровых тканях. Фактически SOF10 выборочно блокирует вредные пути активации, щадя ключевой гомеостатический путь.
Защита печени и почек от медленных повреждений
Чтобы выяснить, может ли такая селективная «зажимная» стратегия ограничивать рубцевание, команда проверила SOF10 в нескольких мышиных моделях. В быстрой модели диетозависимого жирового заболевания печени, прогрессирующего в фиброз, лечение SOF10 снижало экспрессию в печени генов, отвечающих на TGF-β, и генов синтеза коллагена, а также уменьшало уровень гидроксипролина — химического маркера накопленного рубца. В двух различных моделях почек — хирургической обструктивной модели, вызывающей интерстициальный фиброз, и генетической модели синдрома Олпорта, в которой развиваются и клубочковый фиброз, и почечная недостаточность — SOF10 снижал активность фибротических генов, уменьшал содержание коллагена и визуально сокращал площадь рубцовой ткани под микроскопом. В хронической модели Олпорта анализ крови показал улучшение функции почек; эти преимущества были сопоставимы с эффектом более широкого антитела против TGF-β, но при этом не сопровождались блокадой других изоформ TGF-β.
Освобождение иммунной системы внутри опухолей
Поскольку фибротическая ткань вокруг опухолей служит как физическим барьером, так и тормозом для иммунитета, исследователи проверили, улучшит ли SOF10 ответы на ингибиторы контрольных точек. В мышиных моделях рака молочной и толстой кишки, которые обычно слабо реагируют на анти–PD-L1 терапию, сочетание с SOF10 существенно замедляло рост опухолей, тогда как SOF10 или анти–PD-L1 по отдельности имели мало эффекта. Опухоли у животных, получавших комбинацию, содержали больше киллерных CD8 T-клеток и больше токсических ферментов, которыми они разрушают раковые клетки. Фибробласты, выделенные из этих опухолей, показывали снижение активности путей синтеза коллагена и матрикса и повышение активности путей интерферона и презентации антигена — сдвиг в сторону более иммуно-поддерживающего стромального микросреды. Эти изменения тесно напоминали эффекты при широкой блокаде TGF-β, что предполагает: нацеливание только на латентный TGF-β1 способно перенастроить опухолевую среду похожим образом.
Сигналы безопасности у животных
Поскольку ранние попытки широкой блокады TGF-β сталкивались с проблемами безопасности, команда провела 13-недельные токсикологические исследования на мышах и макаках-циноцефалах, вводя многократно высокие дозы SOF10. Препарат вел себя как типичное антитело в кровообороте, и в широком диапазоне доз не было признаков повреждения основных органов, отклонений в количестве клеток крови или нарушений функции сердца и лёгких. Наивысшие испытанные дозы — до 200 мг/кг каждые две недели у мышей и 100 мг/кг у макак — были определены как уровни без наблюдаемых вредных эффектов. Этот профиль безопасности поддерживает идею о том, что щадящее отношение к TGF-β2, TGF-β3 и активации через αvβ6 снижает риски, наблюдавшиеся при ранних, менее селективных подходах.
Что это может значить для пациентов
В совокупности полученные данные свидетельствуют о том, что закрепление TGF-β1 в его неактивной «скорлупе», а не полное уничтожение сигнального пути TGF-β, может уменьшать рубцевание в разных органах, улучшать функцию почек и делать упрямые опухоли более уязвимыми для иммунотерапии — и всё это при обнадеживающей безопасности в исследованиях на животных. Хотя для подтверждения этих преимуществ и наблюдения за долгосрочными эффектами необходимы клинические испытания у людей, SOF10 и сходные стратегии могут открыть новый путь лечения хронических фибротических заболеваний и некоторых видов рака, ослабляя вредоносное рубцевание и сохраняя при этом восстановительные и иммунорегулирующие функции тканей.
Цитирование: Kanamori, M., Sato, I., Koo, C.X. et al. Selective blockade of latent TGF-β1 activation suppresses tissue fibrosis with good safety. Commun Med 6, 131 (2026). https://doi.org/10.1038/s43856-026-01408-w
Ключевые слова: фиброз, TGF-beta1, моноклональное антитело, заболевания почек и печени, иммунотерапия рака