Clear Sky Science · ru
Прогнозирование исхода по пространственному белковому профилированию тройного-негативных раковых опухолей молочной железы
Почему важна «планировка» раковых клеток
Когда врачи рассматривают агрессивный рак молочной железы под микроскопом, они видят переполненный ландшафт: опухолевые клетки, иммунные клетки и поддерживающую ткань. Но до недавнего времени большинство тестов оценивало не то, где находится молекула, а сколько её присутствует. В этом исследовании показано, что физическое расположение белков и клеток в тройно-негативных раках молочной железы может предсказывать исход для пациентов, и предложен новый способ считывать эти пространственные шаблоны напрямую с детализированных изображений.
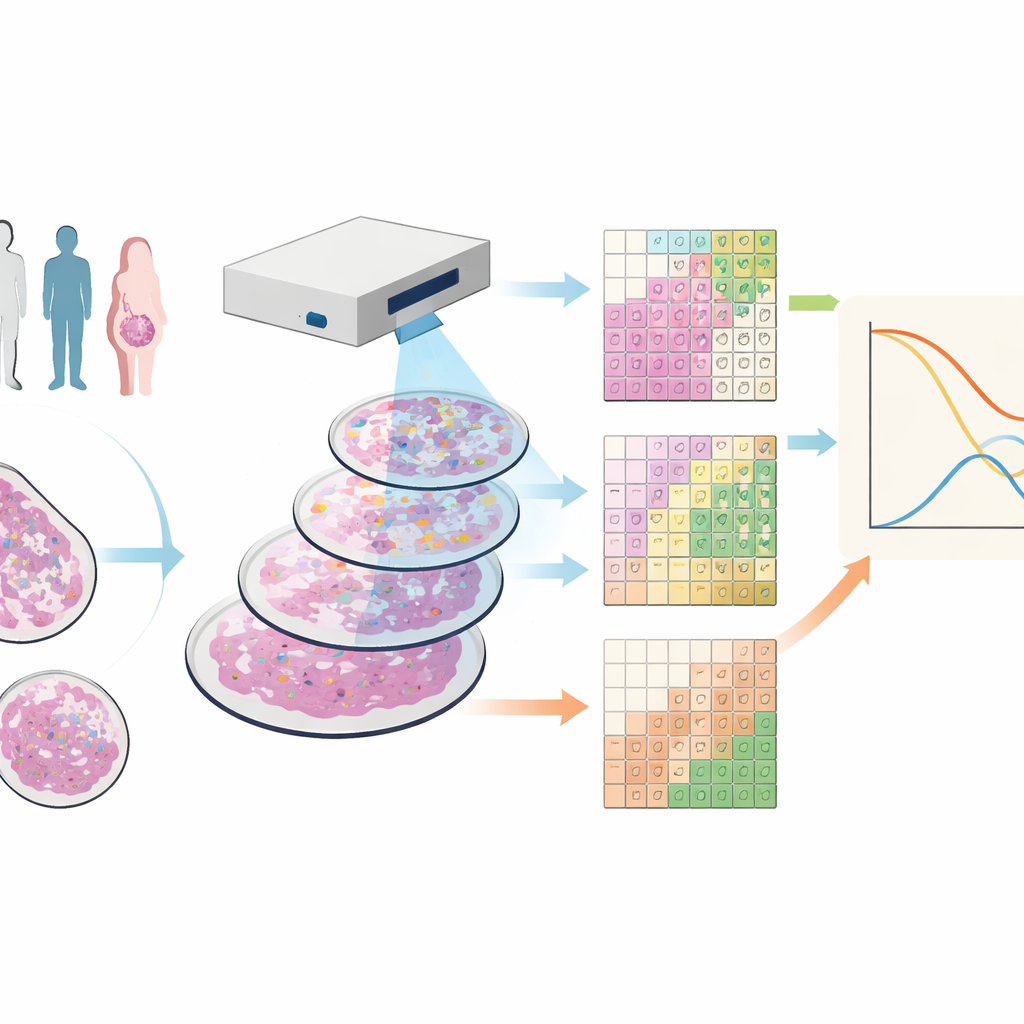
Видеть ткань рака во множестве цветов
Исследователи работали с образцами тканей от 88 человек с тройно-негативным раком молочной железы — формой болезни, лишённой распространённых мишеней для лекарств и часто имеющей плохой прогноз. Они использовали метод имиджинговой масс-цитометрии, при котором каждый образец окрашивают десятками антител с металлическими метками. Под специализированным сканером это даёт изображения, в которых каждая точка ткани несёт подробный «отпечаток» многих белков, одновременно выявляя опухолевые клетки, различные иммунные клетки, кровеносные сосуды и структурные волокна.
Разрезать изображение на плитки вместо клеток
Большинство современных инструментов пытаются обвести границы каждой клетки и затем классифицировать их по типам — процесс, который может быть подвержен ошибкам и медленным, особенно в тонких срезах ткани, где клетки частично обрываются. Команда вместо этого создала SparTile — метод, который пропускает этап обводки отдельных клеток. SparTile делит каждое изображение на множество маленьких перекрывающихся квадратов, или плиток, и применяет математические приёмы для обнаружения повторяющихся шаблонов сочетаний белков внутри этих плиток. Сначала плитки группируются в широкие регионы — опухоль, опорная ткань (строму) или зоны, богатые иммунными клетками — а затем каждый регион дополнительно делится на более специфические «микроокружения», каждое со своим набором белков и соседних типов клеток.
Скрытые «районы» связаны с исходом пациентов
После картирования этих микроокружений учёные измерили, насколько часто каждый шаблон встречался в образце каждого пациента, и сопоставили это с долгосрочной выживаемостью. Выявилось несколько заметных связей. Одно опухоле-центрическое микроокружение, богатое белком MX1 и маркерами миелоидных иммунных клеток, ассоциировалось с существенно более высокой риском смерти. Другой опухолевый шаблон, отмеченный виментином — признаком перехода опухолевых клеток к более подвижному, инвазивному состоянию — также сильно коррелировал с плохим прогнозом. Напротив, области, доминируемые определёнными Т-клетками, были связаны с лучшими исходами, тогда как регионы, богатые В-клетками, показали более слабый эффект, возможно, потому что они были редки в небольших анализируемых тканевых кернах.
Расстояние между опухолевыми и иммунными клетками как сигнал тревоги
Помимо наличия отдельных микроокружений, имели значение и их пространственные отношения. Команда оценивала, насколько плотно опухолевые регионы и миелоидные иммунные регионы располагались рядом друг с другом, вычисляя статистическую меру перекрытия их белковых сигналов в пространстве. Пациенты, у которых миелоидно-богатые участки были вплетены прямо среди опухолевых клеток, как правило, имели худший исход, чем те, у кого эти популяции были более разобщены. Эта мера «расстояния» оставалась сильным предиктором риска даже после учёта стандартных клинических факторов, и её значимость подтвердилась при проверке на двух независимых наборах изображений рака молочной железы из других исследовательских групп.
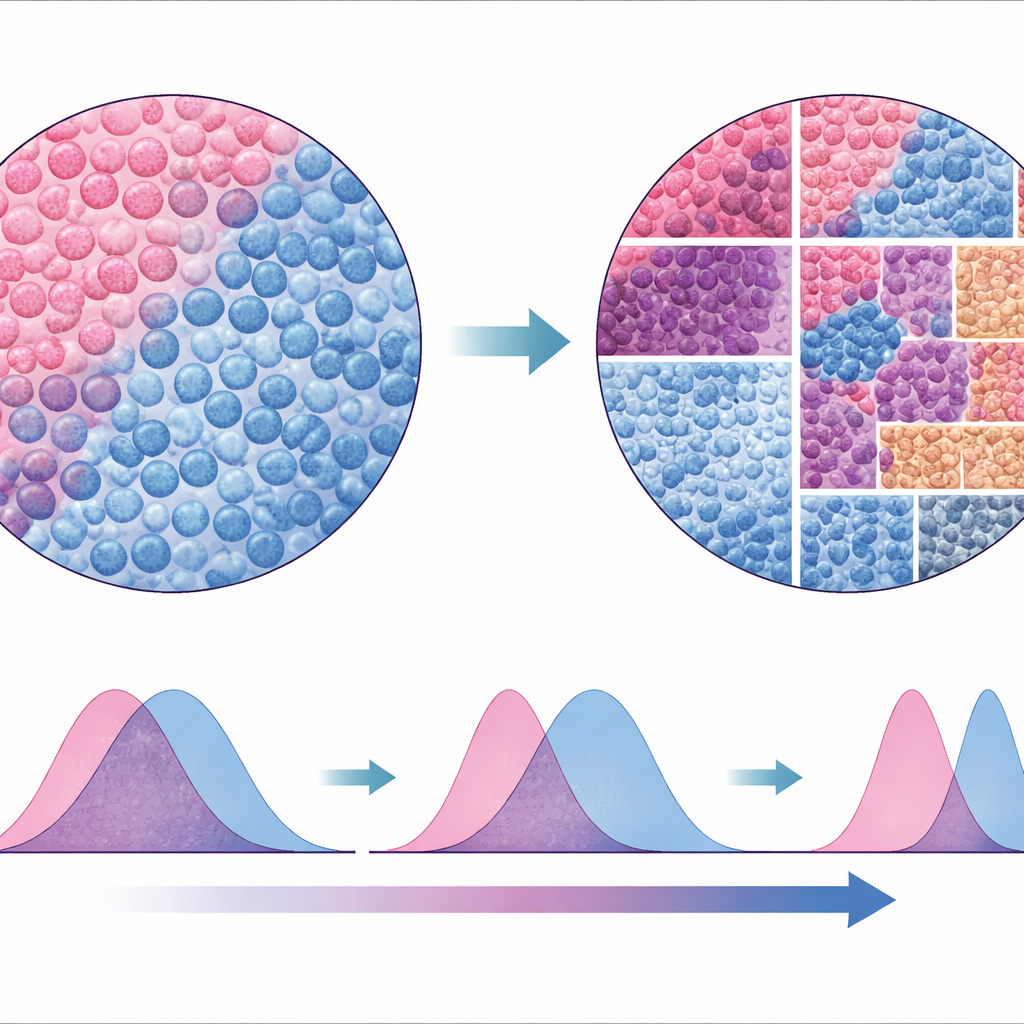
Новый способ читать ландшафт опухоли
Чтобы оценить устойчивость подхода, авторы сравнили SparTile с традиционными методами, которые опираются на сегментацию и классификацию отдельных клеток с последующим построением их соседств. Хотя клеточно-ориентированные анализы восстановили часть тех же шаблонов, они оказались менее согласованными между наборами данных и менее надёжными при обнаружении некоторых рискованных микроокружений, таких как включающие MX1 и миелоидные клетки. Поскольку SparTile работает напрямую с исходными белковыми изображениями, он избегает многих предположений и технических сложностей методов «клетка за клеткой», при этом его можно комбинировать с ними позднее, когда для планирования экспериментов или терапии понадобятся детальные сведения о типах клеток.
Что это значит для пациентов и будущей помощи
Эта работа показывает, что важны не только «ингредиенты», но и «планировка» опухоли для прогнозирования исхода у пациентов с тройно-негативным раком молочной железы. Преобразуя сложные мультипротеиновые изображения в интерпретируемые пространственные шаблоны и простые меры расстояния, SparTile предлагает способ выявлять пациентов с высоким риском по небольшим образцам ткани и обнаруживать биологические компоновки, которые потенциально можно будет нацелить будущими препаратами. Хотя перед применением в рутинной клинической практике требуется дополнительная валидация, подход указывает на будущее, в котором «карта» опухоли станет столь же важной, как и её молекулярный перечень.
Цитирование: Foroughi pour, A., Wu, TC., Noorbakhsh, J. et al. Prediction of outcome from spatial Protein profiling of triple-negative breast cancers. Commun Med 6, 133 (2026). https://doi.org/10.1038/s43856-026-01400-4
Ключевые слова: тройно-негативный рак молочной железы, микроокружение опухоли, пространственная протеомика, имиджинговая масс-цитометрия, прогностические биомаркеры