Clear Sky Science · ru
Недостаточность гомологичной рекомбинации при первичном раке молочной железы с рецепторами эстрогена и без гиперэкспрессии HER2
Почему это важно для пациентов с раком молочной железы
Большинство случаев рака молочной железы относятся к большой группе с позитивностью по рецептору эстрогена и отрицательной экспрессией HER2. Эти опухоли обычно лечат препаратами, блокирующими гормональное действие, иногда в комбинации с химиотерапией. Тем не менее у многих пациентов наблюдаются рецидивы, и врачам не хватает точных инструментов, чтобы решить, кому действительно нужна интенсивная терапия и кто может получить пользу от новых таргетных препаратов. В этом исследовании изучается специфическая уязвимость некоторых опухолей — так называемая недостаточность гомологичной рекомбинации (HRD), из‑за которой клетки опухоли плохо ремонтируют разрывы ДНК, что потенциально открывает путь к более персонализированному лечению.
Скрытая слабость только у части опухолей
Гомологичная рекомбинация — одна из основных систем клетки для исправления опасных разрывов ДНК. Когда эта система не работает — часто из‑за дефектов в известных генах, таких как BRCA1, BRCA2, PALB2 или RAD51C — в клетках накапливаются мутации, и они могут быть особенно чувствительны к определённым препаратам, включая платиновые химиотерапии и ингибиторы PARP. HRD распространена при агрессивной форме рака молочной железы, называемой тройным‑негативным, но её роль в более распространённой группе с позитивными рецепторами эстрогена и отрицательным HER2 оставалась неясной. Чтобы прояснить это, исследователи проанализировали 502 такие опухоли из шведского исследования SCAN‑B методом полного секвенирования генома, а также сопоставили данные об уровне экспрессии генов, метилировании ДНК, полученном лечении и долгосрочных исходах.
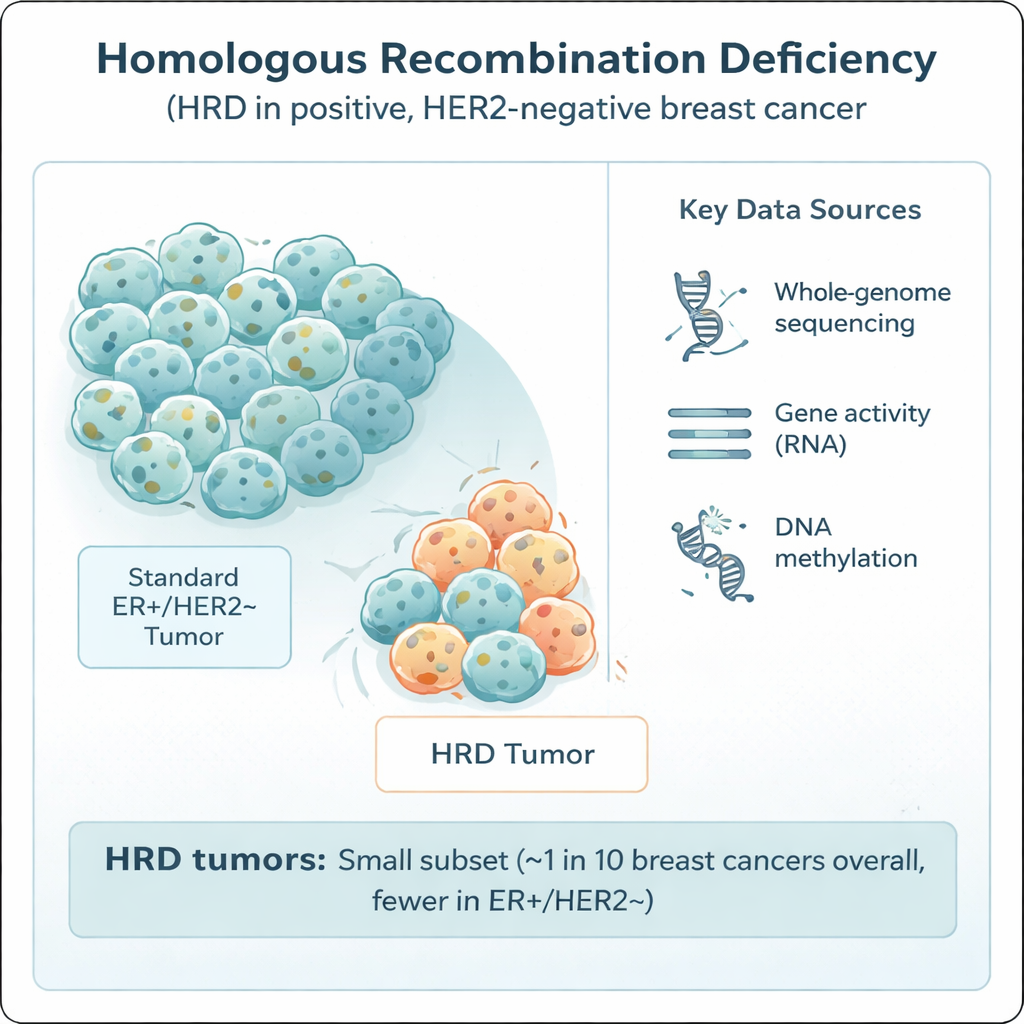
Как проводили исследование
Все опухоли были взяты во время операции до какого‑либо лекарственного лечения, что даёт ясную картину их исходной биологии. Команда использовала сложный инструмент распознавания паттернов HRDetect, чтобы прочесть «мутационные сигнатуры», оставленные в ДНК опухолей при нарушении гомологичной рекомбинации. Опухоли помечали как HRD, если они преодолевали строгий порог вероятности. Учёные также сравнивали разные способы обнаружения HRD — от других ДНК‑базированных показателей до РНК‑теста экспрессии генов — чтобы оценить согласованность методов. Кроме того, они изучали более общие характеристики, такие как общая нагрузка мутаций, паттерны хромосомных приписок и утрат, активность иммунно‑связанных генов и химические метки на ДНК (метилирование), которые могут включать или выключать гены.
Насколько часто встречается HRD и что её вызывает?
Исследователи обнаружили, что лишь 8,4% опухолей с рецептором эстрогена положительным и HER2‑отрицательным в их секвенированной когорте демонстрировали уверенные признаки HRD — значительно меньше, чем примерно 60% при тройном‑негативном заболевании. Объединив эти данные с национальными регистрами и другими исследованиями, они оценили, что около 1 из 20 опухолей в этой клинической подгруппе и примерно 1 из 9 случаев рака молочной железы в целом в западноевропейских/скандинавских популяциях являются HRD. В HRD‑опухолях часто удавалось найти вероятную причину: около 70% имели явные повреждения BRCA1, BRCA2, RAD51C или PALB2 — через наследственные мутации, соматические мутации или делеции, либо эпигенетическое выключение промоутеров генов. Существенно, примерно треть случаев HRD была связана с гиперметилированием промотора — добавочной химической «покрывающей» меткой, которая выключает гены репарации ДНК без изменения последовательности. Однако у приблизительно 30% HRD‑опухолей не выявляли очевидного единственного повреждения, что указывает на дополнительные, ещё не обнаруженные пути к этой нарушенной системе репарации.
Как HRD‑опухоли выглядят под микроскопом и в клинике
HRD‑опухоли в этой распространённой группе рака молочной железы, как правило, имели признаки более агрессивного заболевания: у них чаще наблюдались более высокие показатели деления клеток, более низкая степень окрашивания по гормональным рецепторам и более сложные, насыщенные мутациями геномы по сравнению с опухолями с сохранной гомологичной рекомбинацией. Они встречались почти во всех основных молекулярных подтипах, но были редки в более инертном классе Luminal A и относительнo обогащены в небольшой подгруппе с базальноподобными чертами. Тем не менее при анализе общей экспрессии генов и паттернов метилирования HRD‑опухоли не формировали единого легко узнаваемого профиля. Их профиль экспрессии был разнообразен, а различия внутри конкретных подтипов были умеренными. Некоторые HRD‑опухоли, особенно в группах Luminal B и базальноподобных, демонстрировали более выраженные признаки иммунной активности и повышенную экспрессию PD‑L1, что намекает на их большую «видимость» для иммунной системы и потенциальную чувствительность к иммунотерапии.
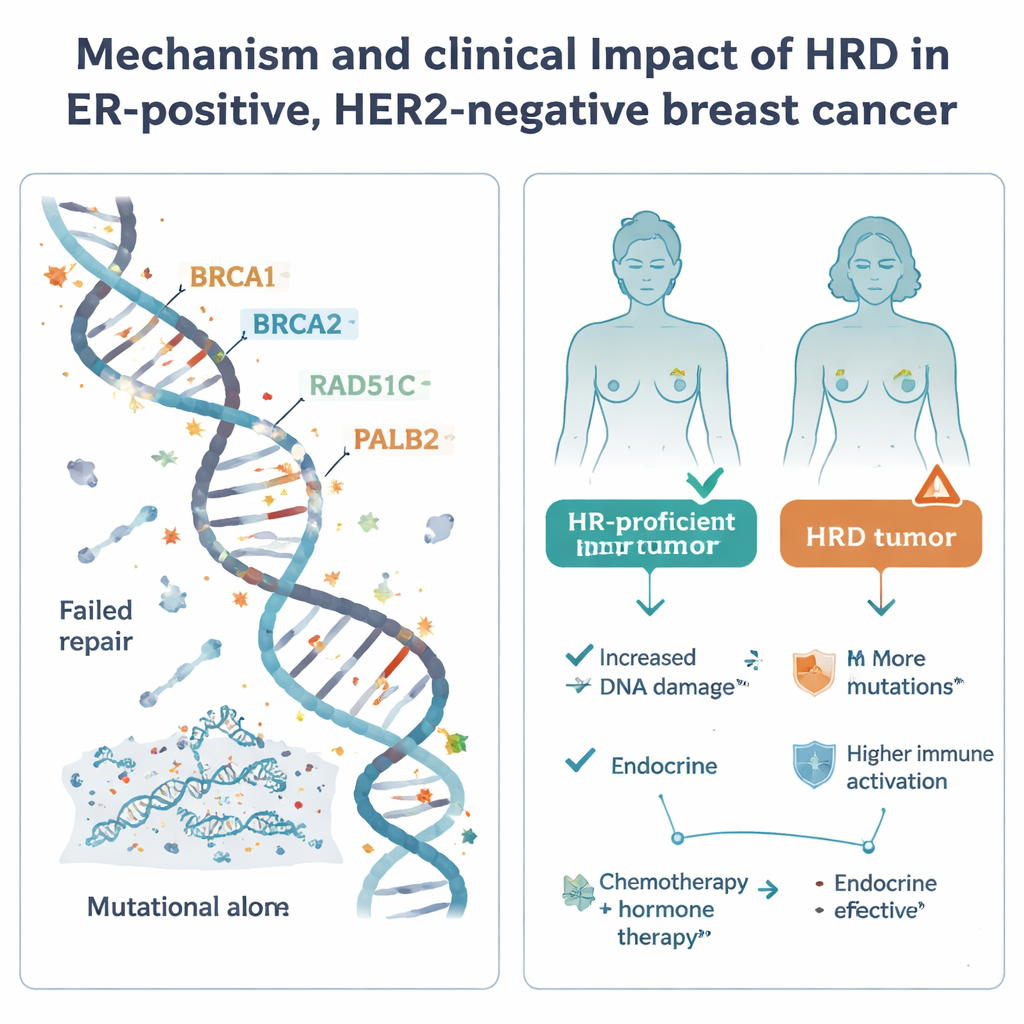
Влияет ли HRD на исходы у пациентов?
Далее авторы исследования сопоставили статус HRD с реальными клиническими исходами при стандартной терапии. У пациентов, получавших только гормональную терапию после операции, HRD‑опухоли демонстрировали тенденцию к худшей выживаемости без отдалённых рецидивов, хотя число случаев HRD было невелико и результат не достиг формальной статистической значимости. Этот паттерн, в сочетании с их агрессивными молекулярными чертами, указывает на то, что полагаться исключительно на эндокринную терапию может быть рискованно для пациентов с HRD‑опухолями. Напротив, среди пациентов, получавших и химиотерапию, и гормональную терапию, статус HRD явно не коррелировал с лучшими или худшими исходами: у всех групп наблюдались в целом сопоставимые показатели рецидивов, и возможно, что химиотерапия частично нивелирует повышенный риск, связанный с HRD.
Что это значит для будущего выбора лечения
Для широкого круга читателей ключевое сообщение таково: лишь меньшинство раков молочной железы с позитивным рецептором эстрогена и отрицательным HER2 несёт эту специфическую проблему с ремонтом ДНК, но при её наличии опухоль, как правило, более агрессивна и может плохо контролироваться только гормональной терапией. Работа подтверждает, что полногеномное секвенирование может надёжно выявлять HRD и прояснять её причины, выходя за рамки только тестирования на наследственные мутации BRCA1 или BRCA2. Хотя исследование ещё не доказывает, что изменение лечения на основании статуса HRD улучшает выживаемость, оно даёт ранние свидетельства того, что пациенты с HRD‑опухолями могут извлечь выгоду от химиотерапии и, в будущих клинических испытаниях, от ингибиторов PARP или иммунотерапии. Проще говоря, тестирование на HRD может стать одним из элементов более тонко настроенного набора инструментов для подбора интенсивности терапии и новых таргетных опций в соответствии с биологией конкретного рака молочной железы пациента.
Цитирование: Davies, H.R., Black, D., Kvist, A. et al. Homologous recombination deficiency in primary ER-positive and HER2-negative breast cancer. Commun Med 6, 118 (2026). https://doi.org/10.1038/s43856-026-01385-0
Ключевые слова: рак молочной железы, репарация ДНК, гены BRCA, секвенирование генома, таргетная терапия