Clear Sky Science · ru
Поверхностно модифицированные липосомальные наночастицы, нагруженные двумя препаратами и нацеленные на опухоль, для преодоления терапевтической резистентности при множественной глиобластоме
Почему это исследование рака мозга важно
Глиобластома — одна из самых смертельных форм рака мозга. Даже при хирургии, радиотерапии и химиотерапии большинство пациентов живут немного больше года после постановки диагноза. Одной из основных проблем является то, что стандартные лекарства часто не могут достигнуть опухоли в мозге, а если и достигают, опухоль быстро адаптируется и становится резистентной. В этом исследовании изучается новый подход, позволяющий провести сразу несколько препаратов через природные барьеры мозга и сконцентрировать их внутри опухоли с целью значительно повысить эффективность существующих методов лечения, таких как радиотерапия.
Крошечный грузовичок для противораковых препаратов
Исследователи создали ультра-мелкие переносчики лекарств — липосомы, нацеленные на опухоль. Это мягкие жировые пузырьки на шкале миллиардных долей метра, которые могут вмещать лекарственные вещества внутри себя. Команда модифицировала поверхность этих пузырьков специальным пептидом, который распознаёт и прикрепляется к клеткам глиобластомы, помогая частицам направляться к опухоли, а не к здоровой ткани. Каждая «пузырьковая» частица была спроектирована для одновременной доставки пары противораковых препаратов: либо эверолимуса в сочетании с винорелбином, либо рапамицина с винорелбином. Идея в том, что два препарата атакуют опухолевые клетки взаимодополняющими способами, а защитная оболочка помогает лекарствам выживать в кровотоке и проникать в мозг.
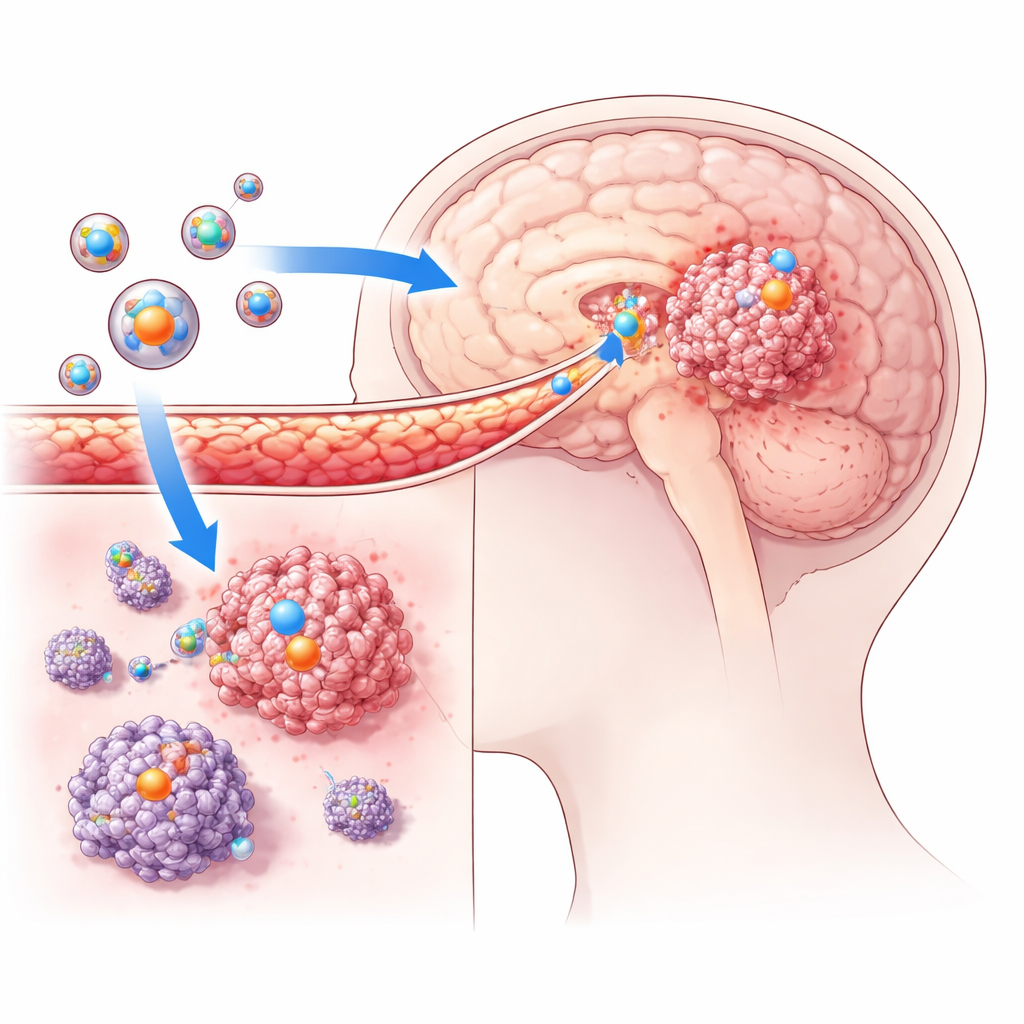
Пересечение защитной стены мозга
Используя мышиные модели с имплантированными человеческими клетками глиобластомы, команда проверила, действительно ли эти липосомы могут достигать опухолей внутри мозга. Частицы мечтали флуоресцентными красителями и отслеживали их движение с помощью продвинутых методов визуализации. По сравнению с нетаргетированными липосомами таргетированные версии показали заметно более сильные сигналы внутри опухолей мозга и слабый сигнал в нормальных участках мозга. Это подтвердило, что сконструированные частицы способны пересекать гематоэнцефалический барьер и накапливаться именно там, где растут раковые клетки. В экспериментах в клеточных культурах клетки глиобластомы также поглощали значительно больше таргетированных липосом, чем контрольные, что подкрепляет идею о том, что поверхностный пептид существенно улучшает нацеливание и проникновение в опухоль.
Наносим более сильный удар по опухоли, щадя остальной организм
Сначала учёные сравнили, насколько хорошо одно- и двухпрепаратные липосомы убивают раковые клетки в культурах. Двухпрепаратные варианты, особенно сочетание эверолимус–винорелбин, оказались более эффективными, чем каждый препарат по отдельности, и превзошли те же препараты, введённые без липосомного носителя. В комбинации с радиотерапией эффект был ещё сильнее: клетки формировали значительно меньше колоний, перемещались реже и демонстрировали признаки усиленного повреждения. В мышиных опухолях мозга животные, получавшие двухпрепаратные липосомы вместе с облучением, демонстрировали более медленный рост опухоли и проживали дольше по сравнению с теми, кто получал только облучение, только липосомы или стандартную химиотерапию темозоломидом. Важно, что исследователи не наблюдали явных повреждений в других органах, что предполагает: фокусирование лечения на опухоли может снизить побочные эффекты.
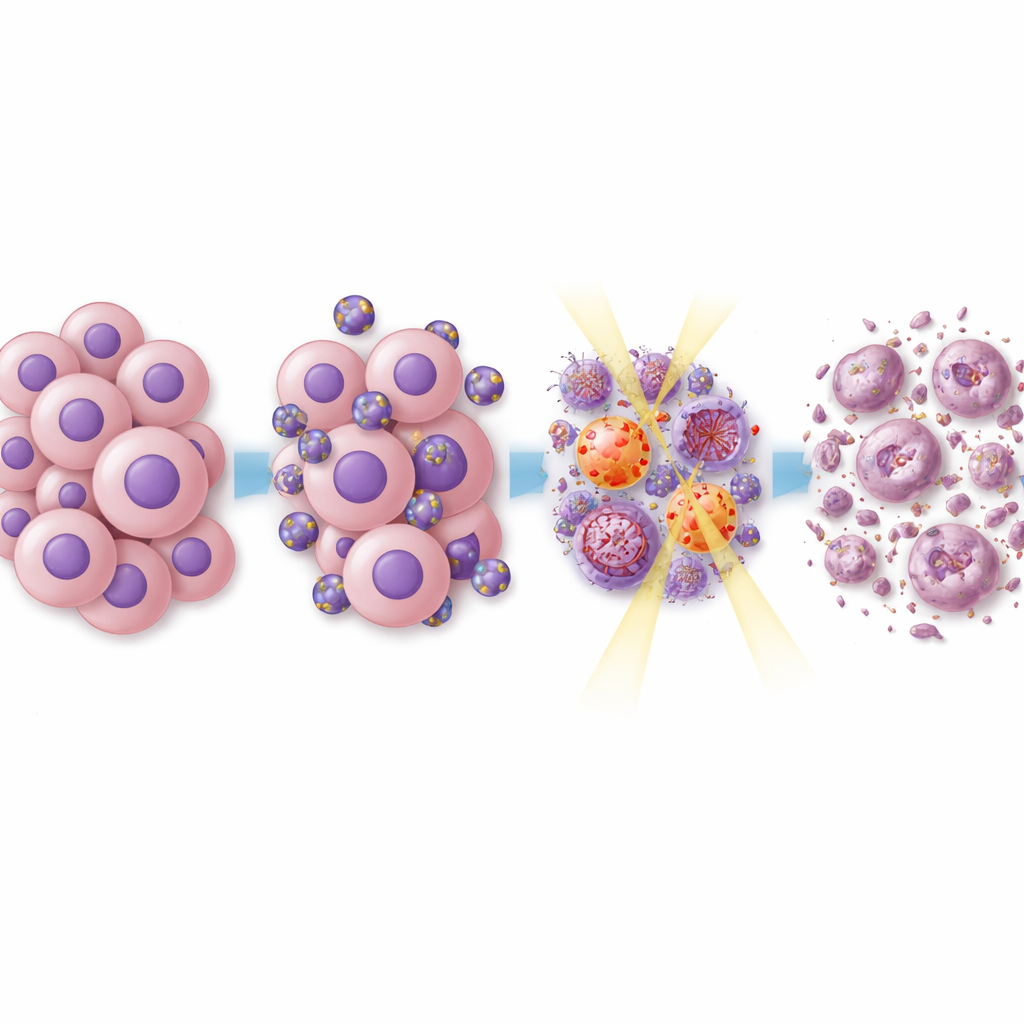
Что происходит внутри раковых клеток
Чтобы понять, почему этот подход повысил чувствительность опухолей к лечению, команда изучила ключевые сигнальные системы внутри раковых клеток. Известно, что эверолимус и рапамицин блокируют путь, называемый mTOR, который помогает клеткам расти и сопротивляться стрессу. Двухпрепаратные липосомы подавляли сигналы, связанные с mTOR, а также другие ростовые пути, стимулирующие деление и движение клеток глиобластомы. При добавлении радиотерапии белки, вовлечённые в репарацию ДНК, также ослабевали. Это означает, что опухолевые клетки были менее способны исправлять генетические повреждения, вызванные облучением, что толкало их к гибели вместо восстановления. Детальный анализ активности генов в обработанных опухолях показал широкие изменения в сетях, связанных с контролем клеточного цикла, репарацией ДНК и взаимодействием опухоли с иммунной системой, и многие гены, ассоциированные с резистентностью к лечению, оказались понижены в экспрессии.
Что это может значить для будущих пациентов
Эта работа демонстрирует, что тщательно спроектированные, нацеливаемые на опухоль наночастицы способны доставлять два сочетающихся препарата через защитный барьер мозга, концентрировать их в глиобластоме и повышать эффективность радиотерапии. На моделях мышей такая стратегия замедляла рост опухоли и продлевала выживание без очевидного увеличения токсичности. Хотя результаты всё ещё остаются доклиническими и до применения у людей требуется множество дополнительных испытаний, исследование указывает на практический путь объединения целевой доставки препаратов с существующими методами лечения для обхода высоко резистентного рака. Если подобные преимущества подтвердятся у людей, такие липосомы с двойной загрузкой могут однажды обеспечить пациентам с глиобластомой более долгую и более качественную жизнь.
Цитирование: Angom, R.S., Rachamala, H.K., Nakka, N.M.R. et al. Surface-engineered dual drug-loaded tumor-targeted liposomal nanoparticles to overcome the therapeutic resistance in glioblastoma multiforme. Commun Med 6, 152 (2026). https://doi.org/10.1038/s43856-025-01279-7
Ключевые слова: глиобластома, наночастицы, липосомы, лечение рака мозга, сенсибилизация к радиотерапии