Clear Sky Science · ru
Резистентность к химиотерапии на основе платины при раке легких и яичников обусловлена нацеливаемым секретом стареющих клеток, активируемым TGFβ
Когда лечение рака срабатывает во вред
Химиотерапия на основе платины — один из столпов современной онкологии, особенно при раке легких и яичников. Эти препараты призваны настолько повреждать ДНК опухоли, чтобы клетки лишались способности делиться. Тем не менее у многих пациентов опухоль сначала сокращается, а затем возвращается, став более агрессивной. В этом исследовании поставлен простой, но тревожный вопрос: не помогают ли те же препараты уцелевшим клеткам восстановиться? Ответ, находят авторы, кроется в особой группе повреждённых, по сути «стареющих» клеток и мощных химических сигналах, которые они посылают.
Двойная роль стареющих клеток опухоли
Химиотерапия действует на клетки опухоли не одинаково. Часть уничтожается, а часть входит в состояние, называемое клеточным старением — они навсегда утрачивают способность делиться, но остаются живыми. Эти сенесцентные клетки увеличиваются в размерах и начинают выбрасывать коктейль белков и сигналов, известный как сенесценс-ассоциированный секреторный фенотип (SASP). На моделях человеческих клеток рака легкого и яичников в культуре и в мышиных моделях исследователи показали, что платиновые препараты, такие как цисплатин и карбоплатин, индуцируют особенно мощные сенесцентные клетки. Когда свежие раковые клетки культивировали в среде, полученной от таких сенесцентных культур, они росли быстрее, активнее мигрировали и формировали большие, более агрессивные скопления и сферы по сравнению с контролем.
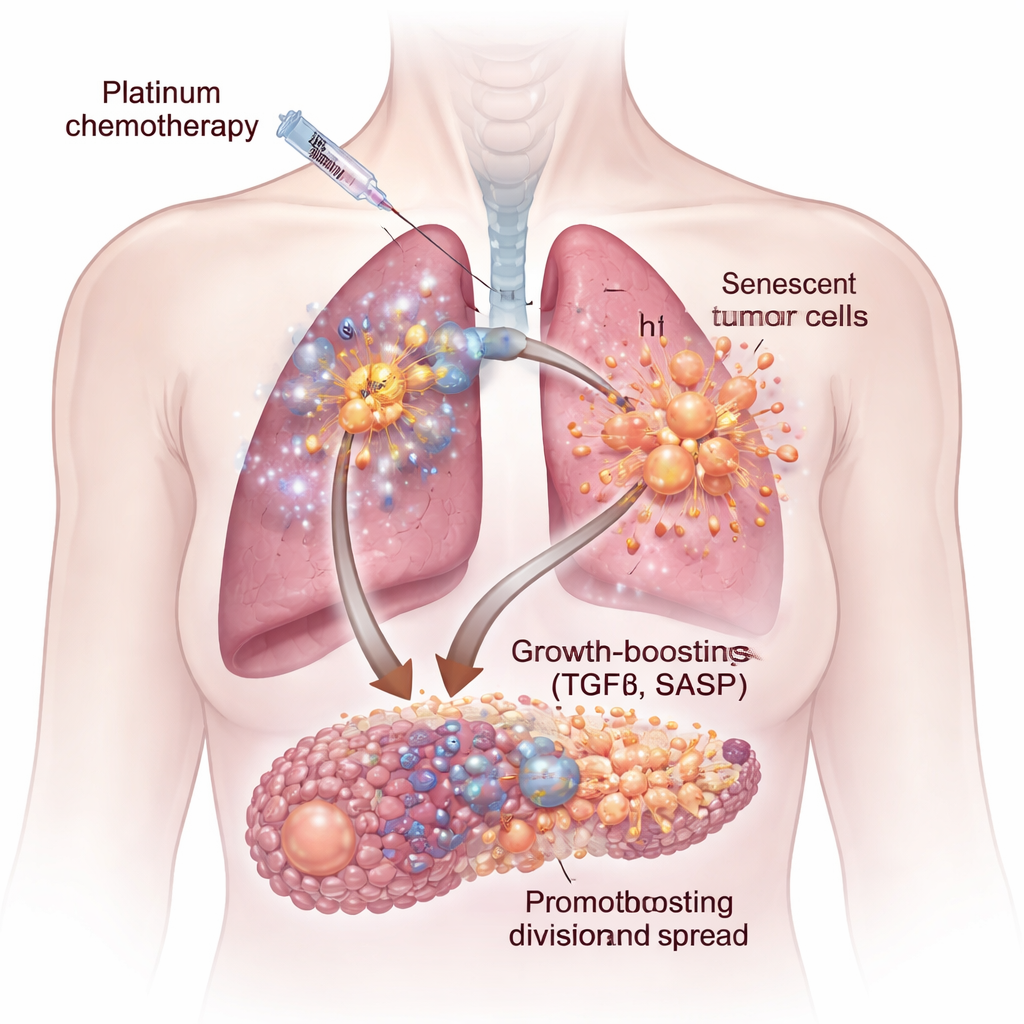
Скрытый сигнál роста: TGFβ
Не все типы химиотерапии вызывали одинаково вредные секреты. Сравнивая платиновые препараты с двумя другими распространёнными агентами — доксетакселом и палбоциклибом — команда обнаружила, что лишь клетки, обработанные платиной, продуцировали SASP, который значительно усиливал рост опухоли. Комбинируя исследования экспрессии генов, измерения белков и высокопроизводительный микросредовой микромассив, они выделили ключевую причину: сигнальная молекула трансформирующий фактор роста-бета (TGFβ). Сенесцентные клетки, вызванные цисплатином, были обогащены несколькими формами TGFβ и связанными путями. Добавление очищенного TGFβ к раковым клеткам имитировало стимуляцию роста, наблюдаемую при воздействии среды от сенесцентных клеток, что подчёркивает эту семью цитокинов как центральный драйвер провоопухолевого секретома.
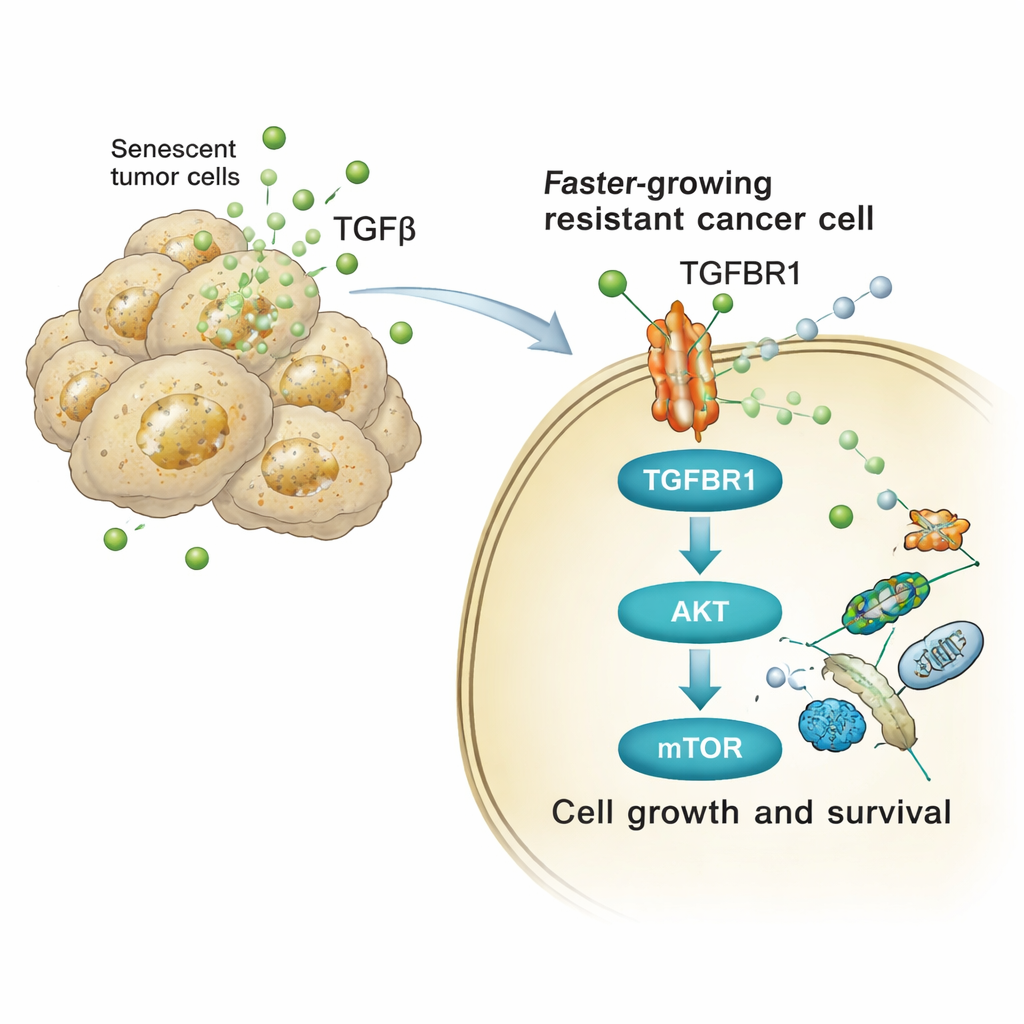
Как сигнал перестраивает раковые клетки
Далее исследование проследило, как сигналы, богатые TGFβ, меняют поведение соседних опухолевых клеток. На поверхности реципиентных клеток TGFβ связывается с рецептором TGFBR1. Это, в свою очередь, запускает внутреннюю цепочку белков — особенно пути AKT и mTOR — известные как регуляторы роста, метаболизма и выживания клеток. В клетках рака легкого человека и мыши воздействие выделений, индуцированных цисплатином, быстро увеличивало активированные (фосфорилированные) формы AKT и его внизпо течному мишени p70S6K, а также усиливало экспрессию генов клеточного цикла. Блокирование TGFBR1 препаратом галунеристибом или прямое ингибирование mTOR в значительной степени подавляло этот всплеск сигнальной активности и уменьшало дополнительную пролиферацию, формирование колоний и инвазивный рост сфер, вызванные сенесцентным секретом.
От мышей к пациентам: общая уязвимость
Эти механизмы не ограничивались чашками Петри. У мышей с опухолями легкого смешивание сенесцентных и не сенесцентных раковых клеток приводило к более быстрому росту опухолей и сокращению выживаемости, тогда как устранение сенесцентных клеток или блокирование TGFBR1 ослабляло этот эффект. При стандартном лечении цисплатином у мышей с генетически индуцированными раками легкого в опухолях накапливались маркёры сенесценции наряду с высокой активностью AKT/mTOR в соседних ещё делящихся клетках. Сочетание цисплатина с ингибитором TGFBR1 или сенолитиками (препаратами, избирательно убивающими сенесцентные клетки) снижало опухолевую нагрузку и увеличивало выживаемость по сравнению с одной только химиотерапией. Важное наблюдение: анализы образцов у людей с раком легкого и высокосерозным раком яичников, взятых после терапии препаратами платины, показали аналогичную картину — возрастание маркёров сенесценции и усиление сигнальной активности AKT/mTOR в микроокружении опухоли, особенно в областях, богатых сенесцентными клетками.
Как превратить слабое место в преимущество
Главный вывод для непрофессионала таков: платиновая химиотерапия может оставлять после себя популяцию повреждённых, но опасных «зомби»-клеток. Эти сенесцентные опухолевые клетки сами уже не делятся, но выделяют TGFβ-обогащённые сигналы, которые пробуждают соседние раковые клетки, помогая опухолям заново разрастаться и сопротивляться дальнейшему лечению. Ободряющая новость — эту уязвимость можно нацелить. В доклинических моделях рака легкого и яичников добавление препаратов, блокирующих рецептор TGFBR1, или применение сенолитиков, избирательно очищающих сенесцентные клетки, сделало платиновую химиотерапию более эффективной и улучшило выживаемость без очевидного увеличения токсичности. Работа нацеливает будущее клинических испытаний, которые комбинируют стандартную платиновую терапию с сенолитическими или анти-TGFβ стратегиями, чтобы сохранить преимущества химиотерапии и обезвредить её скрытые, управляемые сенесценцией побочные эффекты.
Цитирование: González-Gualda, E., Reinius, M.A.V., Macias, D. et al. Treatment resistance to platinum-based chemotherapy in lung and ovarian cancer is driven by a targetable TGFβ senescent secretome. Nat Aging 6, 368–392 (2026). https://doi.org/10.1038/s43587-025-01054-2
Ключевые слова: резистентность к химиотерапии, клеточное старение, сигнализация TGFβ, рак легкого, рак яичников