Clear Sky Science · ru
Повреждение ДНК в макрофагах вызывает аутоиммунную реактивность через презентацию ядерных антигенов
Когда клеточный износ заставляет иммунную систему действовать против нас
С возрастом риск аутоиммунных заболеваний повышается: иммунная система начинает атаковать собственный организм. В этом исследовании рассматривается неожиданный виновник — повседневные повреждения ДНК в иммунных клетках, называемых макрофагами. Проследив, как эти повреждения меняют то, что макрофаги показывают другим иммунным клеткам, исследователи выявили возможную недостающую связь между старением и развитием таких заболеваний, как волчанка.
Стражи организма, вышедшие из-под контроля
Макрофаги — передовые защитники, поглощающие микроорганизмы и мусор, а затем представляющие фрагменты белков Т-клеткам, помогая иммунной системе решить, что атаковать. Авторы создали мышей с дефектными макрофагами по ключевому белку репарации ДНК ERCC1-XPF, из‑за чего эти клетки накапливали постоянные повреждения ДНК. По мере старения у этих мышей появились признаки аутоиммунитета: воспалительные очаги в почках, отложения иммунных комплексов и белков комплемента, увеличенные селезенки и высокие уровни антиядерных антител, похожие на те, что наблюдаются у естественно старых животных. Детальный иммунный профиль показал расширение плазматических клеток, активацию Т-клеток и естественных киллеров — все признаки хронически стимулированной иммунной системы.
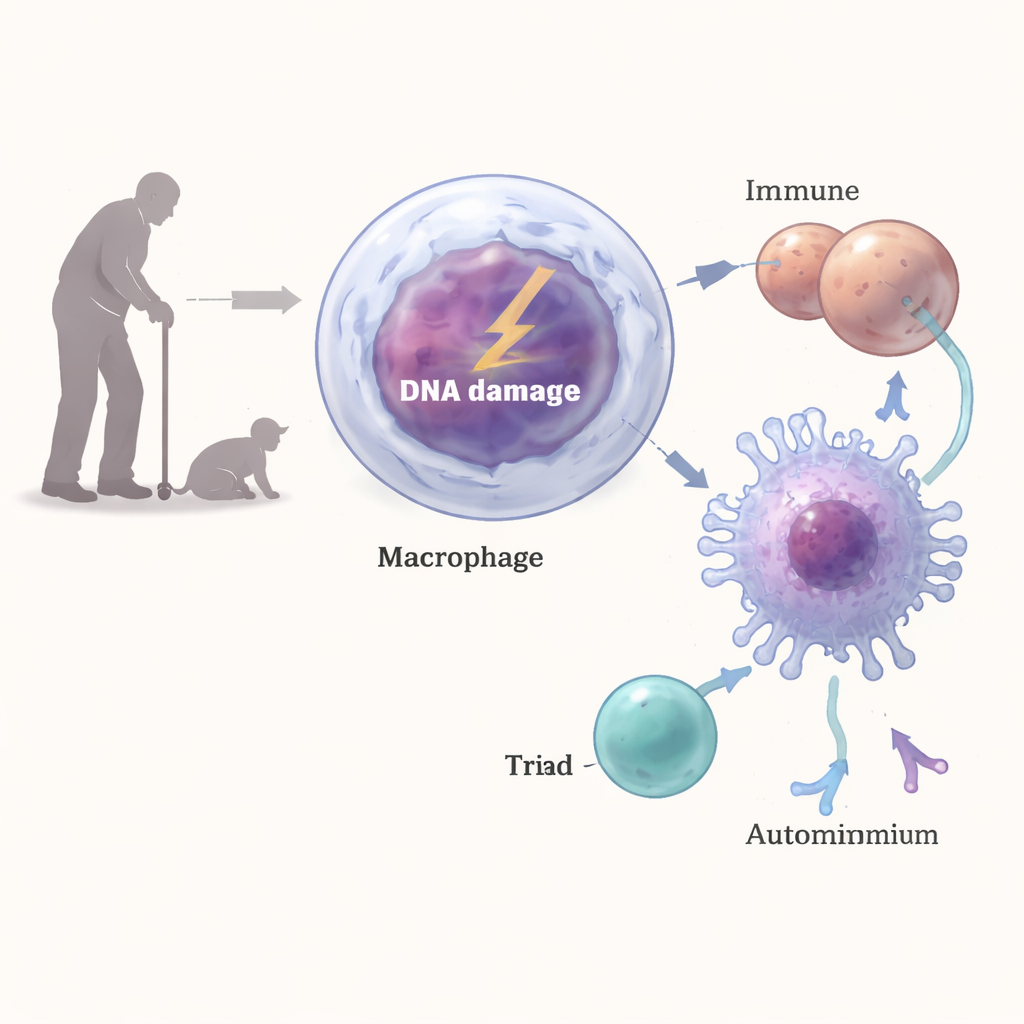
От повреждённой ДНК к Т-клеткам, нацеленным на собственные белки
Как повреждение ДНК в макрофагах могло вызвать столь выраженный аутоиммуноподобный ответ? Исследователи обнаружили, что разрывы ДНК активируют классический путь ответа на повреждение в этих клетках с участием ферментов ATM, ATR и DNA‑PK. Этот сигнальный каскад повышал уровень MHC класса II на поверхности — молекулярных «витрин», используемых для презентации фрагментов белков CD4‑Т‑клеткам. Когда макрофаги с повреждённой ДНК смешивали с Т‑клетками, они вызывали более сильную активацию Т‑клеток и продукцию интерферона‑гамма, чем нормальные макрофаги. Блокирование MHC‑II или вмешательство в путь ответа на повреждение ДНК обратило значительную часть этого эффекта, а in vivo антитела, блокирующие MHC‑II, или истощение CD4‑Т‑клеток снижали воспаление почек и уровень аутоантител.
Ядерные собственные белки выставляются на показ
Чтобы точно понять, что повреждённые макрофаги показывают Т‑клеткам, команда выделила пептиды, связанные с MHC‑II, и проанализировала их методом масс‑спектрометрии. По сравнению с нормальными или стимулированными липополисахаридом клетками, макрофаги с повреждённой ДНК демонстрировали поразительно иной набор пептидов. Вместо преобладания трансмембранных и внеклеточных белков их молекулы MHC‑II были обогащены фрагментами, происходящими из ядерных и рибосомных белков, включая гистоны и другие компоненты, тесно связанные с ДНК. Когда некоторые из этих ядерных пептидов синтезировали и использовали для повторной стимуляции иммунных клеток от генетически модифицированных мышей, они вызывали сильные Т‑клеточные ответы, что указывает на иммуногенность этих собственных фрагментов.
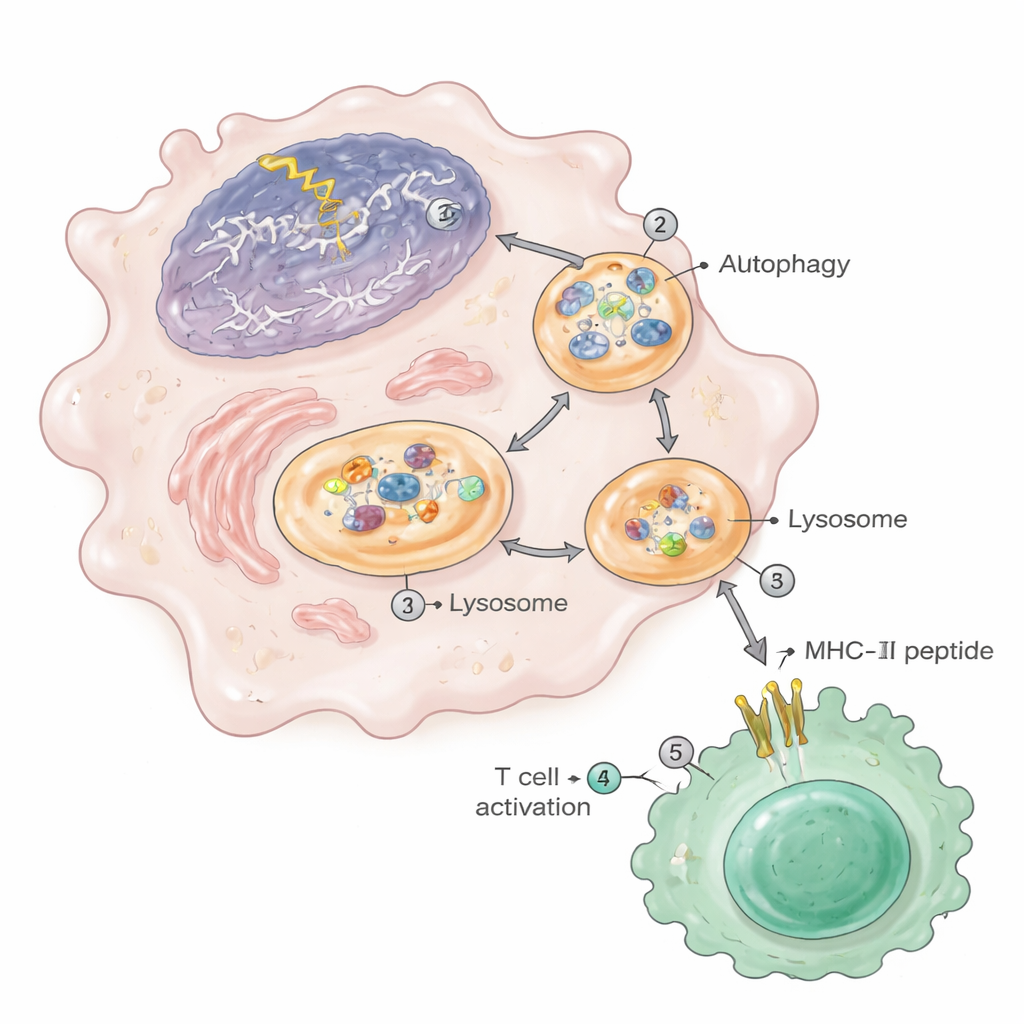
Аутофагия: путь утилизации, подпитывающий аутоиммунитет
Путь переноса ядерного материала в «витрину» MHC‑II в значительной степени зависел от аутофагии, внутриклеточной системы утилизации. При повреждении ДНК аутофагия усиливалась и направляла фрагменты хроматина — из собственной ядровой ДНК — в аутофагосомы, которые затем сливались с лизосомами, где белки расщепляются до пептидов. В этих лизосомах повреждённых макрофагов обнаруживались повышенные уровни ядерных и рибосомных белков. Когда исследователи блокировали аутофагию препаратами или генетически удаляли жизненно важный ген аутофагии Atg5 в миелоидных клетках, у животных уменьшалось количество поражений почек, число активированных Т‑клеток и плазматических клеток, а также резко снижалось появление ядерных пептидов на MHC‑II. Похожие фрагменты хроматина и повышенная презентация антигенов наблюдались в макрофагах мышей, склонных к волчанке, в линиях человеческих моноцитов, обработанных препаратами, повреждающими ДНК, и в макрофагах очень старых мышей.
Почему это важно для старения и аутоиммунных заболеваний
В совокупности результаты указывают на простую, но мощную идею: с возрастом в макрофагах накапливается повреждение ДНК, и эти клетки с помощью аутофагии утилизируют ядерный мусор. При этом они непреднамеренно расщепляют ядерный материал на пептиды, загружаемые в MHC‑II и демонстрируемые Т‑клеткам как чужие. Со временем хроническое предъявление ядерных собственных антигенов может «обучить» иммунную систему реагировать на собственный организм, способствуя аутоиммунитету. Указав этот путь — от повреждения ДНК через аутофагию к презентации ядерных антигенов — исследование выделяет новые стратегии для ослабления возрастного аутоиммунитета: усиление репарации ДНК, тонкая настройка аутофагии или селективное блокирование презентации ядерных собственных пептидов без отключения жизненно важных защит иммунной системы.
Цитирование: Niotis, G., Arvanitaki, E.S., Theodorakis, E. et al. DNA damage in macrophages drives immune autoreactivity via nuclear antigen presentation. Nat Aging 6, 393–413 (2026). https://doi.org/10.1038/s43587-025-01053-3
Ключевые слова: старение и аутоиммунитет, повреждение ДНК, макрофаги, аутофагия, антиядерные антитела