Clear Sky Science · ru
Сенотоксины нацеливаются на сенесценцию через специфичное связывание липидов, ионный дисбаланс и ремоделирование липидома
Почему уничтожение «зомби»-клеток может улучшить лечение рака
С возрастом или после тяжёлых вмешательств, таких как химиотерапия, некоторые клетки прекращают делиться, но отказываются умирать. Эти «зомби»-клетки, известные как сенесцентные, выделяют воспалительные молекулы, повреждающие ткани и способствующие рецидиву опухолей. В этом исследовании описан неожиданный способ выборочного удаления таких проблемных клеток с помощью белка, полученного из яда, что потенциально может сделать лечение рака более эффективным и безопасным.
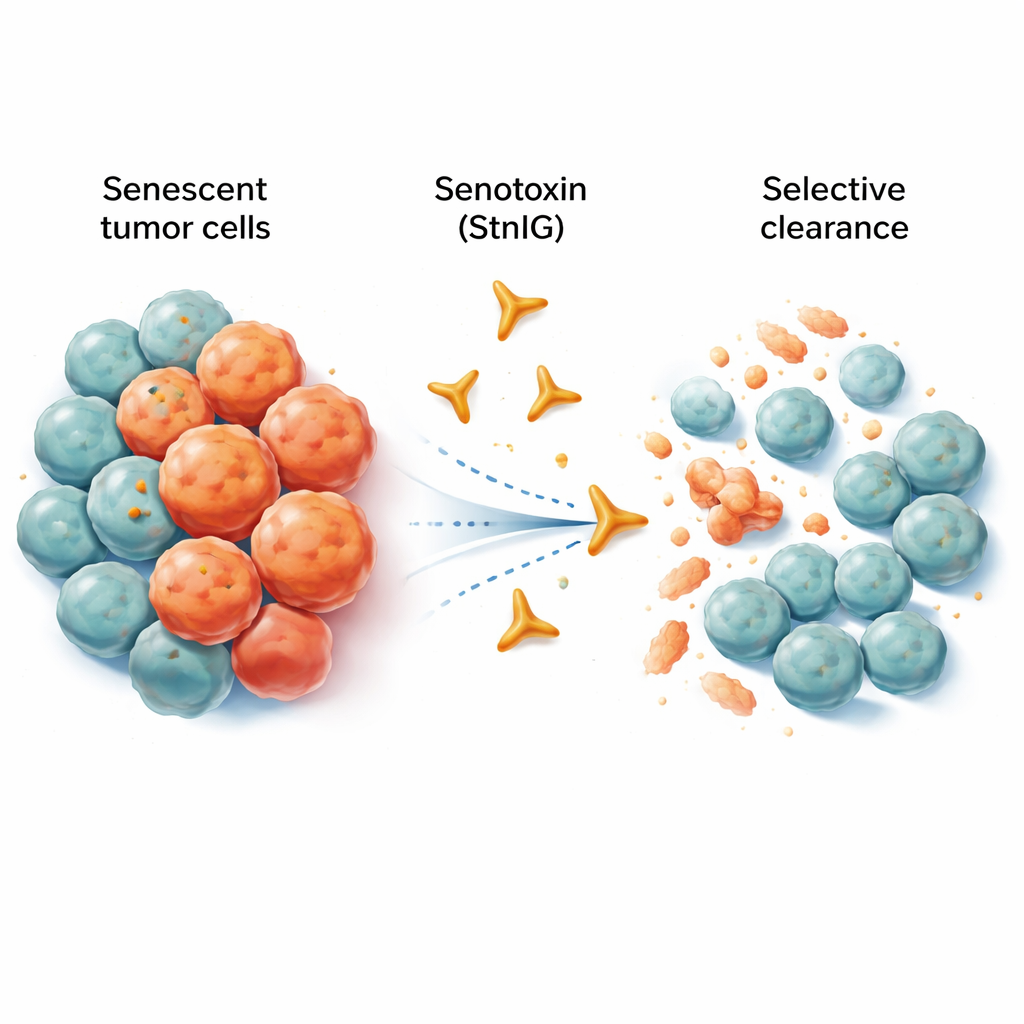
Старые клетки, которые не сдаются
Сенесцентные клетки похожи на вышедших на пенсию сотрудников, которые по-прежнему занимают рабочие места и мешают функционированию офиса. Они больше не делятся, но выделяют коктейль воспалительных сигналов, ослабляющих соседние ткани, способствующих старению и даже поддерживающих рост и метастазирование опухолей. Химиотерапия убивает многие раковые клетки, но часто оставляет после себя скопления сенесцентных клеток в и вокруг опухоли. Эти остаточные клетки подпитывают хроническое воспаление, побочные эффекты и в конечном счёте рецидив. Существующие экспериментальные препараты — сенолитики — нацелены на удаление сенесцентных клеток, но многие из них либо повреждают здоровые клетки, либо действуют в очень узком диапазоне доз, либо плохо усваиваются организмом.
Преобразование яда морской анемоны в точный инструмент
Исследователи обратились к природным специалистам по убийству клеток: животным ядам. Они сосредоточились на порообразующем белке стихолосине I (StnI), обнаруженном в карибской морской анемоне. Этот белок может проделывать крошечные отверстия в клеточных мембранах. Команда выяснила, что StnI и усовершенствованный вариант, который они сконструировали и назвали StnIG, значительно лучше уничтожают сенесцентные раковые клетки по сравнению с их нестареющими соседями. В нескольких типах человеческих раковых клеток (меланома, печень, лёгкие и опухоли нервного происхождения), индуцированных в состояние сенесценции химиопрепаратами, StnI и особенно StnIG уничтожали «постаревшие» клетки при гораздо более низких дозах, чем требовалось для поражения активно растущих клеток. StnIG оказался более селективным, чем ведущий экспериментальный сенолитик нави-токлакс (navitoclax), что говорит о том, что тщательно настроенные токсины могут превзойти существующие подходы.
Как изменённые клеточные мембраны становятся ахиллесовой пятой
Сенесцентные клетки меняются не только внутри; их наружная мембрана — жирная оболочка, окружающая клетку — тоже перестраивается. В здоровых клетках некоторые липиды преимущественно расположены со внутренней стороны мембраны и скрыты от внешней среды. У сенесцентных клеток этот баланс нарушается, и эти липиды оказываются на внешней поверхности. С помощью детального химического анализа и компьютерного моделирования команда показала, что StnIG распознаёт и прочно связывается с этим изменённым липидным ландшафтом. Его структура особенно благоприятствует захвату специфических липидов, выставленных на поверхности сенесцентных клеток. После прикрепления StnIG формирует поры, через которые заряженные атомы — ионы — начинают очень неравномерно перетекать внутрь и наружу.
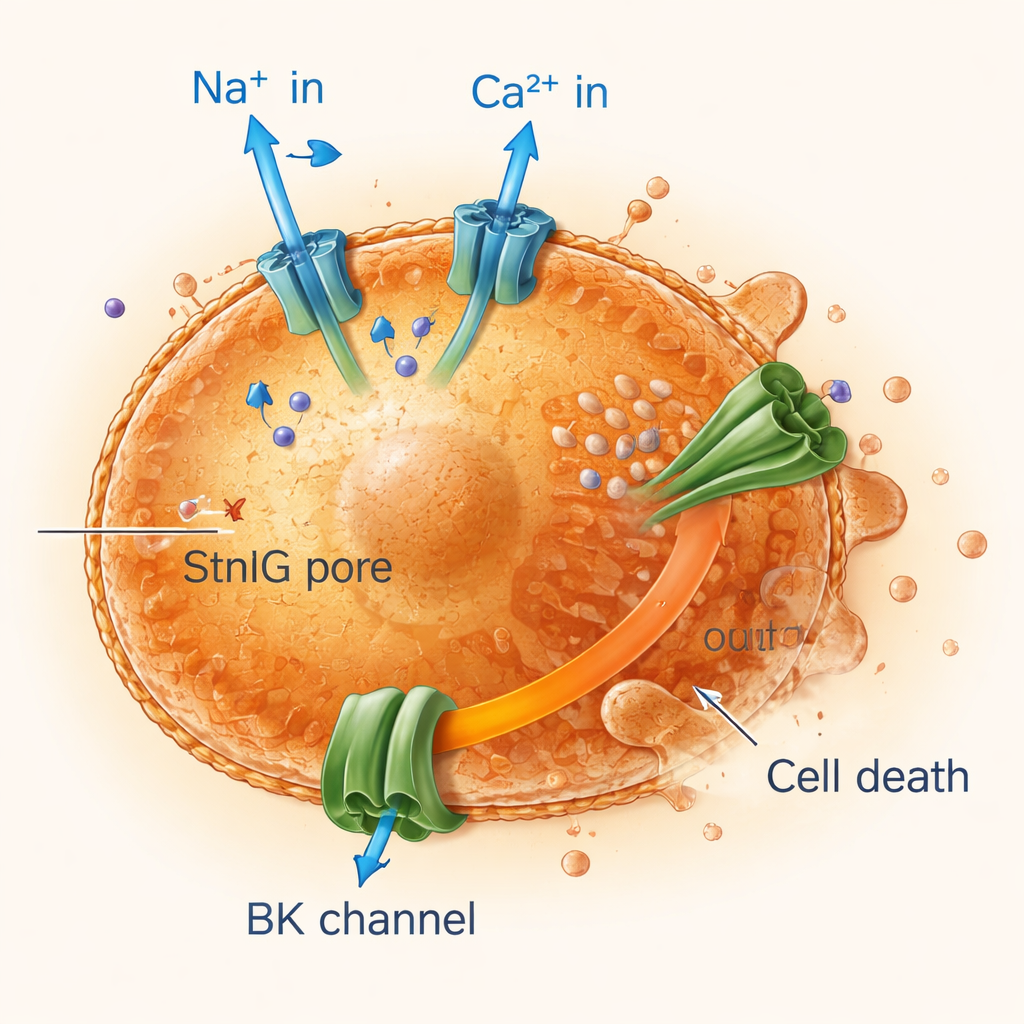
Короткое замыкание стареющих клеток ионным дисбалансом
Отслеживая ток и движение ионов через мембраны, исследователи установили, что поры StnIG пропускают натрий и кальций внутрь сенесцентных клеток, в то время как калий непрерывно утекает наружу. Всплеск кальция активирует большие калиевые каналы, усиливая потерю калия, который критичен для поддержания объёма клетки и её выживания. Сенесцентные клетки, уже менее гибкие и более хрупкие, чем здоровые, не справляются с этим длительным ионным нарушением. Их митохондрии — энергетические станции клетки — теряют электропотенциал, выработка энергии падает, и клетки проходят программируемые формы гибели, включая апоптоз и воспалительную форму гибели, пироптоз. Блокирование входа кальция или калиевых каналов защищало сенесцентные клетки, подтверждая, что именно ионный дисбаланс лежит в основе действия токсина.
От клеточных культур к живым организмам
Дальше команда проверила, работает ли этот подход в живых существах. В эмбрионах рыбок-зебра, несущих человеческие сенесцентные клетки меланомы, низкие дозы StnIG уменьшали число этих клеток так же эффективно, как и navitoclax, без явной токсичности. В мышиных моделях меланомы и рака печени химиотерапия препаратом, блокирующим клеточный цикл (пальбоциклиб), замедляла рост опухолей, переводя многие раковые клетки в состояние сенесценции. При периодическом добавлении StnIG опухоли сокращались или входили в ремиссию эффективнее, чем при одной только химиотерапии, и сопоставимо с комбинацией химиотерапии и navitoclax. Важно, что у мышей, получавших StnIG, наблюдались ограниченные побочные эффекты и явных повреждений основных органов не выявлено, хотя у животных с сенесцентными опухолями уровень калия в крови повышался — вероятно, из‑за массового выхода калия при разрушении клеток опухоли.
Что это означает для будущего лечения рака
Эта работа вводит понятие «сенотоксины»: инженированные белки, вдохновлённые ядами, которые используют уникальные особенности мембран и ионной регуляции сенесцентных клеток. Наводясь на изменённые липиды и вызывая фатальные ионные дисбалансы, StnIG способен выборочно очищать вредные сенесцентные клетки, оставаясь щадящим для большинства здоровых тканей. В сочетании с химиотерапией такие сенотоксины однажды могут помочь устранить «зомби»-клетки, которые питают рецидив и хроническое воспаление, делая лечение рака более долговременным и потенциально уменьшая некоторые отдалённые побочные эффекты.
Цитирование: Moral-Sanz, J., Fernández-Carrasco, I., Ramponi, V. et al. Senotoxins target senescence via lipid binding specificity, ion imbalance and lipidome remodeling. Nat Aging 6, 349–367 (2026). https://doi.org/10.1038/s43587-025-01030-w
Ключевые слова: клеточное старение, сенолитики, терапия рака, лекарства, полученные из яда, ионные каналы