Clear Sky Science · ru
Прогнозирование и интерпретация клеточно-тип-специфических ответов на лекарства в режиме малого объема данных с использованием индуктивных априорных знаний
Почему это исследование важно для будущих лекарств
Когда новый препарат испытывают, одна из главных неизвестных — насколько по‑разному он повлияет на множество типов клеток в организме. Соединение, полезное для одного типа клеток, может мало влиять на другой или даже причинять вред. Получать эти данные экспериментально для тысяч препаратов и бесчисленных типов клеток слишком долго и дорого. В этой статье предлагается компьютерный подход PrePR-CT, который учится предсказывать реакцию отдельных типов клеток на препараты даже при ограниченных данных. Работа указывает путь к более быстрым, дешевым и точным способам изучения потенциальных лекарств in silico перед дорогостоящими лабораторными и клиническими исследованиями.
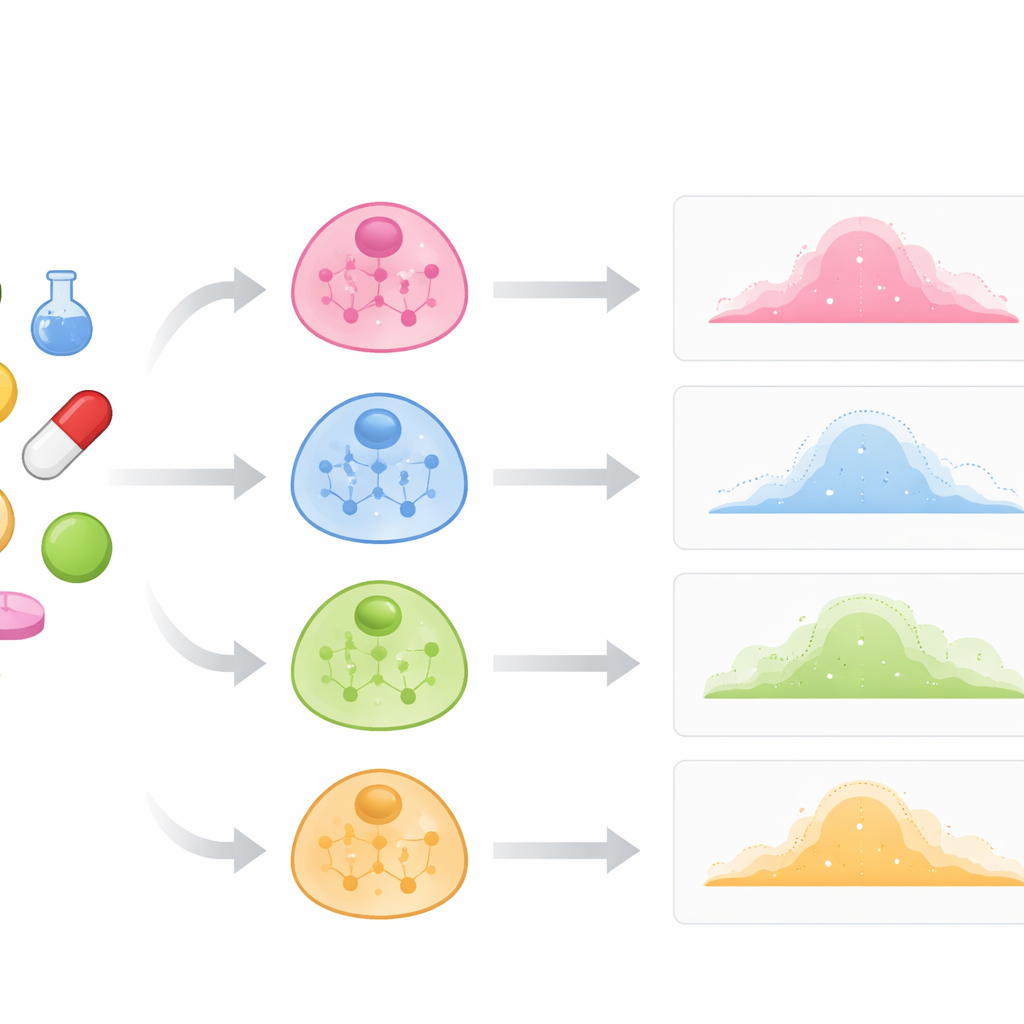
Смотреть внутрь клеток вместо того, чтобы обращать внимание только на препараты
Традиционные скрининги лекарств часто рассматривают клетки как однородные и в основном опираются на усреднённые показатели. На деле иммунные клетки, печёночные клетки и раковые клетки могут очень по‑разному реагировать на одно и то же соединение. Авторы утверждают, что для прогнозирования этих различий модель должна понимать внутреннюю схему работы каждого типа клеток: какие гены склонны проявлять совместную активность и как эти шаблоны определяют идентичность клетки. Они собирают «карты» типов клеток, анализируя, какие гены в неповреждённых (контрольных) клетках повышаются и понижаются синхронно. Каждая карта представлена в виде сети, где узлы соответствуют генам, а связи отражают сильную соактивность. Эти сети служат априорными знаниями о том, как устроен данный тип клеток до введения препарата.
Обучающий механизм, учитывающий сети
PrePR-CT объединяет три компонента: сеть активности генов для типа клетки, базовый уровень экспрессии генов этого типа и компактное представление химической структуры препарата. Модель использует класс нейронных сетей для графов, чтобы «переварить» генетическую сеть клетки и извлечь итоговое представление, отражающее её характерные паттерны. Параллельно каждый препарат преобразуется в числовой отпечаток, основанный на его молекулярной структуре. Эти фрагменты подаются в модуль предсказания, который, обучаясь на доступных экспериментах, определяет, как конкретный препарат смещает распределение активности генов в данном типе клеток. Вместо одного числа на ген метод оценивает как среднее изменение, так и вариабельность ответа между отдельными клетками — что важно для понимания как тонких, так и сильных эффектов.
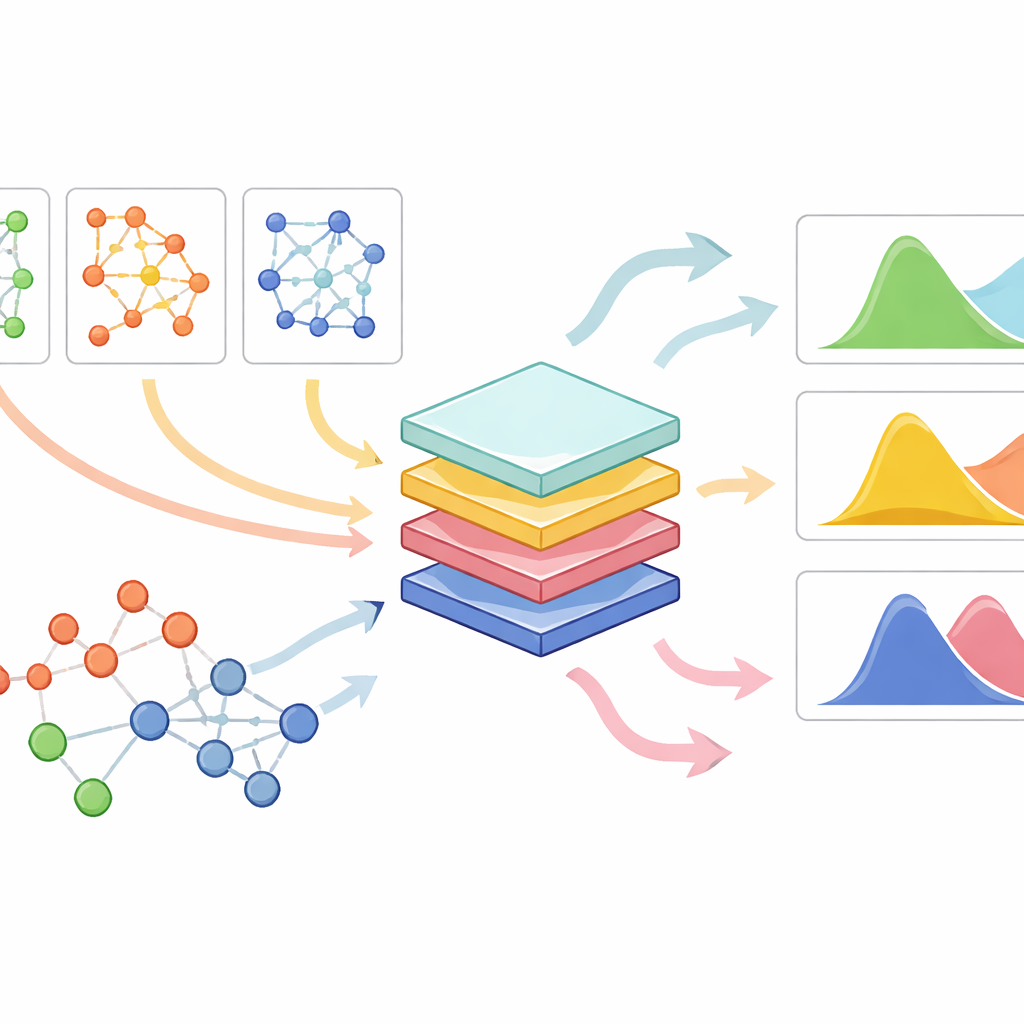
Работа с множеством типов клеток, препаратов и малыми наборами данных
Исследователи протестировали PrePR-CT на широкой коллекции наборов данных, включая человеческие кровяные клетки, подвергнутые иммунным сигналам, различные раковые клеточные линии, обработанные разными соединениями, печёночные клетки мыши, подвергнутые воздействию загрязнителя, и крупномасштабные скрининги лекарств из открытых ресурсов. В сложных сценариях, когда целый тип клеток исключали из обучения, модель всё равно могла предсказать, как этот новый тип отреагирует на знакомый препарат, часто с точностью, превосходящей ранние генеративные модели. Аналогично, когда исключали новый препарат при знакомом типе клеток, метод успешно прогнозировал его влияние, используя только химический отпечаток. Важно, что модель оставалась эффективной при обучении на относительно небольшом числе клеток — ситуации, в которой многие глубокие подходы испытывают трудности.
От «чёрного ящика» к подсказкам о механизме
Помимо чистого предсказания, авторы хотели понять, может ли модель дать представление о том, какие гены и пути управляют ответом клетки. Графовая архитектура включает механизм внимания, который выделяет гены, считающиеся моделью особенно влиятельными для каждого типа клеток. Многие из этих «высоко-внимательных» генов не совпадали с привычными кандидатами, выявляемыми стандартным анализом дифференциальной экспрессии, однако они сгруппировались в иммунно‑связанные пути, согласующиеся с биологией тестируемых препаратов. Когда исследователи целенаправленно нарушали влияние этих важных генов во входных данных модели, качество предсказаний падало, особенно для наиболее отзывчивых генов, что указывает на то, что оценки внимания отражают значимые механистические участники, а не шум.
Что это значит для разработки лучших лекарств
Проще говоря, работа показывает, что предоставление моделям ИИ структурированного представления того, как устроен каждый тип клеток — его внутренней генетической сети — существенно улучшает их способность прогнозировать, как препараты изменят эти клетки, даже при умеренных объёмах данных. PrePR-CT не заменяет эксперименты, но помогает сократить количество кандидатов и типов клеток, которые стоит тестировать, и даёт подсказки, почему те или иные клетки реагируют так, а не иначе. По мере роста наборов данных и включения дополнительных клеточных признаков такие подходы могут стать ключевыми инструментами для адаптации терапий к конкретным тканям или типам клеток пациента, снижая метод проб и ошибок в лаборатории и приближая более точные лекарства к применению.
Цитирование: Alsulami, R., Lehmann, R., Khan, S.A. et al. Predicting and interpreting cell-type-specific drug responses in the small-data regime using inductive priors. Nat Mach Intell 8, 461–473 (2026). https://doi.org/10.1038/s42256-026-01202-2
Ключевые слова: прогнозирование ответа на препарат, одноядерная транскриптомика, графовые нейронные сети, поиск лекарств, клеточная специфичность