Clear Sky Science · ru
Условная диффузия с локально-ориентированным согласованием модальностей для генерации разнообразных ансамблей конформаций белков
Почему движение белков важно
Белки в наших клетках — это не жёсткие скульптуры; они ближе к крошечным гибким механизмам, которые постоянно меняют форму. Эти изменения формы могут управлять тем, как ферменты катализируют реакции, как рецепторы реагируют на лекарства и как сигналы передаются внутри клетки. Тем не менее большинство привычных изображений белков показывают лишь одну «снимочную» структуру, упуская богатый ансамбль форм, которые действительно существуют. В этой статье представлен Mac-Diff, метод искусственного интеллекта, который быстро генерирует множество правдоподобных форм для данного белка, помогая учёным увидеть не только то, как белок выглядит, но и как он «дышит» и движется.
От одиночных снимков к движущимся ансамблям
Долгие годы исследователи полагались на трудоёмкие эксперименты или длительные молекулярно-динамические симуляции, чтобы изучать движения белков — оба подхода могут быть медленными и дорогими. Прорывные инструменты вроде AlphaFold2 сейчас предсказывают наиболее вероятную 3D-структуру белка прямо по аминокислотной последовательности, но обычно возвращают лишь одну или несколько предпочтительных форм. Многие белки, особенно те, что участвуют в сигнальной и аллостерической регуляции, естественным образом занимают несколько, слабо определённых состояний. Авторы утверждают, что чтобы понять, как такие белки действительно работают — и чтобы проектировать лекарства, связывающиеся с менее очевидными, переходными формами — нам нужен способ генерировать целые ансамбли правдоподобных конформаций, а не только одну лучшую догадку.
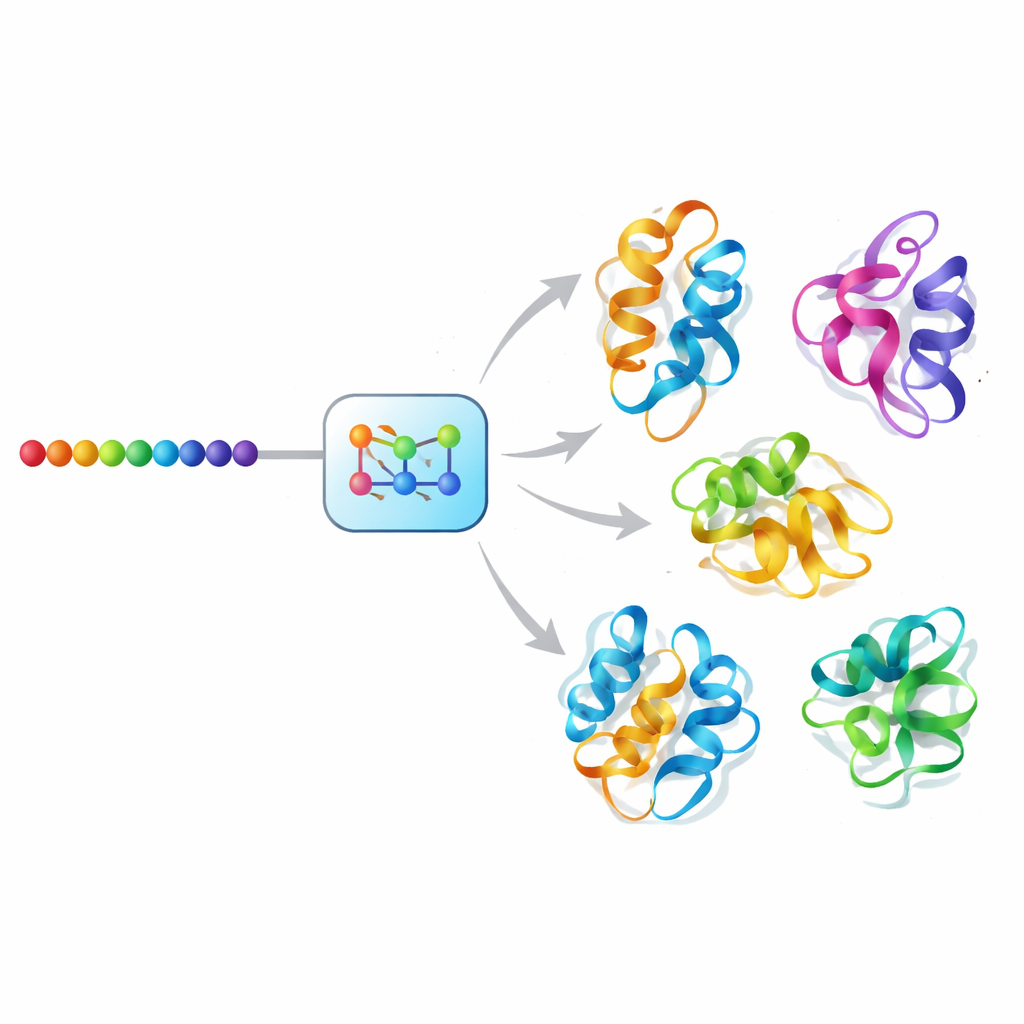
AI-подход «диффузии» к движению белков
Mac-Diff решает эту задачу с помощью генеративной модели в стиле диффузии — класса ИИ, обеспечившего недавний прогресс в синтезе изображений. Вместо удаления шума с фотографий Mac-Diff удаляет шум с абстрактных геометрических описаний каркасов белков. Модель представляет белок как сетку парных взаимосвязей между его остатками — расстояния и углы, нечувствительные к общему повороту или переносам молекулы. На прямом этапе система постепенно добавляет шум к этим геометрическим паттернам, пока они не начнут напоминать случайный статический шум. На обратном этапе она учится по шагам убирать шум, управляемая аминокислотной последовательностью белка, пока снова не появятся связные геометрии, совместимые с 3D, которые затем можно преобразовать в полные атомные модели стандартным программным обеспечением построения структур.
Дать последовательности общаться со структурой локально
Ключевое нововведение — то, как Mac-Diff связывает линейную последовательность остатков с их 3D-соседями. Простое разрешение каждому остатку «внимательно смотреть» на все остальные остатки, как в моделях «текст-в-изображение», размывало бы важные физические ограничения. Вместо этого авторы вводят механизм внимания, «осознающий локальность», который фокусирует каждый остаток на небольшом, вероятном окружении партнёров по взаимодействию. Для оценки этих окрестностей Mac-Diff использует три компонента: языковую модель белков ESM-2, кодирующую биохимический контекст каждого остатка; карту контактов, подсказывающую, какие пары остатков вероятно окажутся рядом; и простое правило, отдающее предпочтение остаткам, близким друг к другу вдоль цепи. Эти сигналы комбинируются так, что в процессе удаления шума модель преимущественно использует информацию от физически правдоподобных партнёров, повышая способность восстанавливать реалистичные гибкие структуры.
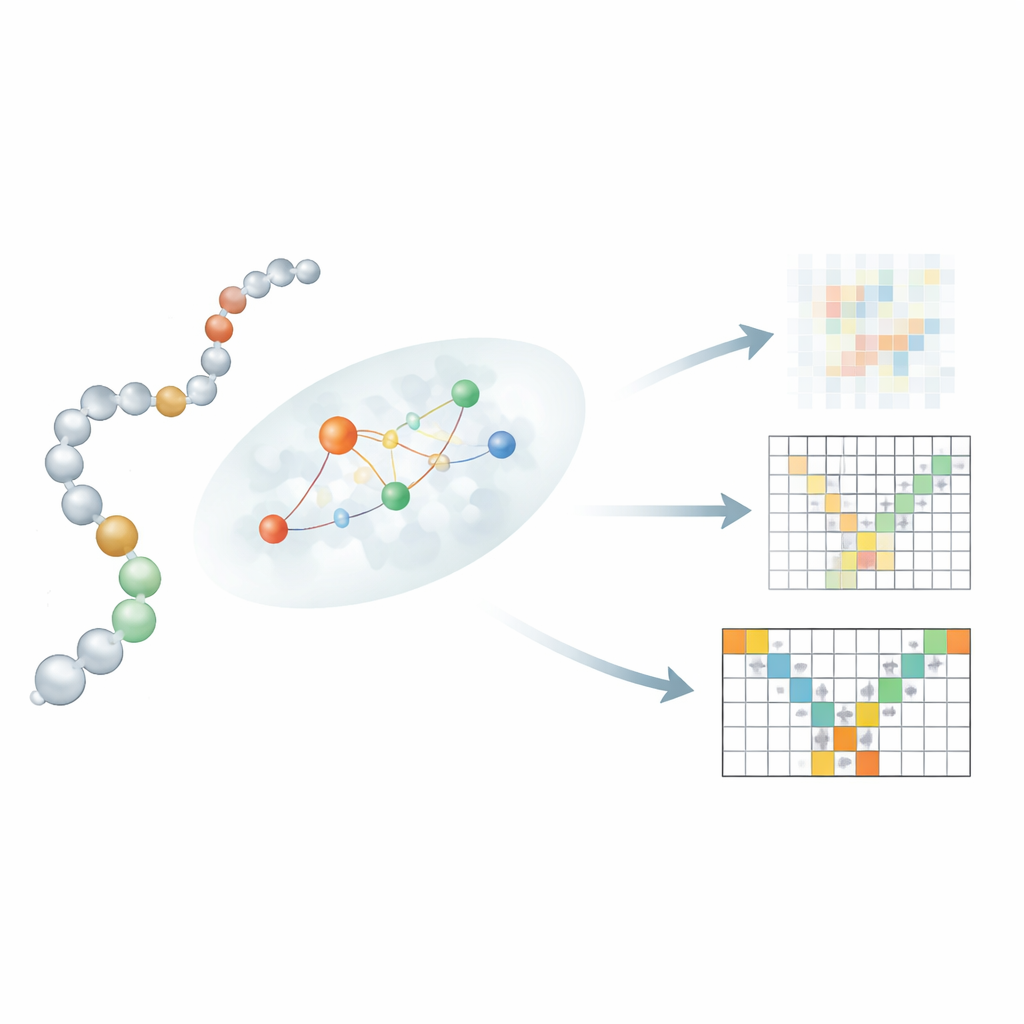
Тестирование против долгих симуляций и белков с меняющейся формой
Исследователи проверили Mac-Diff по двум требовательным направлениям. Во‑первых, они спросили, может ли он воспроизвести широкое распределение форм, наблюдаемое в длительных, тщательно рассчитанных молекулярно-динамических симуляциях быстро складывающихся белков и классического эталонного белка BPTI. По нескольким метрикам, сравнивающим статистические свойства сгенерированных ансамблей с данными симуляций — таким как распределения внутримолекулярных расстояний и общая компактность — Mac-Diff соответствовал или превосходил конкурирующие методы ИИ, одновременно генерируя более широкий спектр конформаций. Он захватывал большинство ключевых «метастабильных» состояний, выявленных в симуляциях, и воспроизводил паттерны гибкости на уровне остатков с высокой корреляцией, что указывает на то, что его ансамбли реалистично отражают как глобальные складывания, так и локальные колебания.
Выявление скрытых функциональных состояний
Во‑вторых, команда испытала Mac-Diff на белках, известных тем, что принимают очень разные формы в процессе выполнения своих функций, включая фермент аденилаткиназу, который переключается между открытой и закрытой формами в ходе метаболизма энергии, и тщательно подобранный набор из 40 белков, для каждого из которых экспериментально определены две конформации. Mac-Diff сгенерировал всего по 100 кандидатных структур на белок — гораздо меньше, чем типичные траектории симуляций — и при этом восстановил большинство известных состояний с хорошим геометрическим соответствием. Например, в случае аденилаткиназы он создал и открытую, и закрытую конформации с высокой схожестью с кристаллическими структурами, тогда как некоторые популярные методы склонялись к предпочтению только одного состояния. Модель также работала примерно в тысячу раз быстрее, чем традиционные симуляции на сопоставимом оборудовании, что делает систематическое исследование разнообразия форм значительно более практичным.
Что это значит для биологии и медицины
Проще говоря, Mac-Diff превращает последовательность белка в галерею правдоподобных поз, а не в один портрет, причём учитывает, какие части вероятнее всего будут подталкивать или обхватывать друг друга в 3D. Благодаря точной и эффективной выборке таких ансамблей метод позволяет исследовать, как тонкие сдвиги формы лежат в основе функций, обнаруживать редкие, но важные конформации и искать сайты связывания лекарств, появляющиеся только в переходных состояниях. Хотя он пока не воспроизводит полностью упорядоченные во времени «фильмы», которые дают симуляции, Mac-Diff делает динамический ландшафт белков доступным для гораздо большего числа систем, обещая новые сведения в структурной биологии, разработке лекарств и инженерии белков.
Цитирование: Wang, B., Wang, C., Chen, J. et al. Conditional diffusion with locality-aware modal alignment for generating diverse protein conformational ensembles. Nat Mach Intell 8, 415–434 (2026). https://doi.org/10.1038/s42256-026-01198-9
Ключевые слова: динамика белков, модели диффузии, ансамбли конформаций, аллостерические белки, поиск лекарств