Clear Sky Science · ru
Фосфорилирование PLIN5 организует связывание митохондрий с липидными каплями для контроля липидного потока в печени и стеатоза
Почему важно жир в печени
У многих людей в печени откладывается лишний жир, и при этом они не чувствуют себя больными, но это тихое накопление со временем может привести к воспалению, рубцеванию и даже к раку. В этом исследовании ставится простой, но ключевой вопрос: когда в печень поступают волны жира во время голодания или с калорийной «западной» диетой, как клетки печени решают, будет ли этот жир сжигаться для выработки энергии или безопасно храниться, и когда эта система защиты начинает давать сбой?
Маленькие электростанции и крошечные жировые пузырьки
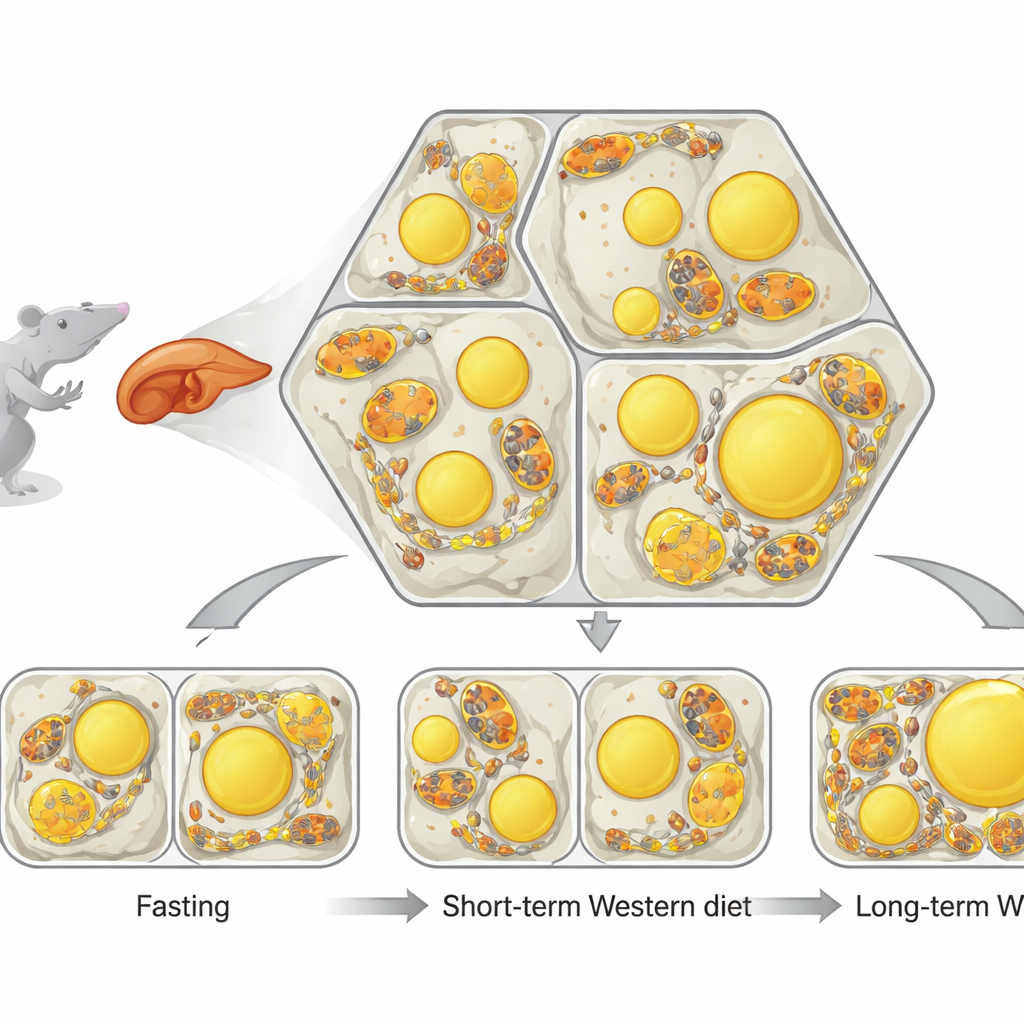
Печень организована в повторяющиеся шестиугольные единицы, через которые течёт кровь с одной стороны на другую. По этому пути клетки печени специализированы: одни в основном сжигают жир для получения энергии, другие — образуют и откладывают жир. Внутри каждой клетки ключевую роль играют две структуры. Митохондрии — это энергетические станции клетки, а липидные капли — маленькие заполненные жиром пузырьки для хранения. Исследователи разработали мощный конвейер визуализации и анализа, называемый фено́типическим профилированием одиночных клеток (scPhenomics), чтобы картировать размер, форму и расположение этих структур в тысячах клеток прямо в срезах ткани. Они обнаружили, что даже у здоровых животных форма митохондрий и содержание липидных капель образуют отчётливые пространственные узоры, которые отражают зоны, где обычно преобладает сжигание по сравнению с хранением.
Голодание против калорийной диеты
Далее команда выясняла, что происходит, когда печень внезапно наполняется жиром. При голодании жир высвобождается из жировых депо и поступает в печень, тогда как кратковременная западная диета приносит дополнительный жир прямо с пищей. У голодавших мышей количество липидных капель увеличилось по всей печени, а митохондрии удлинились и часто тесно обволакивали эти жировые пузырьки, образуя множество контактных участков. У мышей, которых кормили западной диетой в течение нескольких недель, печень тоже наполнилась жиром, но капли были организованы иначе, а митохондрии оставались в основном раздельными и более округлыми. Это показало, что путь поступления жира — через голодание или хроническое богатое питание — вызывает очень разные структурные ответы в клетках печени, даже если общий уровень жира выглядит схожим.
Молекулярный переключатель для обращения с жиром
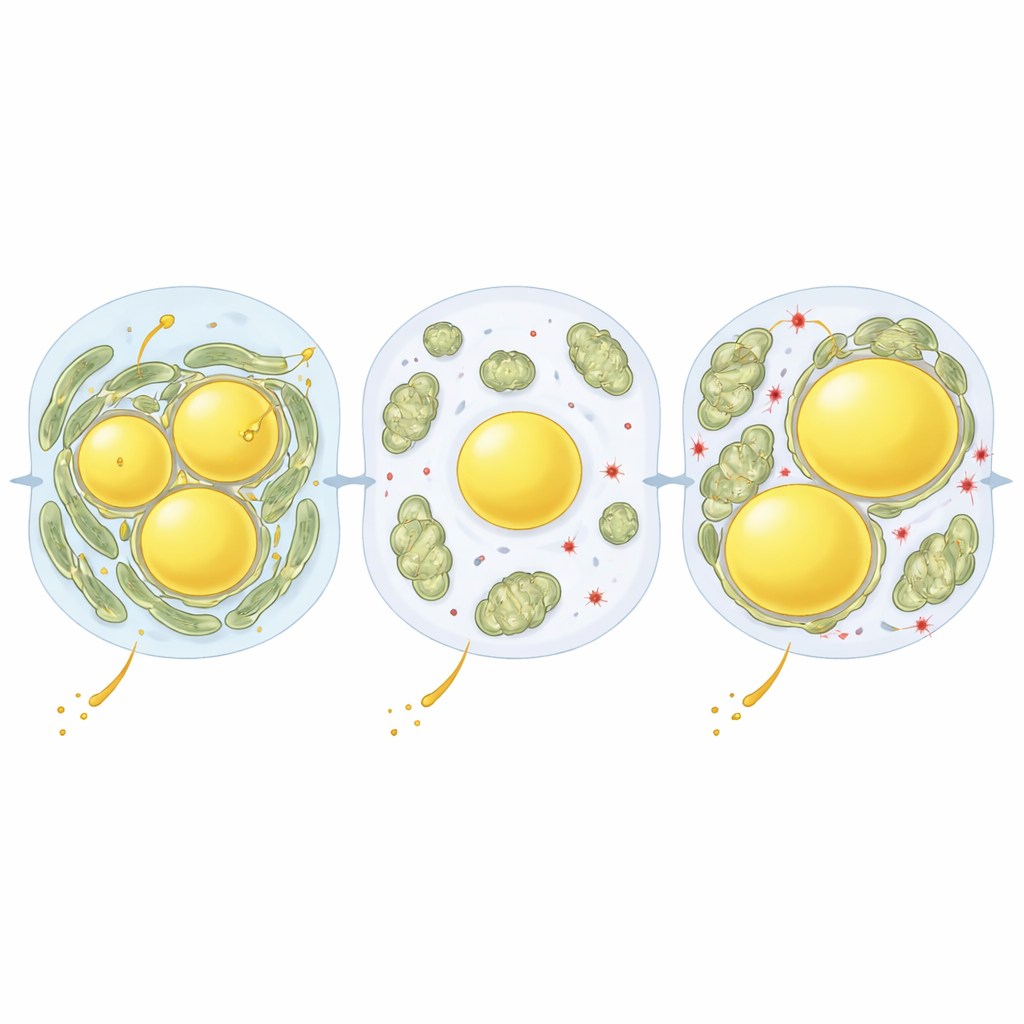
Чтобы выяснить, что управляет этими контактами органелл, авторы совместили их визуализацию с измерениями белков в клетках печени, взятых из разных зон и условий диеты. Одним из заметных белков оказался перилипин‑5 (PLIN5), который покрывает липидные капли и может связывать митохондрии с ними. При голодании уровень PLIN5 повышался и он располагался прямо на интерфейсе между митохондриями и каплями. Затем исследователи использовали печёночно-ориентированный вирус, чтобы повысить уровень PLIN5 и протестировать варианты белка, имитирующие разные «включённые/выключенные» состояния одного химического маркера — фосфорилирования. Вариант, который не может быть фосфорилирован (S155A), сильно увеличивал контакты митохондрий с каплями и приводил к увеличению жировых капель, даже при нормальной диете. Вариант, имитирующий постоянное фосфорилирование (S155E), действовал наоборот: митохондрии редко касались капель, которые оставались менее многочисленными и меньшими по размеру.
Защита клеток от повреждений, вызванных жиром
Команда затем изучила, что это означает для здоровья печени при западной диете. Когда мыши несколько недель питались этой диетой, нефосфорилируемый вариант PLIN5 (S155A) направлял больше жира в капли и повышал содержание триглицеридов в печени, однако маркеры повреждающего окислительного стресса фактически были ниже. Напротив, фосфо-имитирующая версия (S155E) оставляла больше свободного жира и признаки более окисляющей, потенциально вредной среды с меньшими запасами антиоксидантов. По сути, тесные взаимодействия между митохондриями и липидными каплями казались предохранительным клапаном, перенаправляя избыток жирных кислот в нейтральное хранение в виде триглицеридов и ограничивая цепные химические реакции, повреждающие мембраны и белки. Однако при длительном кормлении западной диетой контакты митохондрий с каплями снова увеличивались и ассоциировались с более тяжёлым накоплением жира как у мышей, так и в образцах человеческой печени, наводя на мысль, что та же защитная схема может перегружаться и способствовать прогрессированию болезни.
Новый подход к заболеванию жировой печени
В целом эта работа показывает, что клетки печени активно перенастраивают физические отношения между своими энергетическими станциями и складами жира, чтобы справляться с меняющимися питательными условиями. PLIN5, и в частности его состояние фосфорилирования в одной позиции, действует как точный регулятор, который укрепляет или ослабляет связь митохондрий с липидными каплями. Тесная связь способствует упаковке потенциально токсичных свободных жиров в более безопасные запасы триглицеридов и помогает сглаживать кратковременные пищевые стрессы, такие как голодание или кратковременное воздействие богатой диеты. Когда эта адаптивная программа ослабляется, или когда длительное воздействие высокожировой диеты продолжается месяцы или годы, равновесие смещается в сторону липотоксичности и окислительного повреждения. Описав эту структурную «схему» внутри клеток печени, исследование предполагает, что препараты, модулирующие активность PLIN5 или контакты митохондрий с каплями, могут предложить новый путь замедления или предотвращения жировой болезни печени у людей.
Цитирование: Kang, S.W.S., Brown, L.A., Miller, C.B. et al. PLIN5 phosphorylation orchestrates mitochondria lipid-droplet coupling to control hepatic lipid flux and steatosis. Nat Metab 8, 587–603 (2026). https://doi.org/10.1038/s42255-026-01476-1
Ключевые слова: жировая болезнь печени, метаболизм печени, митохондрии, липидные капли, перилипин 5