Clear Sky Science · ru
PFKM управляет метаболическими сдвигами в процессе дифференцировки скелетной мышцы
Почему мышечным клеткам нужен умный подход к использованию сахара
Когда мы тренируемся или просто встаём со стула, скелетные мышцы немедленно включаются в работу, сжигая сахар для питания каждого сокращения. Но молодые мышечные стволовые клетки и полностью сформированные мышечные волокна обращаются с сахаром по‑разному. В этом исследовании описана встроенная переключающая система — в центре которой один фермент PFKM — которая определяет, сжигать ли глюкозу для немедленной энергии или перенаправлять её для защиты и восстановления клеток. Понимание этого переключателя может открыть новые пути терапии мышечной слабости, возрастных изменений мышц и наследственных метаболических заболеваний.
Светофор для клеточного топлива
Проникающая в клетку глюкоза может идти по нескольким путям. Один крупный путь, гликолиз, быстро превращает сахар в энергию и строительные блоки для растущих мышечных волокон. Другой путь, пентозофосфатный путь, даёт молекулы, защищающие клетки от окислительного стресса, и поддерживает синтез ДНК и липидов. Исследователи сосредоточили внимание на PFKM — варианте фосфофруктокиназы‑1, стоящем на ключевом ответвлении гликолиза. Измеряя сотни метаболитов в течение минут и часов после активации сигнала роста Wnt, они обнаружили быстрый накопление ранних промежуточных продуктов гликолиза при одновременном падении продукта, контролируемого PFKM, и росте метаболитов пентозофосфатного пути. Это наводит на мысль, что клетки активно «прижимают» PFKM, чтобы перенаправить сахар в защитную химию вместо простого производства энергии. 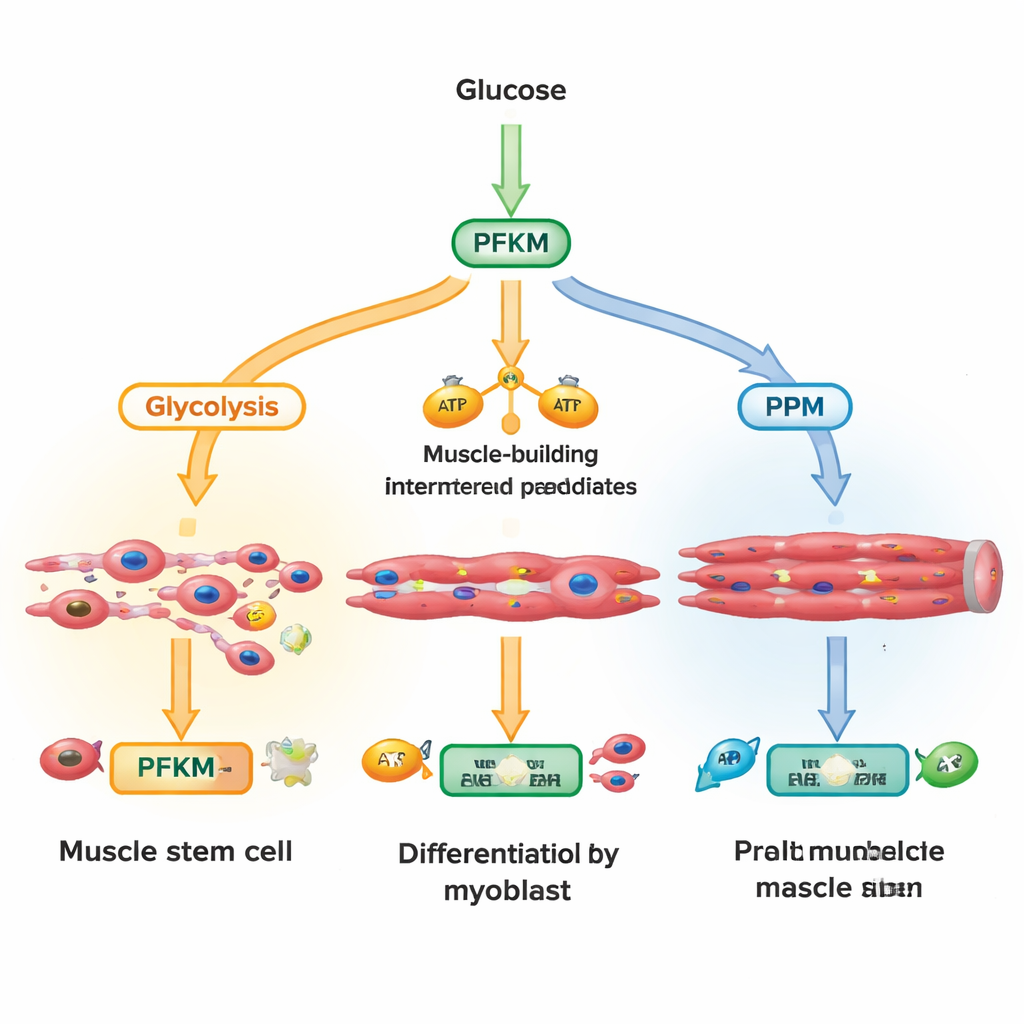
Метка и удаление «привратника» фермента
Чтобы понять, как контролируется PFKM, команда проследила локализацию белка в клетках. В покое PFKM распределялся по цитоплазме. Через несколько минут после стимуляции Wnt он собрался в яркие точки, совпадающие с лизосомами — клеточными отделениями для разрушения белков. Две родственные изоформы, PFKL и PFKP, не перемещались и их уровни не менялись, что указывает на то, что целью был только мышечный PFKM. Биохимические тесты показали, что блокирование функции лизосом предотвращало потерю PFKM, тогда как ингибирование протеасомы — другой основной системы утилизации белка — не влияло на это. Анализ последовательности выявил короткий мотиф «метил-аргинин дегрон», уникальный для PFKM. Фермент PRMT1 добавлял специфическую метильную метку на аргинин в этом мотife, и эта метка позволяла механизму микроаутопагии, включая белок VPS4, втягивать PFKM в лизосомы для деградации. Отключение PRMT1 или VPS4 стабилизировало PFKM и блокировало его удаление.
От стволовой клетки к работающему мышечному волокну
Используя крупные наборы данных по отдельным человеческим клеткам, авторы сопоставили уровни PFKM в разных типах мышечных клеток. Мышечные стволовые клетки, находящиеся в состоянии покоя до востребования при ремонте, имели очень мало PFKM, но при этом экспрессировали многие гены пентозофосфатного пути и компоненты лизосом. По мере того как клетки становились предопределёнными к образованию мышц и сливались в многоядерные волокна, транскрипты и белок PFKM резко возрастали, в то время как таргеты Wnt и лизосомные гены снижались. В культурах человеческих и мышиных мышечных клеток Wnt быстро направлял PFKM в лизосомы в ранних одноядерных клетках, но не в зрелых многоядерных волокнах. Эта картина поддерживает модель, в которой недифференцированные клетки держат PFKM на низком уровне — через лизосомную деградацию — чтобы благоприятствовать защитному метаболизму, а затем вновь экспрессируют его по мере перехода в энергозатратные сократительные волокна.
Что происходит, когда переключатель «застревает»
Чтобы проверить, насколько важен PFKM для формирования мышц, команда снизила его уровни с помощью РНК‑интерференции. Клетки с низким PFKM испытывали трудности с запуском характерных мышечных генов, производили меньше миозина и формировали меньше и меньших по размеру многоядерных волокон, хотя общее число клеток не изменилось. Профилирование метаболитов показало снижение downstream‑посредников гликолиза и субстратов цикла трикарбоновых кислот, но увеличение генов и маркеров пентозофосфатного пути, а также повышенную устойчивость к окислительному стрессу. Важно, что подача клеткам 3‑фосфоглицерата — промежуточного продукта гликолиза, который обычно лежит ниже по потоку от PFKM — спасала многие дефекты дифференцировки. Мышечные маркеры и образование волокон восстанавливались, что показывает: главным узким местом были недостающие метаболиты, а не отсутствие самого белка PFKM. 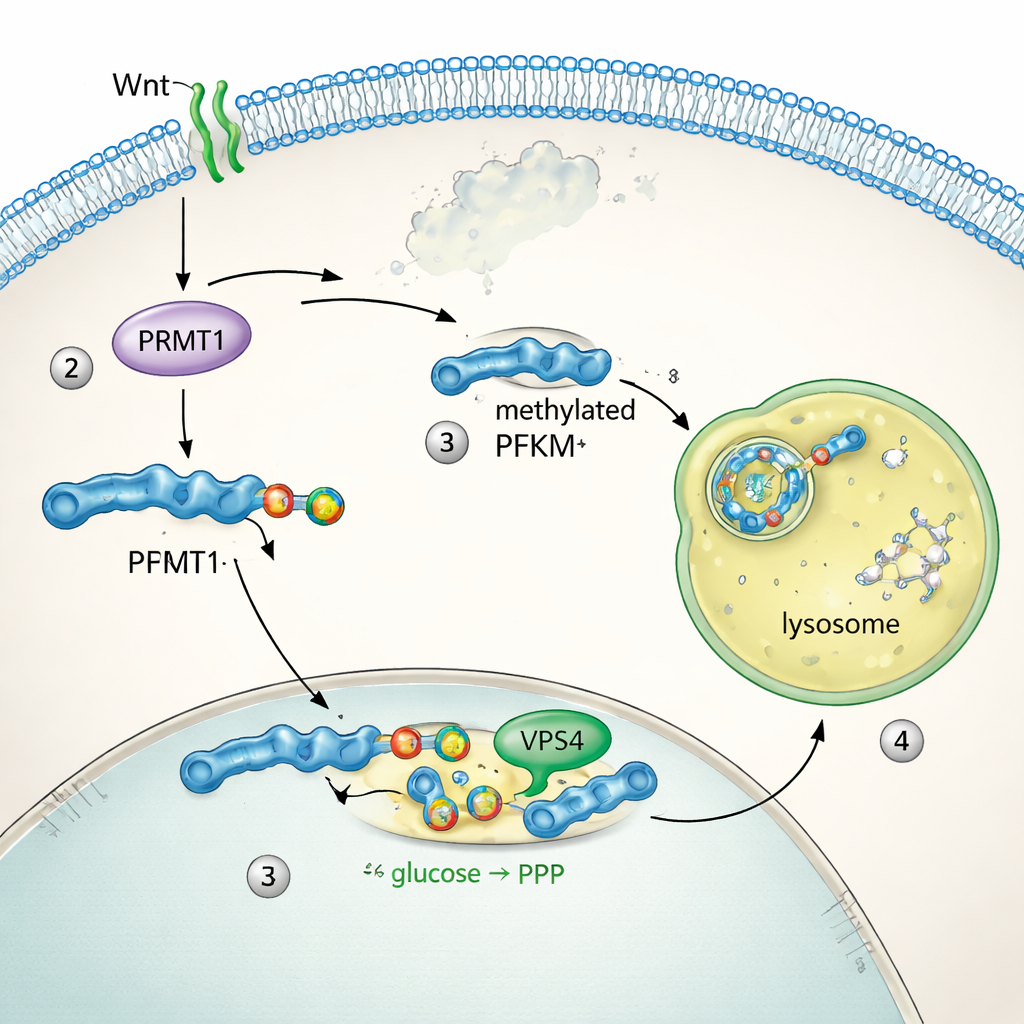
Последствия для здоровья и восстановления мышц
Неспециалисту главное сообщение состоит в том, что мышечные клетки не просто «больше или меньше сжигают сахар»; они тонко перенаправляют его между выработкой энергии и защитой клеток в зависимости от стадии своего развития. PFKM действует как регулируемый клапан на этом ответвлении. В клетках, похожих на стволовые, Wnt‑обусловленная маркировка и лизосомное уничтожение PFKM перенаправляют глюкозу в путь, который защищает клетки и готовит их к будущему росту. По мере созревания в работающие волокна клетки восстанавливают запасы PFKM и переводят метаболизм в режим высокой выработки энергии. Нарушение этого баланса, как в редких дефектах PFKM, срывает нормальное развитие мышц. Раскрывая молекулярную «ручку» этого переключателя, исследование намекает, что в будущем можно будет тонко настраивать регенерацию мышц или защищать мышцы при заболеваниях и старении путём умеренной коррекции активности PFKM или поставки нужных downstream‑метаболитов.
Цитирование: Campos, M., Nguyen, S.T., Kong, X. et al. PFKM governs metabolic shifts throughout skeletal muscle differentiation. Nat Metab 8, 489–505 (2026). https://doi.org/10.1038/s42255-026-01457-4
Ключевые слова: дифференцировка скелетной мышцы, метаболизм глюкозы, фермент PFKM, пентозофосфатный путь, лизосомный протеолиз