Clear Sky Science · ru
Эктопическая экспрессия цитозольной DHODH отделяет синтез пиримидинов de novo от митохондриального электронного транспорта
Почему важно разорвать скрытую связь в наших клетках
Каждая клетка вашего тела постоянно копирует и ремонтирует свою ДНК — процесс, требующий непрерывного поступления химических «букв», называемых пиримидинами. У большинства животных синтез этих букв тесно связан с тем, как митохондрии — энергетические станции клетки — окисляют топливо с участием кислорода. Такое сцепление означает, что при нарушении митохондриального дыхания запасы строительных блоков ДНК сокращаются, и клетки перестают расти. Резюме исследования, приведённое здесь, показывает, что заимствование одного гена из хлебопекарных дрожжей позволяет чётко разорвать эту связь. Эта генетическая модификация даёт млекопитающим клеткам возможность продолжать синтез пиримидинов даже при нарушенной функции митохондрий — открывая новый путь для изучения и, возможно, в будущем — лечения заболеваний, связанных с нарушением энергетического метаболизма.
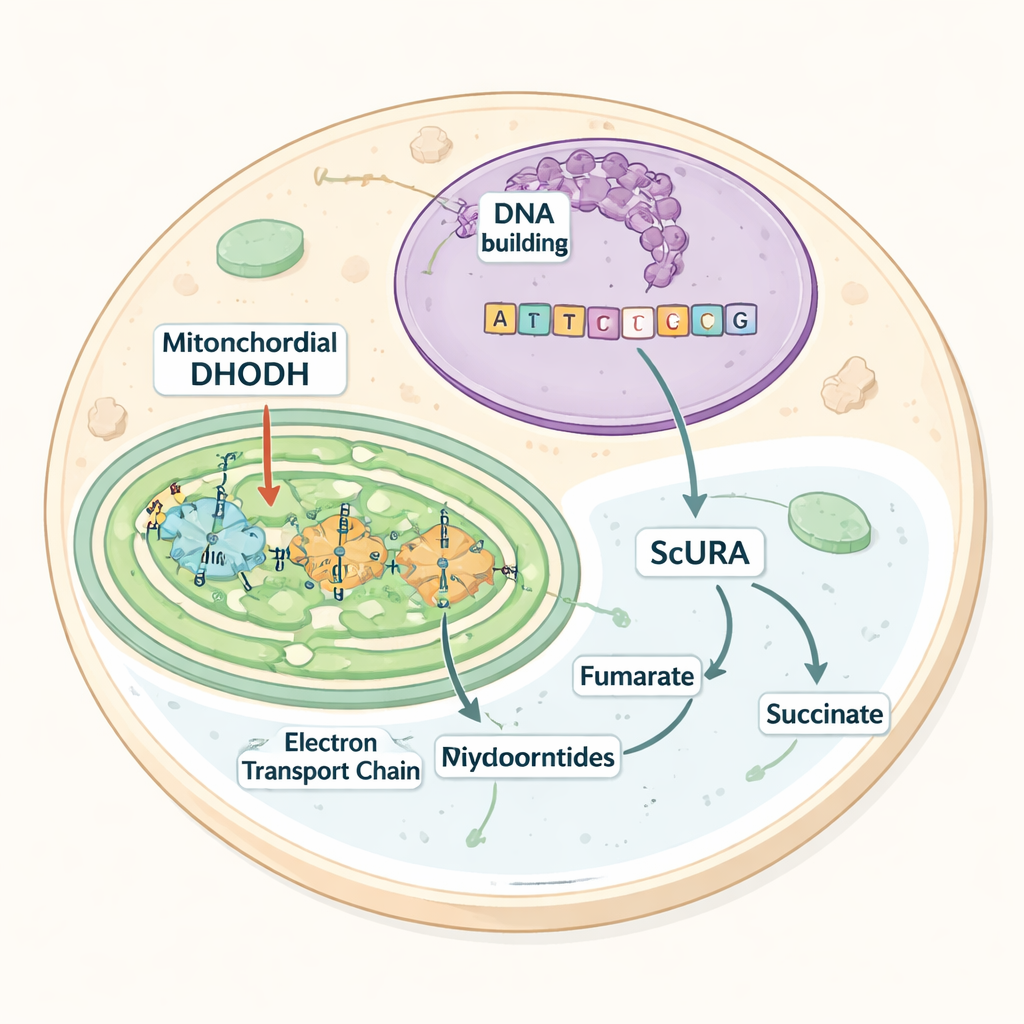
Заимствованный инструмент от дрожжей
Работа сосредоточена на ферменте дигидрооротат дегидрогеназе (DHODH), который выполняет ключевой шаг в синтезе пиримидинов. У млекопитающих DHODH располагается во внутренней мембране митохондрий и передаёт электроны переносчику, питающему дыхательную цепь. Если этот электронный поток блокируется — например, ингибиторами лекарств или генетическими дефектами — DHODH останавливается, синтез пиримидинов прекращается, и клетки становятся зависимы от пищевого или добавочного уридина, готового строительного блока. Многие микроорганизмы, способные жить без кислорода, обходят это узкое место, используя альтернативные версии DHODH, плавающие в цитозоле и использующие другие акцепторы электронов. Авторы задали вопрос, можно ли внедрить такой кислородонезависимый маршрут в млекопитающие клетки.
Перепрограммирование способа производства «букв» ДНК
Исследователи ввели ген URA1 из дрожжей Saccharomyces cerevisiae в человеческие клетки. URA1 кодирует цитозольный фермент, названный ScURA, который выполняет тот же химический шаг, что и митохондриальная DHODH, но передаёт электроны молекуле фумарата вместо митохондриального переносчика. Биохимические тесты показали, что ScURA формирует активные димеры в цитозоле и добавляет новую активность DHODH, устойчивую к препаратам. При нормальных условиях введение ScURA не нарушало структуру митохондрий, дыхание или рост, что указывает на то, что он функционирует как резервный путь, а не как дополнительная нагрузка.
Клетки, не обращающие внимания на митохондриальные препятствия
Чтобы проверить, сможет ли этот резервный путь заменить нативную систему, команда химически блокировала либо сам DHODH, либо митохондриальную цепь переноса электронов — воздействия, которые обычно останавливают деление клеток, если не добавлять уридин. Клетки, экспрессирующие ScURA, продолжали пролиферировать без какой-либо помощи, даже при сильной ингибиции комплекса III дыхательной цепи или после генетического удаления эндогенного гена DHODH. Подробное трассирование азота и углерода из меченого глутамина показало, что клетки с ScURA продолжали синтез пиримидиновых нуклеотидов несмотря на эти блоки. Измерения метаболитов выявили, что вместо накопления токсичных прекурсоров клетки ScURA направляли электроны на фумарат, продуцируя сукцинат и тонко перестраивая цикл трикарбоновых кислот (TCA) в поддержку шунта фумарат–сукцинат между цитозолем и митохондриями.
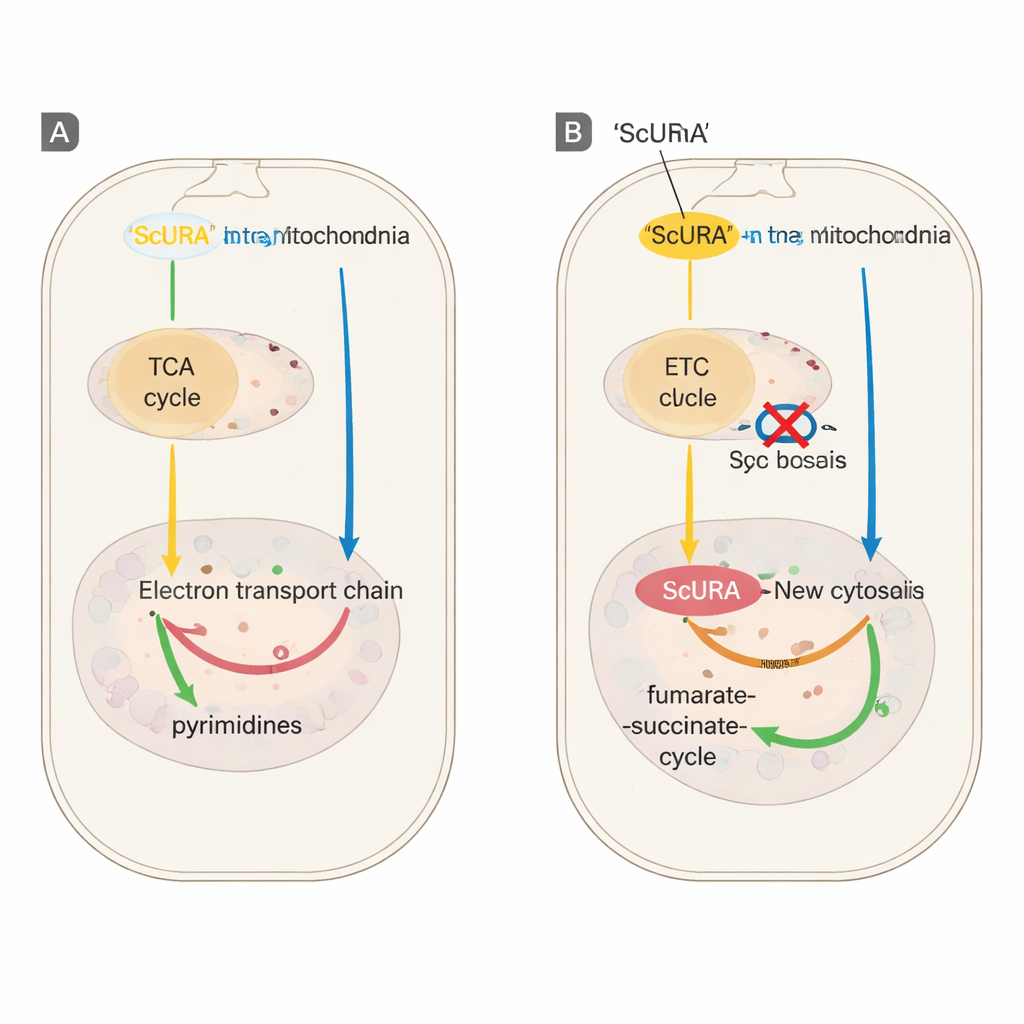
Спасение клеток с повреждёнными электростанциями
Авторы затем протестировали ScURA в моделях клеток с митохондриальными заболеваниями. Клетки без митохондриальной ДНК или несущие мутации, разрушающие комплексы III или IV дыхательной цепи, обычно зависят от добавленного уридина для роста. После инженерной экспрессии ScURA эти разнообразные мутантные клетки смогли пролиферировать без уридина, хотя им всё ещё требовался пируват, что отражает сохраняющуюся необходимость в некоторой митохондриальной активности. На уровне экспрессии генов ScURA также предотвращал выключение генов рибосомальных белков, которое обычно следует за хронической ингибиции электронного транспорта, удерживая запасы пиримидиновых строительных блоков достаточно высокими для поддержания синтеза РНК.
Что это значит для здоровья и болезней
Чётко отделив синтез пиримидинов от митохондриального дыхания, ScURA даёт исследователям мощный новый рычаг: теперь можно в ряде случаев проверить, действительно ли тот или иной дефект или эффект препарата вызван потерей энергообеспечения или же нехваткой предшественников ДНК и РНК. В долгосрочной перспективе аналогичные стратегии могут дополнить существующие генотерапии для митохондриальных расстройств или помочь объяснить, почему некоторые опухоли настолько зависят от восстановления функции митохондрий. Хотя перенос дрожжевого фермента в клиническое лечение потребует большой осторожности, это исследование демонстрирует, что один тщательно подобранный ген может переписать фундаментальную метаболическую связь, которую эволюция долгое время удерживала взаимосвязанной.
Цитирование: Curtabbi, A., Jaroszewicz, S.N., Sanz-Cortés, R. et al. Ectopic expression of cytosolic DHODH uncouples de novo pyrimidine biosynthesis from mitochondrial electron transport. Nat Metab 8, 454–466 (2026). https://doi.org/10.1038/s42255-026-01454-7
Ключевые слова: метаболизм пиримидинов, функция митохондрий, цепь переноса электронов, перепрограммирование обмена веществ, митохондриальная болезнь