Clear Sky Science · ru
Регулируемый приемом пищи метаболизм гликогена задает ритмичную секрецию белков печенью
Почему суточный ритм печени важен
Большинство из нас думает о том, что мы едим, но редко задумывается, когда печень тихо упаковывает и отправляет жизненно важные белки в кровь. Это исследование показывает, что «график доставки» печеночных белков далек от постоянного: он следует суточному ритму, который сильно зависит от времени приема пищи и от того, как печень использует запасенный сахар — гликоген. Понимание этой часовой системы помогает объяснить, почему режим питания, ожирение и некоторые редкие генетические болезни могут нарушать уровни гормонов, факторов свертывания и многих других кровяных белков, поддерживающих гомеостаз организма.
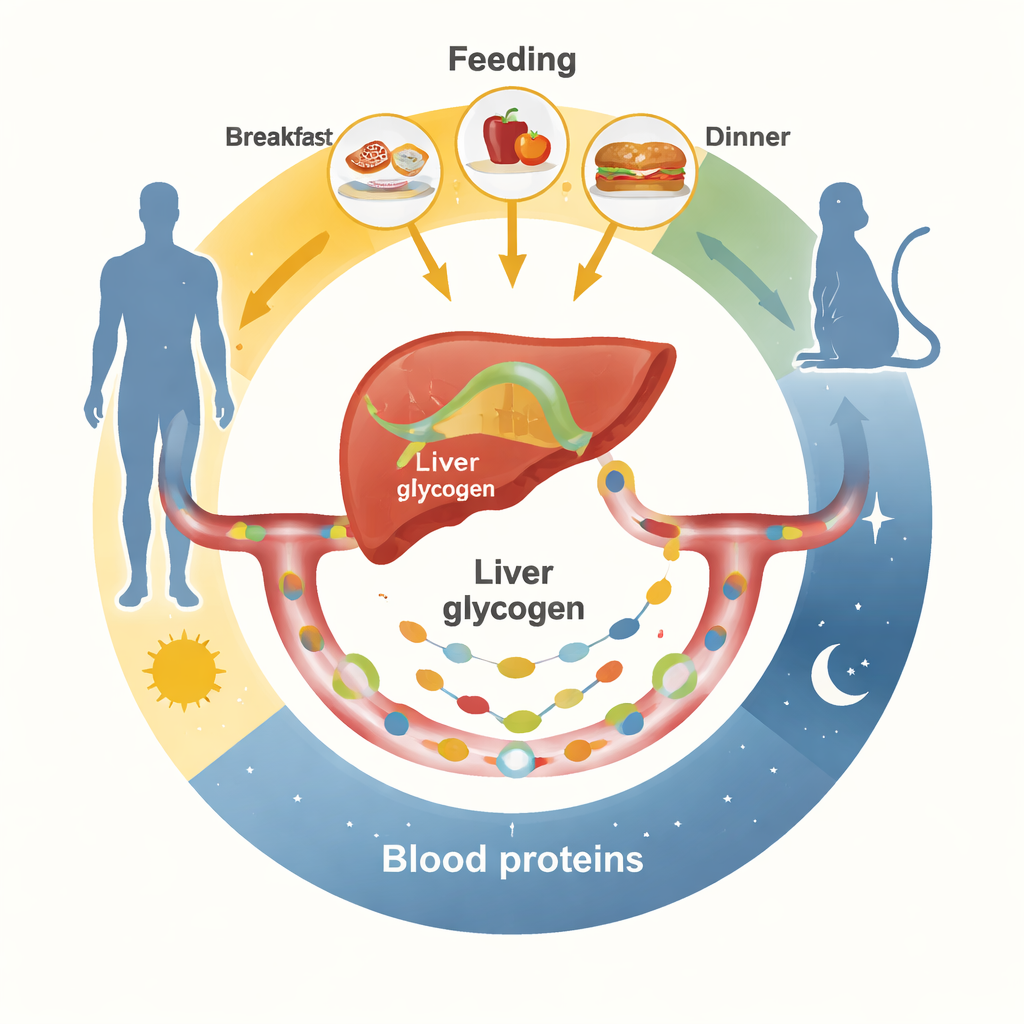
Приемы пищи задают ритм кровяным белкам
Исследователи сначала отслеживали сотни белков в крови в течение 24 часов у здоровых мужчин при двух контролируемых режимах питания. В одном случае добровольцы ели обычными приемами пищи; в другом — те же калории распределялись равномерно в течение бодрствующего дня. При регулярных приемах многие белки в крови поднимались и падали в определенных суточных волнах, часто достигая пиков ранним утром и поздним днем. К ним относились метаболические гормоны, факторы свертывания, белки иммунной системы и транспортные белки, в основном синтезируемые печенью. Когда еду потребляли медленно и равномерно в течение дня, большинство этих ритмов выравнивалось. Похожими оказались эксперименты на мышах: при неограниченном доступе к еде или при питании в определенные дневные или ночные окна изменение графика кормления существенно перестраивало, какие белки в крови становятся ритмичными и когда достигают пиков.
Секреторная линия печени работает по часам
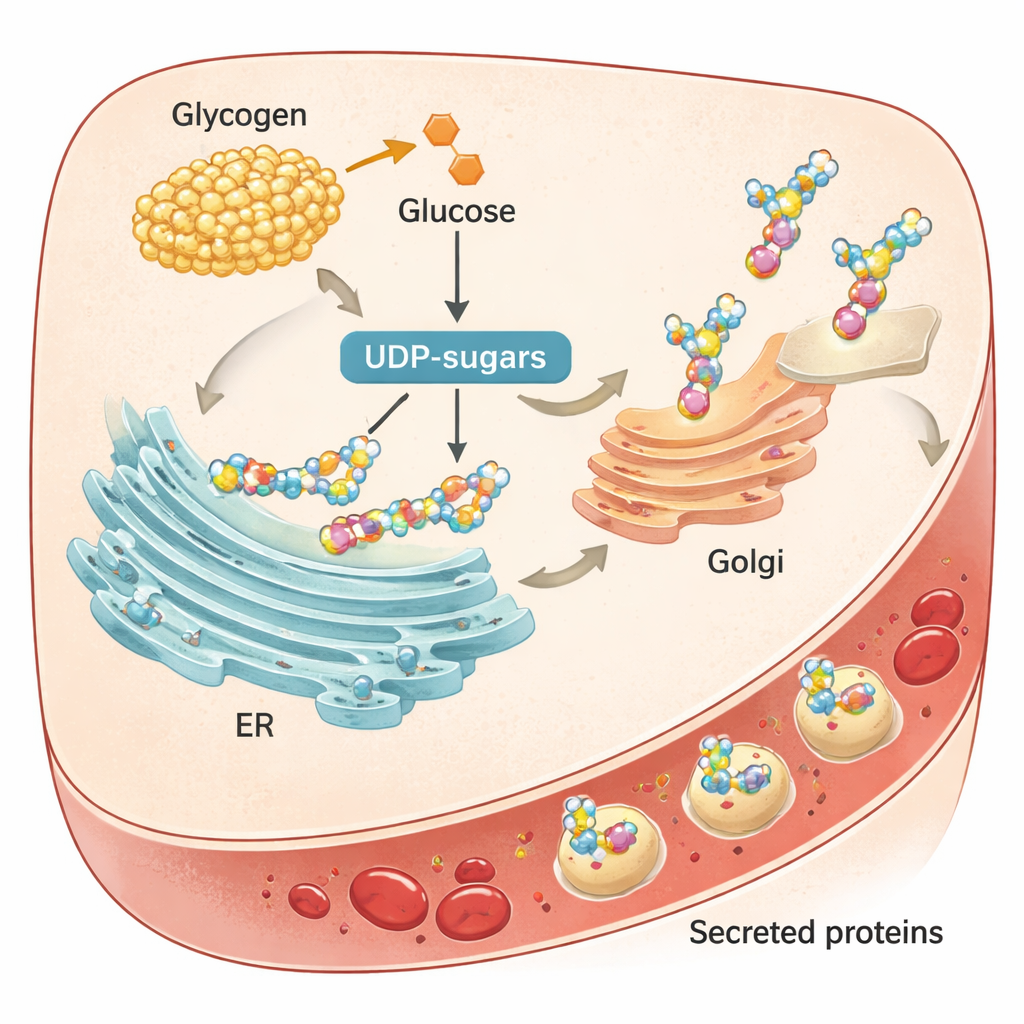
Чтобы выяснить, как возникают эти шаблоны, команда изучила внутреннее устройство печени. Они обнаружили, что белки, задействованные в классическом «секреторном пути» — когда вновь синтезированные белки попадают в эндоплазматический ретикулум (ЭР), модифицируются в аппарате Гольджи и затем выделяются — также изменяют уровни в течение дня. Вместо постоянной конвейерной ленты этот путь настроен по времени суток. Большинство ритмичных белков крови несло молекулярные «сигнальные пептиды», помечающие их для этого пути, а блокирование транспорта ЭР–Гольджи в срезах печеночной ткани мышей резко уменьшало выделение белков. Напротив, маркеры повреждения клеток и распада белков не показывали выраженных суточных колебаний, что указывает на то, что именно секреция, а не разрушение, в основном формирует наблюдаемые ритмы в крови.
Гликоген: запасенный сахар, питающий упаковку белков
Авторы затем связали эти временные эффекты с тем, как печень обращается с гликогеном, своим основным углеводным запасом. После еды печень накапливает гликоген; во время голодания она раскладывает его — процесс, называемый гликогенолизом. Продукты распада поступают в «UDP-сахара», активированные сахара, используемые для украшения белков сахарными цепями — модификацией, называемой гликозилированием. У мышей уровни UDP-сахаров сильно колебались в течение дня, синхронно с активностью ферментов, строящих и разрушающих гликоген. Когда команда блокировала ключевой печеночный фермент гликогенолиза PYGL с помощью препарата, гликоген накапливался, уровень сахара в крови снижался во время голодания, а запас UDP-сахаров падал. Это приводило к уменьшению гликозилирования печеночных белков, признакам стресса в ЭР и сниженной секреции нескольких важных белков в кровь.
Сигналы стресса и связи с болезнями
Нарушение распада гликогена повлекло за собой не только замедление экспорта белков; оно активировало систему контроля качества клетки. Клетки печени, обработанные препаратом, блокирующим PYGL, активировали ответ на неправильно свернувшиеся белки — набор путей ER-стресса, которые могут усиливать деградацию белков и избирательно менять профиль секретируемых белков. У тучных мышей, у которых естественно нарушена обработка гликогена, обычные суточные колебания гликогена были приглушены, и число ритмичных белков в крови уменьшилось. Аналогично происходило у нормальных мышей при временно-ограниченном питании, фактически снижавшем калории. Наконец, в большом генетическом исследовании людей носители вариантов в генах, связанных с болезнями накопления гликогена или врожденными нарушениями гликозилирования, имели измененные уровни многих белков в крови, что укрепляет связь между метаболизмом гликогена, гликозилированием белков и их секрецией.
Что это значит для повседневного здоровья
Для широкого читателя главная мысль такова: печень ведет хронологизированный экспорт белков в кровь, используя запасенный сахар как топливо, которое обеспечивает правильную упаковку и выпуск. Когда режимы питания, внутренние часы или гены, участвующие в переработке гликогена, нарушены, этот график дает сбои, меняя уровни гормонов, факторов свертывания и иммунных белков в кровотоке. Эти изменения могут объяснять, почему время приема пищи, ожирение и некоторые редкие метаболические состояния связаны с широким спектром проблем со здоровьем. Работа указывает на то, что важно не только что мы едим, но и когда мы едим, — и что врачам возможно стоит учитывать время суток и режим питания при интерпретации результатов анализов крови.
Цитирование: Weger, M., Mauvoisin, D., Hoyle, D. et al. Feeding-regulated glycogen metabolism drives rhythmic liver protein secretion. Nat Metab 8, 327–349 (2026). https://doi.org/10.1038/s42255-026-01453-8
Ключевые слова: циркадный ритм, печеночный гликоген, секреция белков, времена приема пищи, метаболизм