Clear Sky Science · ru
Регуляция распада цистеина ламинами A/C модулирует судьбу стволовых клеток через перепрограммирование эпигенома
Как каркас клетки общается с её метаболизмом
Почему одни клетки сохраняют юность и пластичность в выборе судьбы, тогда как другие стареют или закрепляют неправильную идентичность? Это исследование раскрывает неожиданное внутреннее «общение» в клетке между ядерным «каркасом», формирующим ДНК, и содержащим серу нутриентом — цистеином. Показав, как этот диалог направляет стволовые клетки к здоровым судьбам или к преждевременному старению, работа дает основание полагать, что то, что клетки «потребляют», и то, как они это перерабатывают, однажды можно будет настроить для предотвращения некоторых генетических заболеваний и, возможно, замедления отдельных аспектов старения.
Скрытая роль ядерной оболочки
Глубоко внутри каждой клетки ДНК прижимается к белковой сетке, называемой ядерной ламиной, в которой частично участвуют белки ламин A и C. Эти ламины не только придают ядру форму; они также помогают решать, какие гены заперты, а какие остаются доступными. Авторы изучали эмбриональные стволовые клетки мыши в их наиболее пластичном, «наивном» состоянии и обнаружили, что ламин A/C обычно сдерживает два метаболических фермента, CBS и CTH, участвующие в синтезе и расщеплении цистеина. При наличии и активности ламина A/C эти ферменты удерживаются в подчинении, и переработка цистеина остается на низком уровне, что поддерживает стабильное, юное состояние стволовых клеток. 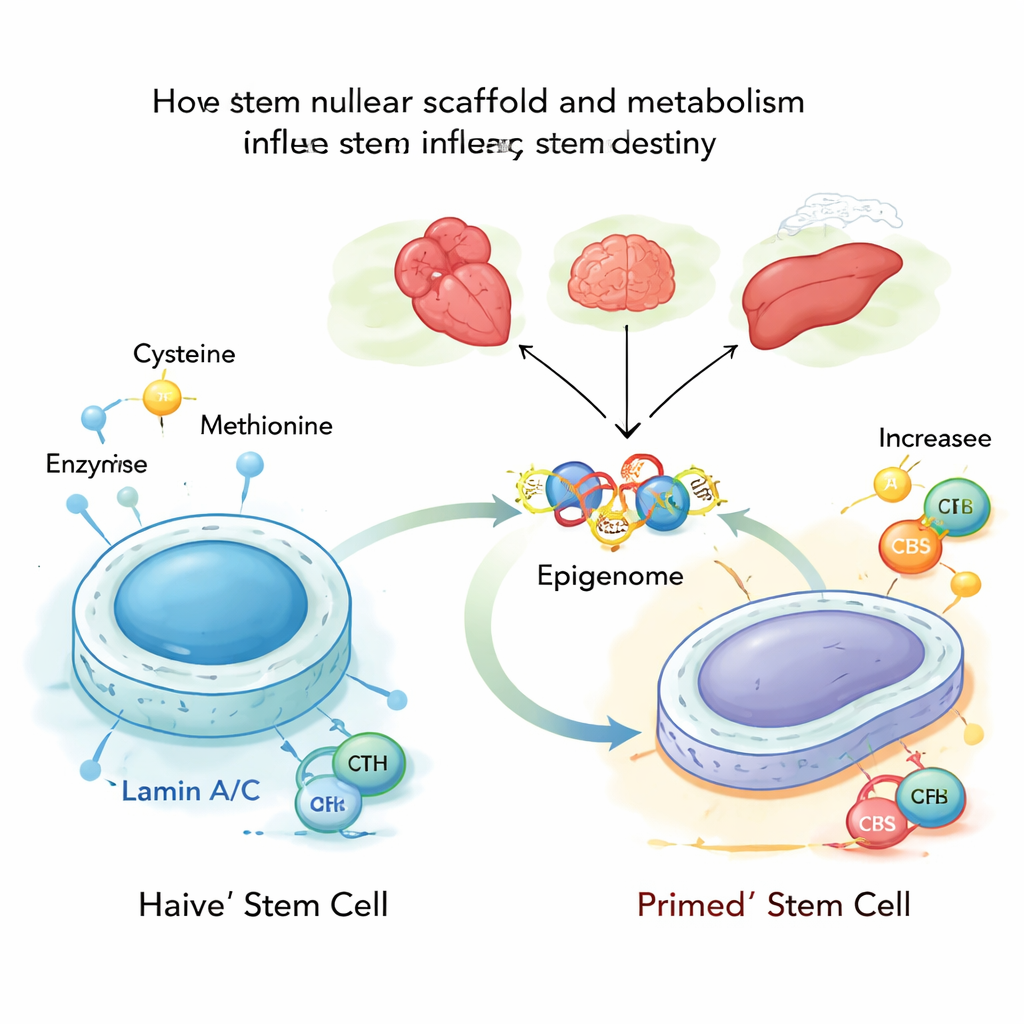
Когда структура дает сбой, метаболизм ускоряется
Далее исследователи удалили ламин A/C или ввели мутацию, связанную с болезнью, имитирующую человеческое заболевание преждевременного старения Хатчинсона–Гилфорда (прогерия). Без нормального ламина A/C гены CBS и CTH становятся более доступными и сильнее связываются с транскрипционным фактором SP1, что активирует их. Это смещает больший поток цистеина по метаболическому пути, заканчивающемуся образованием ацетил‑CoA — небольшой молекулы, переносчика ацетильных групп, которые ослабляют упаковку ДНК. По мере того как цистеин все активнее направляется в синтез ацетил‑CoA, ацетильные группы предпочтительно добавляются в определенные позиции на гистонах — особенно в две позиции гистона H3, известные как K9 и K27, — делая соседние гены более легко активируемыми.
От химических меток к решениям о судьбе клетки
Эти сдвиги в гистоновых «метках» действуют как глобальная перенастройка панели управления клетки. В наивных стволовых клетках усиление CBS и CTH или простое увеличение поступления цистеина продвигает клетки к более продвинутому, «подготовленному» состоянию, близкому к формированию реальных тканей. Гены, вовлеченные в развитие сердца и других линий, становятся более активными, и трехмерная укладка ДНК меняется в пользу этих программ. Наоборот, подавление CBS и CTH или ограничение цистеина способствует восстановлению более наивной, юной идентичности даже при повреждении ядерной ламины. В эмбриональных моделях такое метаболическое «перекручивание» приводило к искажённому формированию трёх зародышевых слоев — ранних строительных блоков всех органов — и ненормальной предрасположенности к образованию сердечной мышцы, если только уровни CBS и CTH не были восстановлены. 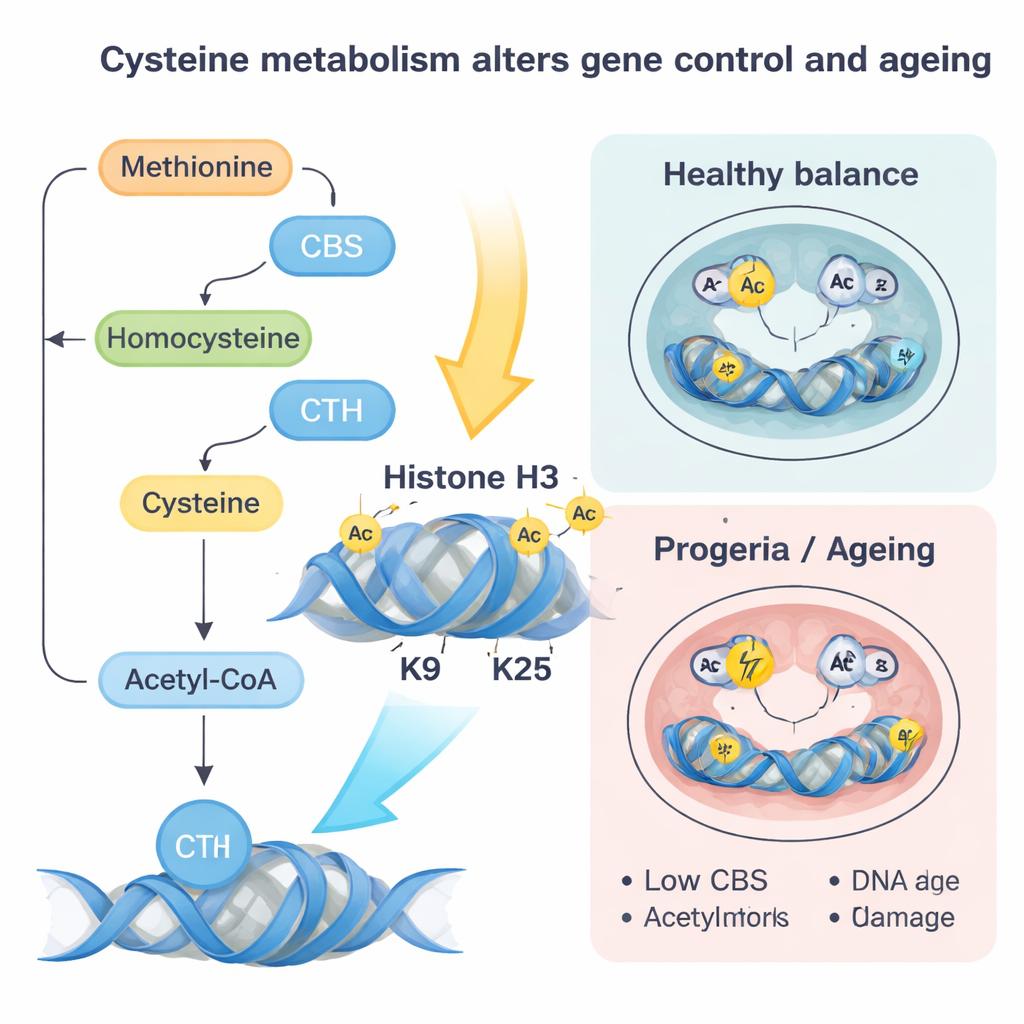
Метаболизм, метки ДНК и преждевременное старение
Мутация ламина, похожая на прогерию, рассказала дополняющую историю. Здесь уровни CBS и CTH падают, уменьшая поток цистеина и образование ацетил‑CoA по этому пути. Одновременно гомоцистеин перенаправляется обратно в метиониновый цикл, повышая уровни SAM — универсального донора метильных групп. Это способствует увеличению метильных меток, особенно отметки H3K9me3, устанавливаемой ферментом SUV39H1, которая уплотняет хроматин и связана с нарушением репарации ДНК. Авторы показали, что мягкое восстановление CBS или ограничение метионина снижало SAM, уменьшало эти репрессивные метильные метки, улучшало репарацию ДНК, снижало окислительный стресс и маркеры сенесценции, а также частично восстанавливало дифференцировку сердечных клеток. Похожие падения CBS и рост репрессивных меток наблюдались и в нормально постаревших сердцах мышей, и в фибробластах людей пожилого возраста и пациентов с прогерией, что указывает на то, что этот контур действует и при естественном старении.
Что это значит для здоровья и старения
Для неспециалиста суть в том, что структурная основа клетки и её метаболизм тесно связаны: когда ядерная оболочка из ламина A/C нарушается, меняется использование цистеина, а это в свою очередь переписывает химические метки на белках, упаковывающих ДНК. Эти метки решают, какие гены включаются по мере того, как стволовые клетки строят организм, и во многом определяют, насколько эффективно клетки восстанавливают повреждения в течение жизни. Тонкая настройка ферментов вроде CBS и CTH — или регулирование поставок таких нутриентов, как метионин и цистеин — может позволить исправлять некоторые искажения этих меток при ламин‑зависимых заболеваниях и, возможно, смягчать аспекты преждевременного или обычного старения.
Цитирование: Wang, Y., Shi, H., Wittig, J. et al. Lamin A/C-regulated cysteine catabolic flux modulates stem cell fate through epigenome reprogramming. Nat Metab 8, 431–453 (2026). https://doi.org/10.1038/s42255-025-01443-2
Ключевые слова: стволовые клетки, ядерная ламина, метаболизм цистеина, эпигенетика, старение