Clear Sky Science · ru
Реакция Дильса–Альдера даёт циркумпирен тетракарбоксидиимид с характером внутримолекулярного переноса заряда в возбужденном состоянии
Почему эта светящаяся молекула важна
Электроника на основе углеродных молекул обещает гибкие телефоны, светящиеся обои и ультратонкие солнечные панели. Чтобы приблизить это будущее, химикам нужны молекулы, которые эффективно проводят заряд и сильно взаимодействуют со светом, особенно в красной и ближней инфракрасной областях спектра. В этой работе сообщается о новом семействе таких молекул, получаемых путём увеличения небольшого фрагмента графена и его функционализации так, чтобы при освещении внутри молекулы в контролируемом направлении происходил перенос заряда.
Создание более крупного ядра для сбора света
Исследование сосредоточено на полициклических ароматических углеводородах — плоских, слитых кольцах «нанографенах», напоминающих маленькие чешуйки графена. Авторы начинают с высоколюминесцентного нанографена, называемого дибензо[hi,st]оваленом, который уже хорошо излучает свет. Их задача — как расширить эту углеродную рамку, так и присоединить специальные боковые группы, имиды, которые тянут на себя электроны. Окружив электронно‑богатое углеродное ядро электронно‑бедными имидами, они стремятся создать конфигурацию акцептор–донор–акцептор, которая естественно стимулирует сдвиг заряда по молекуле при возбуждении светом. 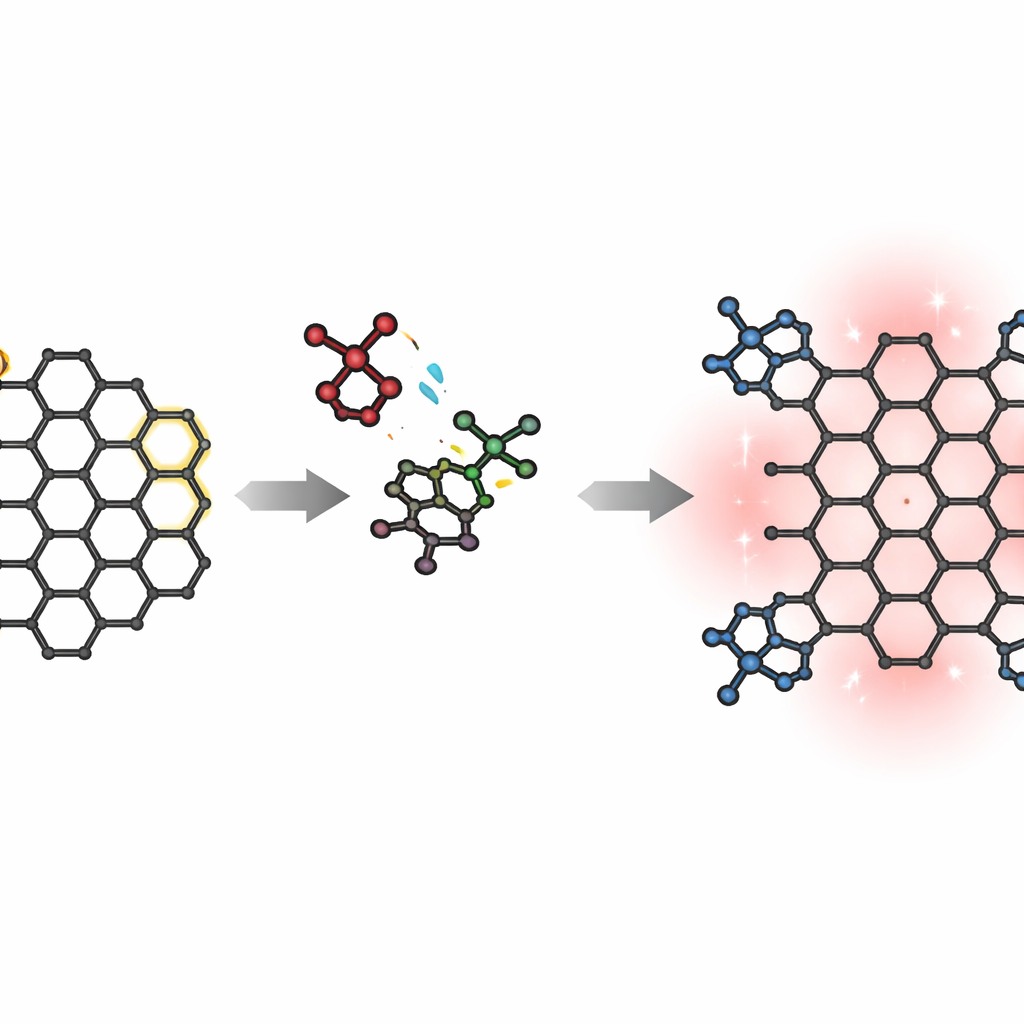
Встраивание новых колец
Чтобы переработать нанографен, исследователи применяют классический метод образования связей — реакцию Дильса–Альдера, которая способна припаивать новые кольца к уже существующим ароматическим системам. Они направляют эту реакцию на «заливные» области — выемки вдоль края исходного нанографена. Реагируя с малеимидными строительными блоками при высокой температуре, они получают два основных продукта: моноаддукт с одним новым кольцом и одним имида, и диаддукт, называемый циркумпирен тетракарбоксидиимидом, в котором обе заливные области расширены и установлены четыре имида. Хотя эта стратегия кажется прямолинейной, выходы полностью расширенного диаддукта невысоки, что указывает на тонкий путь реакции.
Выявление скрытого шага реакции
Чтобы понять, почему второй шаг образования кольца замедлен, авторы прибегают к квантово‑химическим расчётам. Эти симуляции показывают, что после первой аддукции Дильса–Альдера, когда система полностью «ареоматизируется» обратно в плоскую графеноподобную структуру, она становится удивительно инертной к второму присоединению. Вместо этого наиболее вероятный путь к диаддукту проходит через частично гидрогенизированный интермедиат, который только частично разглажен. У этого промежуточного соединения ниже барьер для присоединения второго малеимида. Расчёты таким образом объясняют экспериментальные наблюдения: если моноаддукт полностью релаксирует в свою наиболее стабильную ароматическую форму, он по сути перестаёт реагировать. Любая стратегия, которая стабилизирует частично ароматизированный интермедиат, должна улучшить образование желаемого полностью расширенного продукта.
Генерирование красного света и перенос заряда
Попав в руки исследователей, новый циркумпирен тетракарбоксидиимид демонстрирует выразительное оптическое поведение. По сравнению с ранними циркумпиренами без имида группы его поглощение и излучение смещены к более длинным длинам волн, в глубоко‑красную область, а флуоресценция становится заметно ярче. Электрохимические измерения и теоретические модели подтверждают, что имида‑группы понижают энергетические уровни молекулы, уменьшая разрыв между состояниями, которые поглощают и испускают свет. Детальная спектроскопия в разных растворителях выявляет широкие, красно‑смещённые полосы поглощения и испускания, усиливающиеся в более полярных жидкостях — классические признаки внутреннего состояния переноса заряда, когда возбуждение перемещает плотность электронов от центрального нанографенового ядра к имида‑«пробкам». 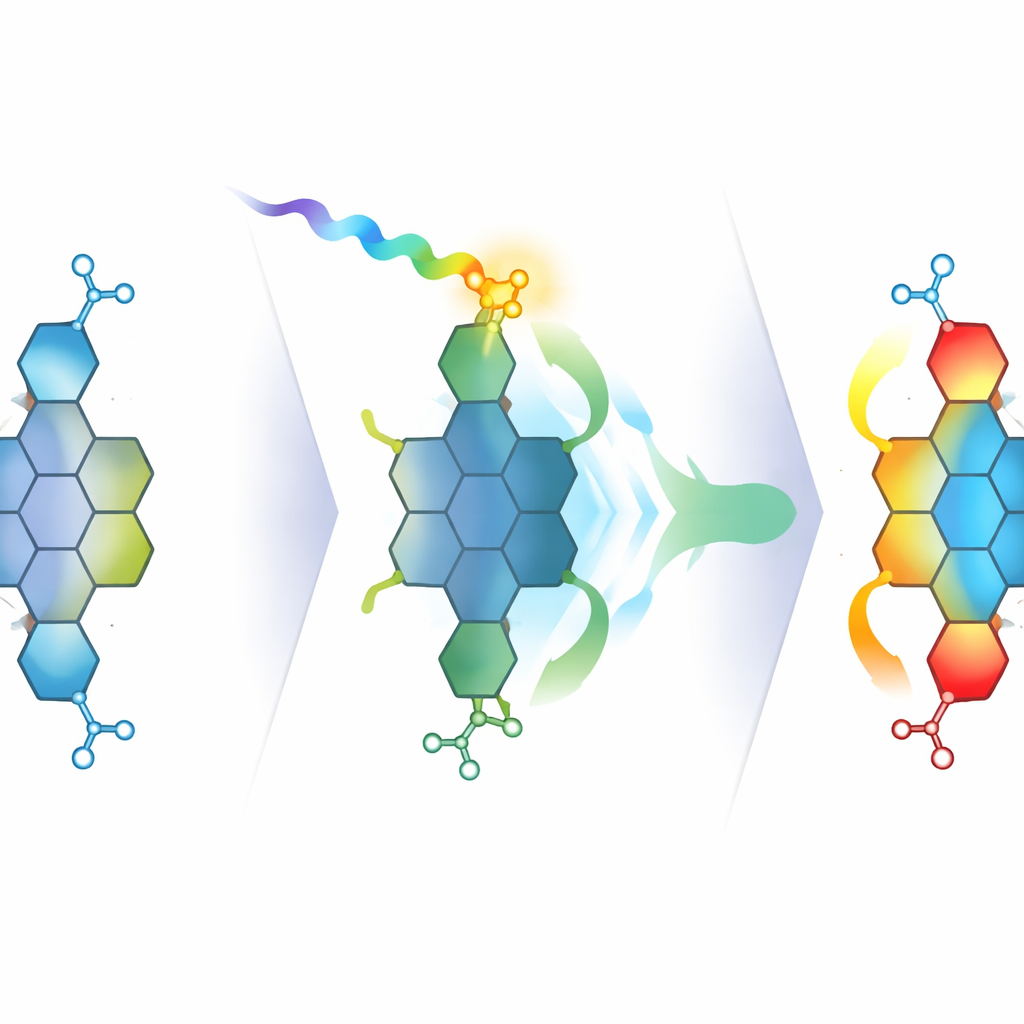
Наблюдение за сдвигом заряда в реальном времени
Чтобы визуализировать образование и эволюцию этого состояния переноса заряда, команда использует ультрабыструю транзиентную абсорбционную и двумерную электронную спектроскопию. Эти методы отслеживают на фемто‑ и пикосекундных временных масштабах, как появляются, превращаются и релаксируют возбужденные состояния молекулы после очень короткого светового импульса. При возбуждении основной полосы поглощения преимущественно населяется более локализованное возбужденное состояние на углеродном ядре. Но при возбуждении чуть дальше в красную область они напрямую получают яркое состояние переноса заряда, которое даёт свои собственные отличительные сигналы и сохраняется сотни пикосекунд. Двумерные карты подтверждают, что это состояние не просто тёмный побочный продукт, достигаемый в результате релаксации, а подлинный оптический переход, к которому можно обращаться напрямую светом.
От молекул‑дизайнеров к будущим устройствам
Проще говоря, исследователи разработали способ вырастить большую, аккуратно «проведённую» часть графена, которая ярко светится и внутри себя смещает заряд при освещении. Ключевой синтетический вывод — необходимо поймать частично релаксированный промежуточный продукт до того, как он полностью устаканится; ключевой физический вывод — что присоединённые имида‑группы создают встроенный путь для переноса заряда без потери яркости. Такие молекулы привлекательны как строительные блоки для органических солнечных элементов, оптических переключателей и биомаркеров, где важно эффективно превращать поглощённый свет либо в разделённые заряды, либо в яркое испускание в красной — ближне‑ИК — области.
Цитирование: Chen, Q., Guizzardi, M., Méndez, F. et al. Diels-Alder reaction affords circumpyrene tetracarboxydiimide with excited state intramolecular charge transfer character. Commun Chem 9, 122 (2026). https://doi.org/10.1038/s42004-026-01946-3
Ключевые слова: нанографен, Дильс–Альдера, перенос заряда, органическая оптоэлектроника, флуоресцентные красители