Clear Sky Science · ru
ABEL‑FRET заполняет временной разрыв в одномолекулярных измерениях структурной динамики аденозинового рецептора A2A
Наблюдая крошечные клеточные переключатели в реальном времени
Многие современные лекарства действуют, переворачивая молекулярные «переключатели» на поверхности клеток — так называемые рецепторы. Эти переключатели постоянно изменяют свою форму при включении и выключении сигналов, но большинство инструментов видят либо только самые быстрые, либо только самые медленные движения — не оба одновременно. В этой работе предложен метод, позволяющий наблюдать единичный рецептор‑мишень в растворе значительно дольше, чем раньше, раскрывая, как он задерживается в определённых формах, важных для действия препаратов.
Почему эти изменяющиеся формы белков важны
Исследование сосредоточено на крупном классе мембранных белков — G‑белок‑связанных рецепторах (GPCR). Эти белки контролируют жизненно важные процессы, включая зрение, настроение, артериальное давление и иммунные реакции; более трети одобренных лекарств на них действуют. Хорошо изученный представитель, аденозиновый рецептор A2A, участвует в регуляции сна, боли, воспаления и мозговой сигнализации и является перспективной мишенью при лечении таких заболеваний, как болезнь Паркинсона и рак. GPCR крайне подвижны: при связывании различных молекул рецептор сдвигается в разные формы, отдавая предпочтение тем или иным сигнальным путям. Именно эта гибкость затрудняет разработку лекарств на основе статических снимков, полученных методом рентгеновской кристаллографии или криоэлектронной микроскопии.
Следить за одним рецептором, не закрепляя его
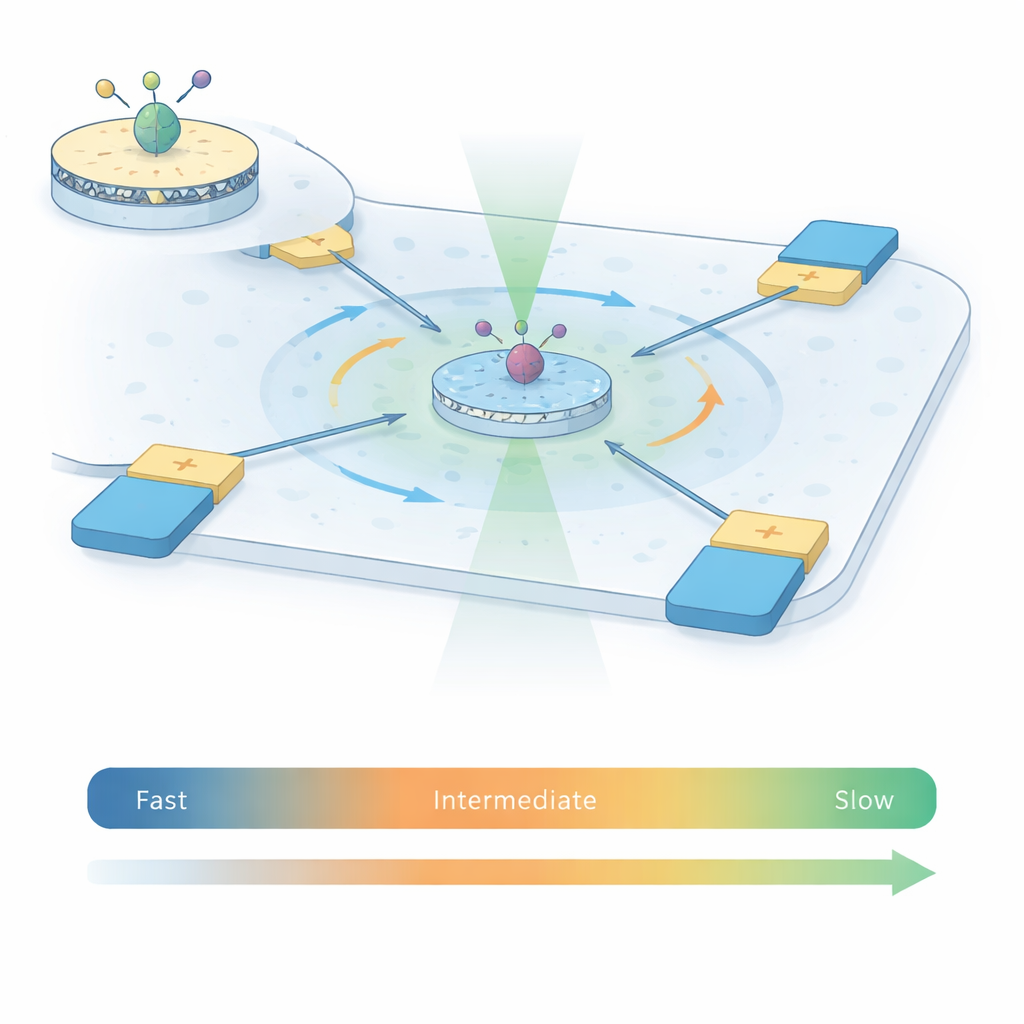
Чтобы зафиксировать движения рецептора A2A, авторы объединяют два мощных подхода в метод, названный ABEL‑FRET. Сначала они реконситуируют одиночные рецепторы в крошечные фрагменты искусственной мембраны — нанодиски — что обеспечивает белку более естественную среду, чем детергенты. На две подвижные части внутренней стороны рецептора прикрепляют пару флуоресцентных красителей. По мере изменения формы рецептора расстояние и взаимная ориентация между красителями меняются, что изменяет энергообмен между ними — явление, известное как резонансный перенос энергии Форстера (FRET). Во‑вторых, вместо прикрепления рецептора к поверхности используют анти‑брауновскую электрокинетическую (ABEL) ловушку: микрофлюидную камеру с электродами, которые фиксируют положение флуоресцирующей частицы и плавно возвращают её в центр, компенсируя случайное броуновское движение.
Заполнение отсутствующего временного окна
Традиционные одномолекулярные эксперименты FRET либо наблюдают свободно диффундирующие рецепторы в течение лишь нескольких тысячных долей секунды, либо фиксированные на поверхности рецепторы в течение секунд или минут — каждый подход охватывает своё временное окно. С помощью ловушки ABEL в этой работе отдельные рецепторы A2A держат в поле зрения от одной до двух секунд при том, что они остаются свободными в растворе — примерно в 100 раз дольше, чем в экспериментах, ограниченных диффузией. Это увеличенное время наблюдения позволяет команде измерять флуктуации FRET‑сигнала внутри каждой захваченной вспышки и по тысячам молекул в четырёх условиях: без лиганда, с антагонистом и с двумя различными активирующими молекулами (агонистами). Статистические инструменты из анализа сигналов — дисперсия, корреляция и анализ повторений — помогают отделить случайный фотонный шум от подлинных, медленных структурных изменений рецептора.
Обнаружены скрытые долгоживущие состояния
Считывания FRET показывают, что рецепторы занимают несколько различных конформаций, которые не полностью преобразуются друг в друга в типичные времена наблюдения — несколько сотен миллисекунд. Во всех условиях распределение значений FRET существенно шире, чем можно объяснить только шумом, что указывает на структурную гетерогенность: разные молекулы находятся в разных долгоживущих формах. При связывании активирующих молекул средний уровень FRET смещается вверх, что указывает на то, что рецептор проводит больше времени в «активоподобной» компоновке внутренних спиралей. Тем не менее корреляционный анализ показывает, что оказавшись в высоком или среднем FRET‑состоянии, рецептор с большой вероятностью остаётся в нём по крайней мере сотни миллисекунд. Эти результаты обновляют прежние оценки, основанные на более быстрых экспериментах, увеличивая характерные «времяпребывания» в долгоживущих состояниях с нескольких миллисекунд до более чем одной десятой секунды.
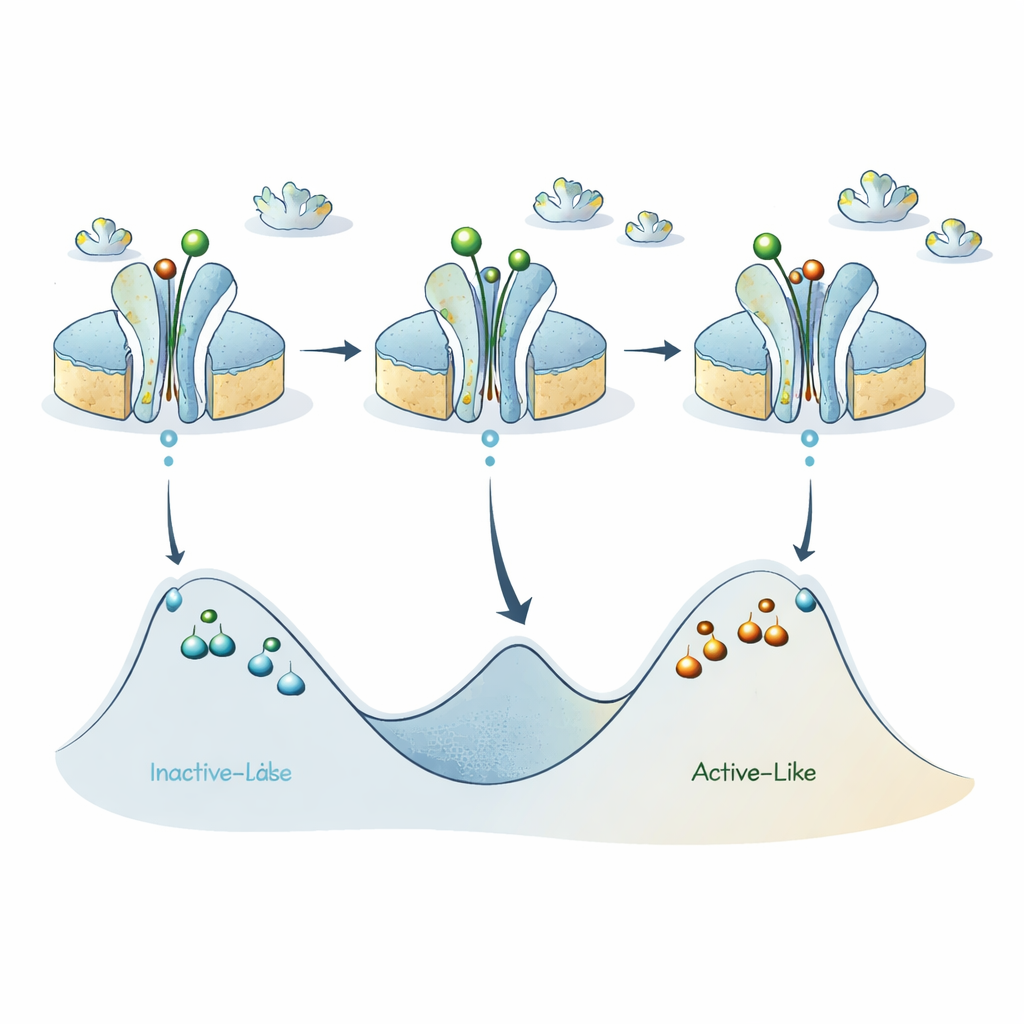
Новая карта энергетического ландшафта рецептора
Собрав эти данные вместе, авторы уточняют предыдущую модель, в которой рецептор A2A переключается в основном между неактивоподобным и активоподобным состояниями. Новые данные указывают, что каждую из этих двух широких категорий на самом деле составляют несколько под‑состояний, разделённых значительными энергетическими барьерами, так что отдельные рецепторы могут «застревать» в конкретной версии активоподобного или неактивоподобного состояния удивительно долго. Активирующие лиганды понижают барьер между основными неактивной и активной «впадинами», способствуя быстрому переключению на субмиллисекундном масштабе, но внутренние барьеры внутри каждой впадины остаются высокими, порождая долгоживущие под‑состояния, которые обнаруживает ABEL‑FRET.
Что это значит для будущих лекарств
Для неспециалистов ключевая мысль такова: мишень, такая как рецептор A2A, не просто переключается между «выключено» и «включено». Вместо этого она исследует изрезанный ландшафт форм, некоторые из которых сохраняются достаточно долго, чтобы влиять на передачу сигналов внутри клетки и на действие лекарств во времени. Расширяя время, в течение которого отдельные рецепторы можно наблюдать в их естественном, несвязанном состоянии, ABEL‑FRET заполняет важный разрыв между ультрабыстрыми и очень медленными измерениями. Этот подход теперь может быть применён к множеству мембранных белков, предоставляя более полную, разрешённую по времени картину того, как потенциальные лекарственные мишени «дышат», меняют форму и реагируют на терапевтические соединения.
Цитирование: Maslov, I., Borshchevskiy, V., Pérez, I. et al. ABEL-FRET bridges the timescale gap in single-molecule measurements of the structural dynamics in the A2A adenosine receptor. Commun Chem 9, 114 (2026). https://doi.org/10.1038/s42004-026-01941-8
Ключевые слова: G‑белок‑связанные рецепторы, одномолекулярный FRET, аденозиновый рецептор A2A, конформационная динамика белков, ловушка ABEL