Clear Sky Science · ru
Механистическое исследование миграции сульфатов в гликозаминогликанах во время фрагментации МS
Почему сдвиг химических меток на сахарах имеет значение
Клетки покрыты длинными цепочками сахарных остатков, которые регулируют такие разные процессы, как свертывание крови, иммунная защита и прикрепление вирусов к клеткам. Многие из этих цепочек несут крошечные химические метки — сульфатные группы, — чьи точные положения вдоль сахарного каркаса действуют как молекулярный штрих‑код, указывая белкам, когда и где связываться. Ученые во многом полагаются на масс‑спектрометрию, мощный метод взвешивания, чтобы «прочитать» эти штрих‑коды. В этом исследовании показано, что во время таких измерений сульфатные метки могут тихо перемещаться, что потенциально вводит в заблуждение при определении истинной структуры этих биологически важных сахаров.
Сложные сахарные цепочки с критичными метками
Гликозаминогликаны — это длинные линейные сахарные цепочки, часто присоединённые к белкам на поверхности клеток. Их сульфатные украшения не случайны; небольшие изменения в положении сульфатной группы на конкретном сахарном звене могут радикально изменить взаимодействия цепочки с факторами роста, белками свёртывания или патогенами. Поэтому учёные стремятся выяснить не только, сколько сульфатов присутствует, но и где именно они расположены. Масс‑спектрометрия, часто в сочетании с контролируемым разрушением сахарных цепочек, является одним из основных методов для этого. Однако ранее появились указания на то, что заряженные группы, такие как сульфаты, могут перемещаться во время измерения, что усложняет чтение истинного паттерна модификаций.
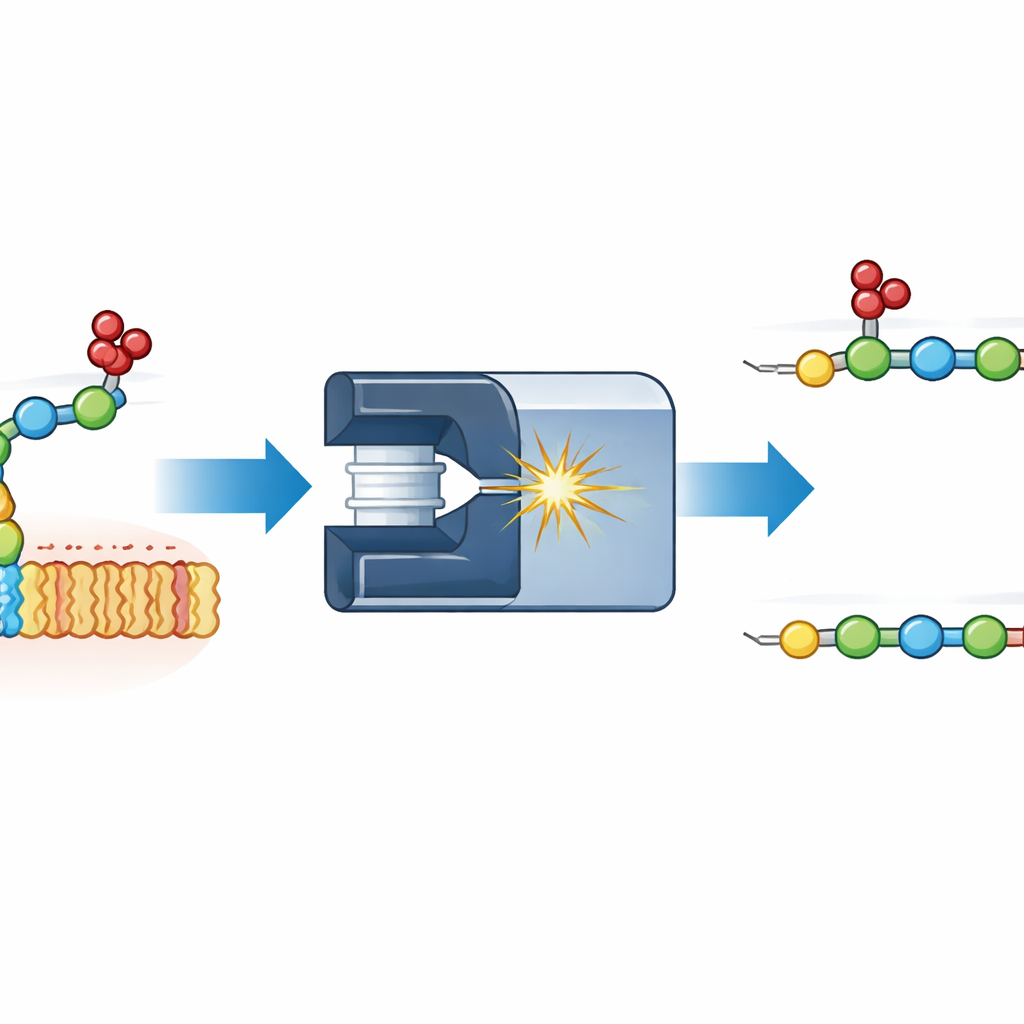
Наблюдение миграции сульфатов во время измерения
Авторы сосредоточились на простой модели: дисахариде гепарансульфата, одном из наиболее известных гликозаминогликанов. Они прикрепили разные флуоресцентные метки к одному концу дисахарида и фрагментировали его внутри масс‑спектрометра. Измеряя, как образующиеся фрагменты дрейфуют через газ под действием электрического поля — метод, известный как иономобильность — они смогли различить формы, которые иначе имели бы одинаковую массу. Появился неожиданный фрагмент, тяжелее ровно на одну сульфатную группу, но находящуюся не в том месте: вместо того чтобы оставаться на первом сахаре, сульфат мигрировал на второй. Сравнения с тщательно синтезированными эталонными соединениями показали, что мигрирующая сульфатная группа может осесть в двух разных положениях на втором сахаре, давая две различные формы, чётко разрешаемые методом иономобильности.
Точное определение новых мест посадки и проверка меток
Чтобы лучше понять, где именно оказался сульфат и возможны ли другие положения, команда сочетала измерения с подробными компьютерными моделями. Они рассчитали множество возможных трёхмерных конформаций для кандидатных структур и предсказали, как каждая должна перемещаться в газовой фазе. Только сульфаты, расположенные в двух конкретных положениях на втором сахаре — известные специалистам как позиции 6O и 3O — соответствовали экспериментальному поведению, тогда как другие гипотетические локализации выглядели маловероятными. Исследователи затем проверили, не вызывают ли сами приклеенные метки реструктуризации, заменив исходную метку тремя более простыми. В каждом случае миграция сульфата сохранялась и давала сходные типы фрагментов, что указывает на то, что выбор метки мало влияет на сам факт миграции, хотя может тонко менять, насколько легко различимы различные продукты.
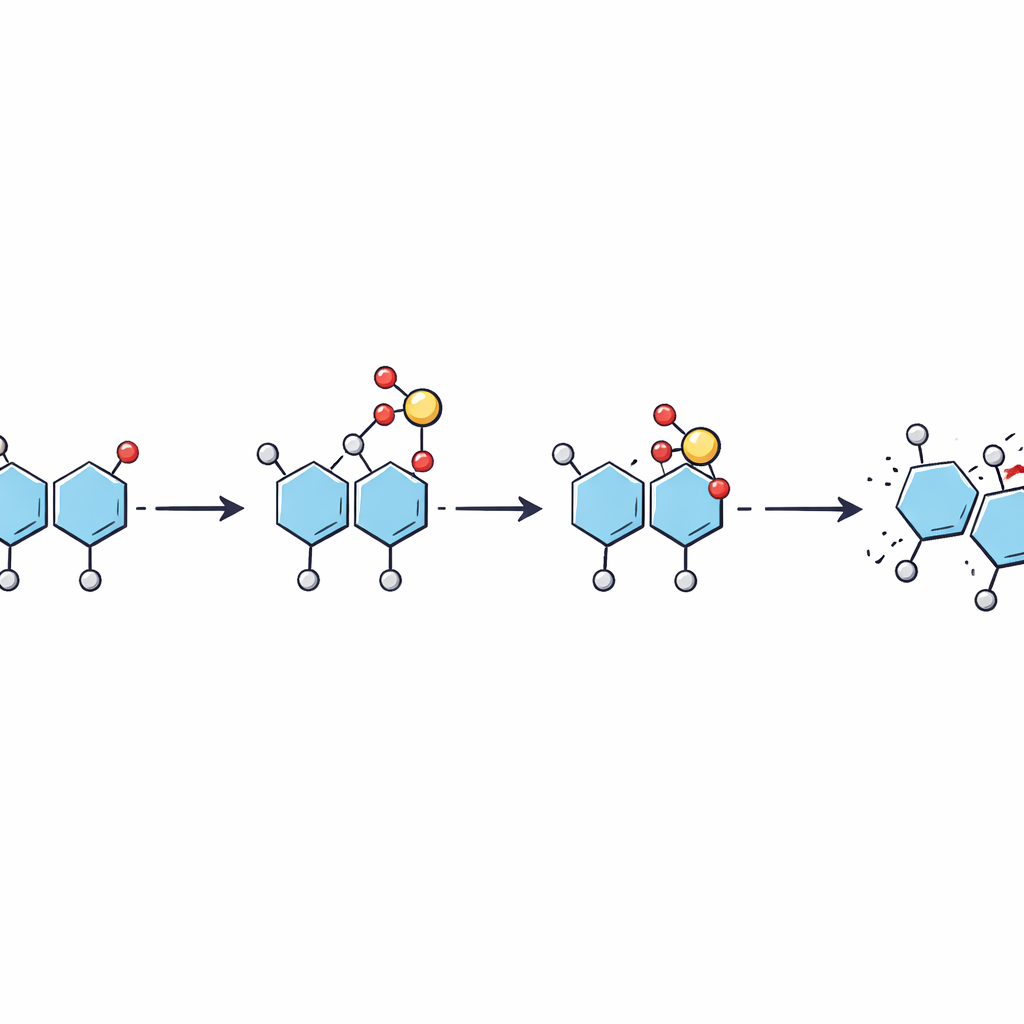
Пошаговое перескакивание вместо одного прыжка
Сочетая эксперименты с фрагментацией при настроенной энергии и дополнительные моделирования, авторы восстановили пошаговую картину того, как сульфат перемещается. По мере того как ион получает энергию в масс‑спектрометре, подвижный протон сначала активирует сульфатную группу, которая затем перескакивает с исходного сахара на определённое место на соседнем звене по мере разрыва связи между ними. Это даёт фрагмент, в котором сульфат находится в промежуточном положении. При дополнительной энергии сульфат может сместиться вновь вдоль того же сахара в более стабильное положение. Работа показывает, что эти перестановки могут происходить при более низких энергиях, чем те, которые требуются для разрыва сахарного каркаса, то есть они могут происходить незаметно во время рутинных анализов.
Что это означает для расшифровки структуры сахаров
Для неспециалистов ключевое сообщение таково: химические метки на важных биологических сахарах не всегда остаются фиксированными во время анализа; они могут соскальзывать по цепочке, пока молекула летит через масс‑спектрометр. Исследование подробно показывает, что по крайней мере для типичного фрагмента гепарансульфата сульфатная группа может мигрировать от одного сахарного звена к другому и затем осесть в новых положениях, создавая вводящие в заблуждение фрагменты, имитирующие подлинные структурные особенности. Это означает, что некоторые прошлые и будущие измерения могут неправильно интерпретировать «сульфатный код», если не применять дополнительные методы, такие как иономобильность и продвинутое моделирование, чтобы зафиксировать эти скрытые перемещения. Работа требует более систематических исследований, чтобы выяснить, насколько широко распространена такая миграция сульфатов, чтобы учёные могли надёжнее связывать паттерны сахаров на поверхности клеток со здоровьем и болезнями.
Цитирование: Polewski, L., Yaman, M., Tokić, M. et al. Mechanistic study on the sulfate migration in glycosaminoglycans during MS fragmentation. Commun Chem 9, 130 (2026). https://doi.org/10.1038/s42004-026-01939-2
Ключевые слова: гепаран сульфат, гликозаминогликаны, масс-спектрометрия, миграция сульфата, иономобильность