Clear Sky Science · ru
Глубина позы в связывании модулирует эффективность фотопереключаемых лигандов на рецепторе 5-HT2A
Освещая переключаемые препараты для мозга
Представьте лекарство, которое можно включать и выключать одним вспышкой света, точно направляя активность рецепторов мозга и при этом избегая побочных эффектов. Это исследование как раз изучает такую идею для ключевого серотонинового рецептора, связанного с настроением, восприятием и психоделическими препаратами. Авторы разобрались, почему два почти идентичных светочувствительных молекул ведут себя так по-разному — один действует почти как идеальный выключатель, а другой упорно не хочет полностью выключаться. Их ответ сводится к неожиданно простому фактору: как глубоко молекула садится внутри рецептора.
Препараты, управляемые светом, в мозге
Светоактивируемые препараты, или фотофармакологические инструменты, сконструированы так, чтобы луч света переворачивал часть молекулы между двумя формами, как согнутой и прямой. Эти формы меняют силу, с которой препарат удерживает свою мишень. В этой работе мишенью является человеческий рецептор 5-HT2A — белок на поверхности нейронов, реагирующий на серотонин и играющий центральную роль как в антипсихотических, так и в психоделических эффектах. Изученные молекулы представляют собой производные N,N-диметилтриптамина (DMT), модифицированные фото-чувствительной азобензольной группой. Две версии различаются лишь положением крошечной метокси-группы на кольце — либо в пара-, либо в мета-положении — но их биологическое поведение под светом драматически отличается.
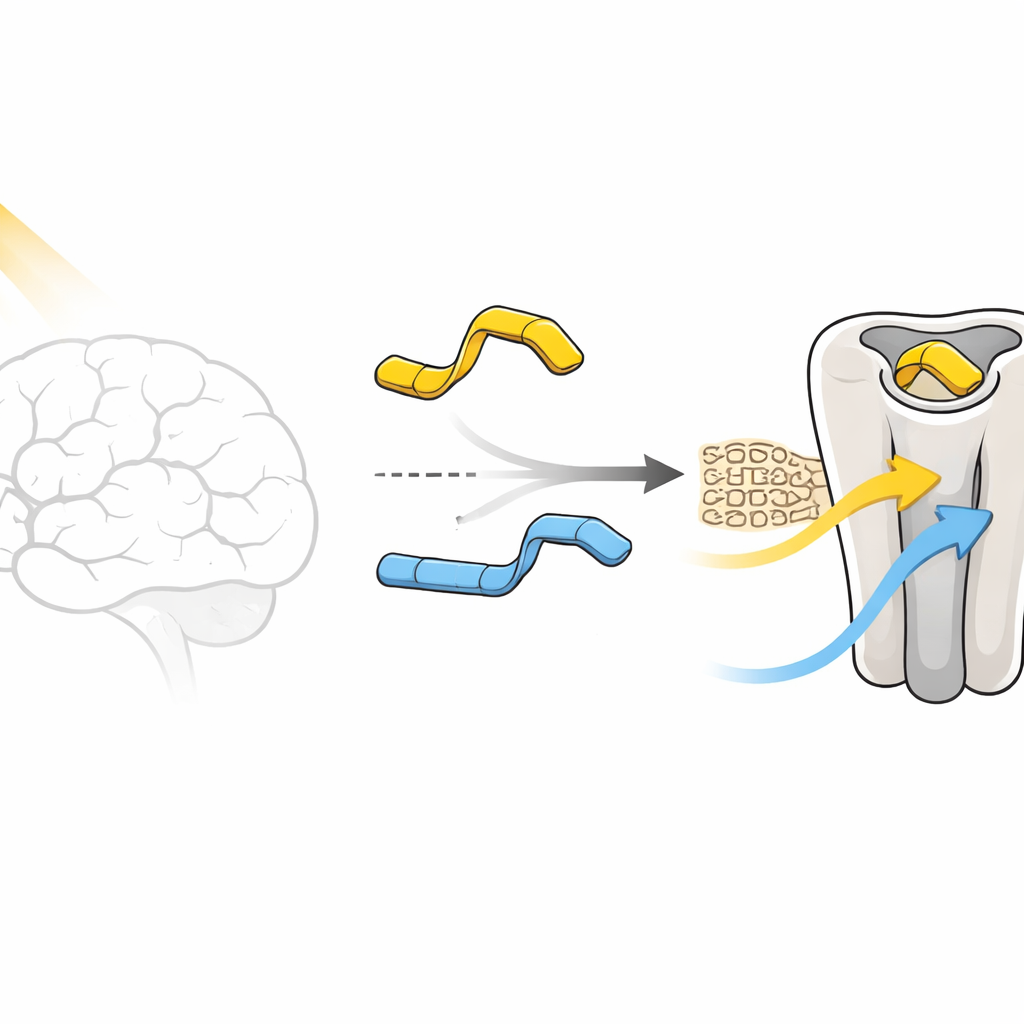
Два почти близнеца-молекулы, очень разные переключатели
В клеточных тестах пара-версия, названная соединением 1, ведет себя почти как цифровой переключатель. В темноте её «транс»-форма едва активирует рецептор и даже слегка блокирует его, действуя как слабый антагонист. Когда свет переводит её в «цис»-форму, та же молекула становится умеренным активатором, частично включая рецептор. Мета-версия, соединение 2, не желает сотрудничать таким образом: и в светлом, и в темном состояниях оно поддерживает рецептор в сравнительно активном состоянии, никогда не давая настоящего «выключения». Центральная головоломка этой работы — почему такое минимальное химическое изменение — всего лишь смещение одной малой группы на кольце — так сильно меняет ответ рецептора.
Заглядывая внутрь с атомным разрешением
Чтобы решить эту проблему, команда использовала обширные молекулярно-динамические симуляции с атомным разрешением, фактически проигрывая подробные «фильмы» для каждого атома рецептора, окружающей мембраны, воды и каждого лиганда в сумме около 80 микросекунд. Они моделировали обе молекулы в каждой их светоуправляемой форме и в обоих состояниях рецептора 5-HT2A — неактивном и активном. Отслеживая известные структурные «микропереключатели» внутри белка — такие как ключевой триптофан, который переворачивается, сольевой мост, который разрывается, и движение натрия и воды в глубине ядра — они могли сказать, склоняется ли рецептор к выключенному или включенному состоянию. Они также сравнивали, насколько новые молекулы имитируют позу связывания ЛСД, хорошо изученного частичного активатора, используя перекрытие их кольцевых систем как ориентир.
Глубина важнее формы одна
Ключевой вывод в том, что эффективность молекул определяется главным образом тем, как глубоко они внедряются в карман связывания рецептора. В неактивном рецепторе транс-форма пара-соединения формирует особый набор водородных связей, который втягивает его необычно глубоко, ниже той области, где обычно находятся активирующие контакты. Это «чрезмерное внедрение» мешает ему касаться ключевых полярных остатков, помогающих переключить рецептор в активное состояние, поэтому оно стабилизирует выключенное состояние. Транс-форма мета-соединения не может образовать тех же анкерных контактов и вместо этого располагается выше в более ЛСД-подобной позе, совместимой с активацией, что объясняет его остаточную активность. Когда свет переводит обе молекулы в цис-формы, они, как правило, смещаются в более мелкие, более активатороподобные положения. Однако и здесь геометрия имеет значение: в активном рецепторе цис-соединение 2 может соскользнуть глубже в гидрофобный туннель между двумя спиралями и образовать устойчивую водородную связь, усиливающую его сильную агонистическую активность, тогда как цис-соединение 1 стерически блокировано и не может этого сделать.
Тонкая регулировка внутренней воды и ионов
Симуляции также показывают, что глубина связывания тонко настраивает внутренний натриевый карман и водный путь, которые известны влияющими на активацию рецептора. Глубокое, жёсткое связывание пара-соединения в его транс-форме удерживает ион натрия плотно «в клетке» и делает окружающую область относительно сухой — признаки, связанные с выключенным состоянием. В отличие от этого, более подвижное связывание мета-соединения или цис-форм допускает больше проникновения воды и ослабляет окружение натрия, подготавливая рецептор к активации. Ключевой ароматический «переключатель» может менять ориентацию легче, когда лиганды гибки и не слишком заякорены, дополнительно подталкивая рецептор в сторону включённого состояния, особенно в случае цис-соединения 2.
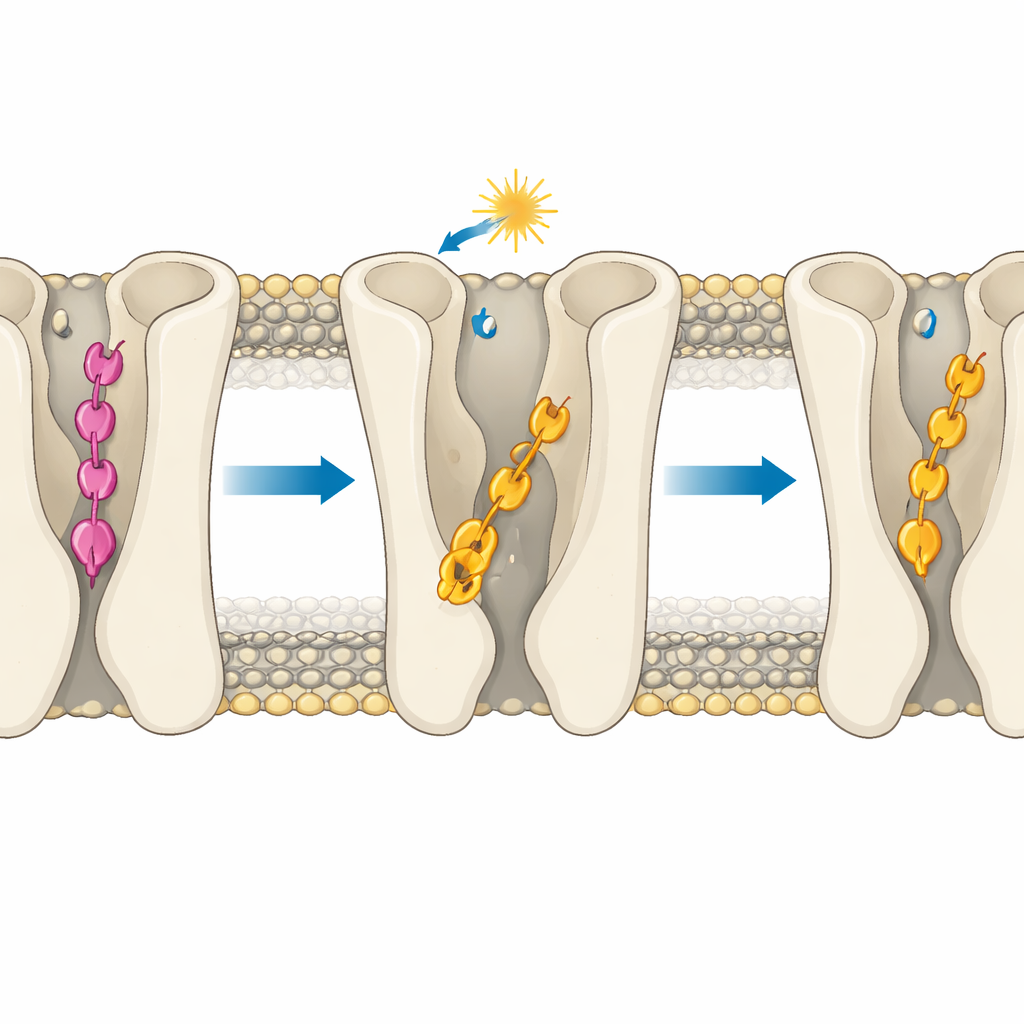
Правила проектирования для будущих препаратов, управляемых светом
Для неспециалиста сообщение таково: точная глубина, на которой препарат располагается в кармане рецептора, может определять разницу между выключенным, частично включённым и сильно включённым состояниями — даже когда химическое изменение выглядит крошечным. Показывая, как один фотопереключаемый лиганд может чрезмерно внедриться и зафиксировать рецептор в выключенном состоянии, тогда как близкий аналог остается на глубине, благоприятной для активации, исследование предлагает ясное правило проектирования: контролируйте глубину внедрения с такой же тщательностью, с какой контролируете свет-индуцированные изменения формы. Эти наблюдения могут направить создание следующего поколения светочувствительных соединений для лечения заболеваний мозга с беспрецедентной точностью, позволяя управлять сигналами вверх или вниз контролируемым, обратимым способом и минимизируя побочные эффекты.
Цитирование: Weber, V., Salvadori, G., Natale, F. et al. Binding pose depth modulates photoswitchable ligands’ efficacy at the 5-HT2A receptor. Commun Chem 9, 121 (2026). https://doi.org/10.1038/s42004-026-01936-5
Ключевые слова: фотофармакология, серотониновый рецептор 5-HT2A, фотопереключаемые лиганды, активация GPCR, молекулярно-динамические симуляции