Clear Sky Science · ru
Кристаллизация, вызванная массовой диффузией при более низком локальном пересыщении
Почему это важно за пределами лаборатории
Кристаллы соли кажутся обыденными, но способ их образования имеет серьёзные последствия — от производства лекарств до извлечения ресурсов из солёных сточных вод. В этом исследовании показано, что кристаллы могут начинать образовываться раньше и в других местах, когда жидкость мягко выводят из равновесия градиентами температуры и концентрации. Понимание такого тонкого поведения может помочь разработать более чистые и дешёвые методы управления рассолами, создавать лучшие материалы и контролировать нежелательное отложение на трубах и оборудовании.

Как обычно появляются кристаллы
Кристаллизация происходит, когда растворённое вещество, например хлорид калия (KCl) в воде, превышает количество, которое может оставаться растворённым. Такое состояние называется пересыщением. Классические теории утверждают, что кристаллы возникают только тогда, когда пересыщение достаточно велико, чтобы преодолеть энергетический барьер, и что нуклеация должна начинаться там, где раствор наиболее пересыщен. В промышленности обычно доводят растворы до этого состояния путём охлаждения, выпаривания растворителя или добавления «антирастворителя». При этих привычных, почти однородных условиях исследователи выделили метастабильную зону — окно, в котором жидкость пересыщена, но видимых кристаллов ещё нет.
Три разных способа заставить ту же соль кристаллизоваться
Авторы изучали появление кристаллов KCl в трёх тщательно контролируемых сценариях внутри специально сконструированной плоской ячейки с раздельным термоконтролем сверху и снизу. Сначала они провели стандартные эксперименты по охлаждению, равномерно понижая температуру от 20 °C и наблюдая, когда появятся первые кристаллы. Это установило эталонную границу на карте концентрация–температура: ниже определённой температуры кристаллы всегда формировались; выше неё раствор оставался свободным от кристаллов в течение часов. Затем этот эталон сравнили с двумя более сложными ситуациями, при которых в растворе происходил направленный массообмен, а не простое однородное охлаждение.
Когда тепло приводит соль в движение
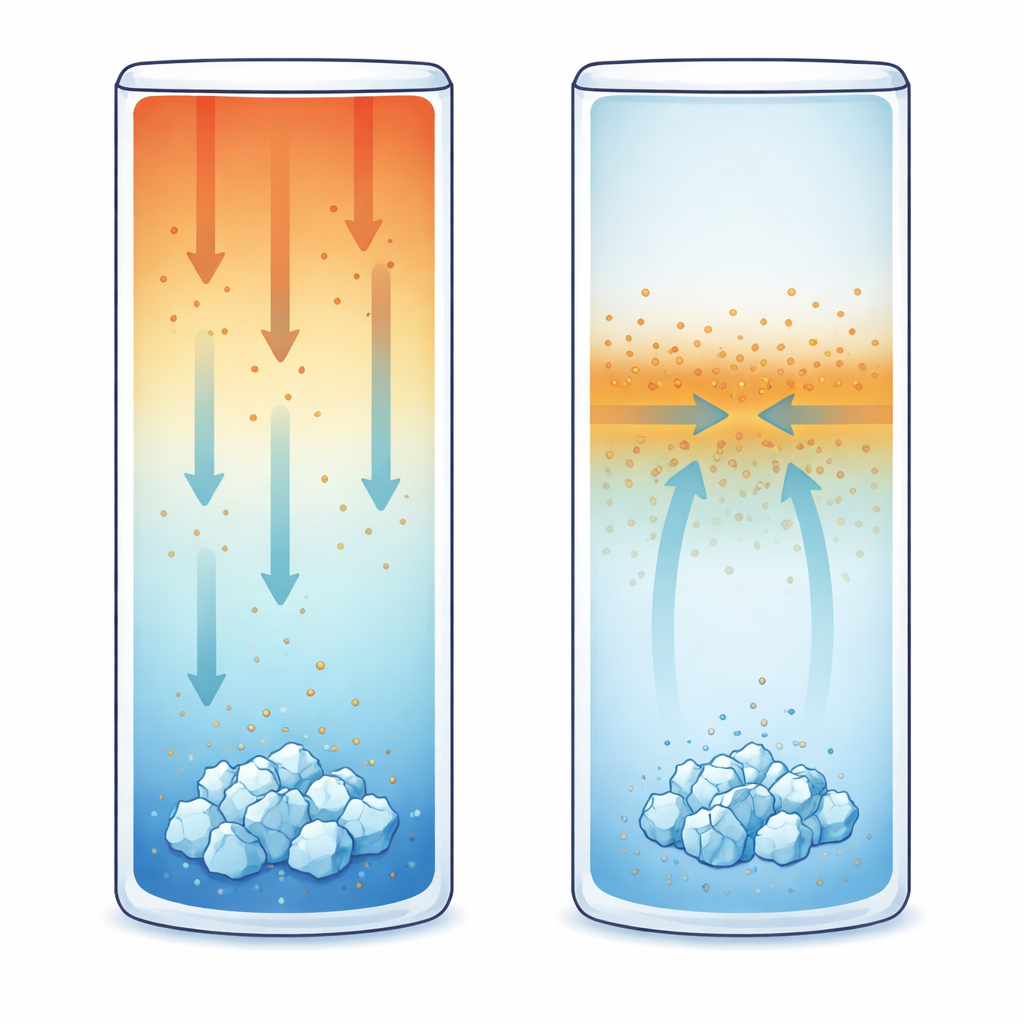
Во втором наборе экспериментов начальный состав раствора был тем же, но верхняя часть удерживалась при 20 °C, а нижняя — охлаждалась до 15 °C. Этот вертикальный температурный градиент вызывает термодиффузию, то есть растворённые ионы дрейфуют в ответ на температуру, а не только на концентрацию. Для KCl в исследованном диапазоне поведение термофобное: ионы стремятся перемещаться в более холодную область, накапливая соль у нижней стенки. С помощью чувствительного оптического метода — фазосдвиговой интерферометрии — исследователи отслеживали крошечные изменения показателя преломления, которые показывают, как меняются концентрация и температура. Оказалось, что кристаллы последовательно образовывались у холодной нижней стенки в областях с самым резким градиентом концентрации — при этом локальное пересыщение там было немного ниже, чем в случае равномерного охлаждения. Иными словами, наличие устойчивого массового потока позволяло кристаллизации начаться раньше, чем ожидалось.
Когда соль диффундирует при идеально ровной температуре
В третьем сценарии температурные различия были полностью устранены. Вся ячейка поддерживалась при одинаковой 17 °C и первоначально была заполнена эталонным раствором. Затем из одного верхнего угла аккуратно ввели меньший объём более разбавленного раствора KCl, создавая резкий контраст концентраций, но почти без перемешивания. Затем диффузия сгладила этот контраст по мере того, как ионы мигрировали из более концентрированной области в разбавленную. Интерферометрия вновь показала, как со временем эволюционирует поле концентрации. Удивительно, но первые видимые кристаллы появились не там, где раствор был наиболее пересыщен. Вместо этого они формировались примерно на полпути вверх по ячейке, у интерфейса, где градиент концентрации — а значит и диффузионный массовый поток — был наибольшим.
Что это означает для теории и техники
Во всех трёх методах — охлаждение, термодиффузия и изотермическая диффузия — первые появившиеся кристаллы выглядели очень похоже: в основном кубические кристаллы KCl с привычными формами роста. Менялись не структура кристаллов, а условия, вызвавшие их зарождение. При наложенных массовых потоках кристаллы возникали при более низком локальном пересыщении и в местах, управляемых градиентами, а не пиками концентрации. Это позволяет предположить, что направленное молекулярное движение в жидкости способствует образованию плотных участков ионов, служащих ранними ядрами, эффективно сужая метастабильную зону. В то время как классическая теория нуклеации не может полностью объяснить такое поведение, современные идеи многоступенчатой нуклеации согласуются с полученными результатами. С практической точки зрения работа указывает на более разумное управление кристаллизацией в процессах вроде опреснения с нулевым сбросом жидкостей, где использование термодиффузии может помочь превращать отходные рассолы в твердые соли с меньшими затратами энергии и химикатов.
Цитирование: Xu, S., Torres, J.F. Crystallisation triggered by mass diffusion at a lower local supersaturation. Commun Chem 9, 125 (2026). https://doi.org/10.1038/s42004-026-01925-8
Ключевые слова: кристаллизация, термодиффузия, пересыщение, опреснение, массовый транспорт