Clear Sky Science · ru
Синергетические эффекты катионов и граней ускоряют кинетику щелочного образования водорода на ступенчатых поверхностях Pt
Почему это важно для чистой энергетики
Производство чистого водорода из воды — ключевой элемент многих планов по достижению нулевых выбросов, но в современных наиболее практичных устройствах теряется энергия, поскольку реакция, дающая пузырьки водорода, может идти удивительно медленно в щелочной (основной) среде. В этом исследовании авторы уточняют причины на уровне отдельных атомов и молекул воды, объясняя, почему одни поверхности платины работают лучше других и как обычные растворённые ионы в жидкости могут взаимодействовать с металлической поверхностью, ускоряя образование водорода.
Формирование поверхности металла для управления водой
Исследователи сосредотачиваются на платине — эталонном материале для расщепления воды — и сравнивают два типа атомных ландшафтов на её поверхности. Один — плоский, как гладкая терраса (обозначаемая Pt(111)); другой — ступенчатый, как крошечная лестница (Pt(311)). Используя передовые квантово‑механические моделирования, включающие и электроны, и подвижные молекулы воды, они моделируют поведение этих поверхностей при реалистичных рабочих напряжениях в щелочном электролизёре. Цель — понять, как локальная среда прямо у металла — где встречаются вода, ионы и электроны — контролирует скорость первого этапа образования водорода.
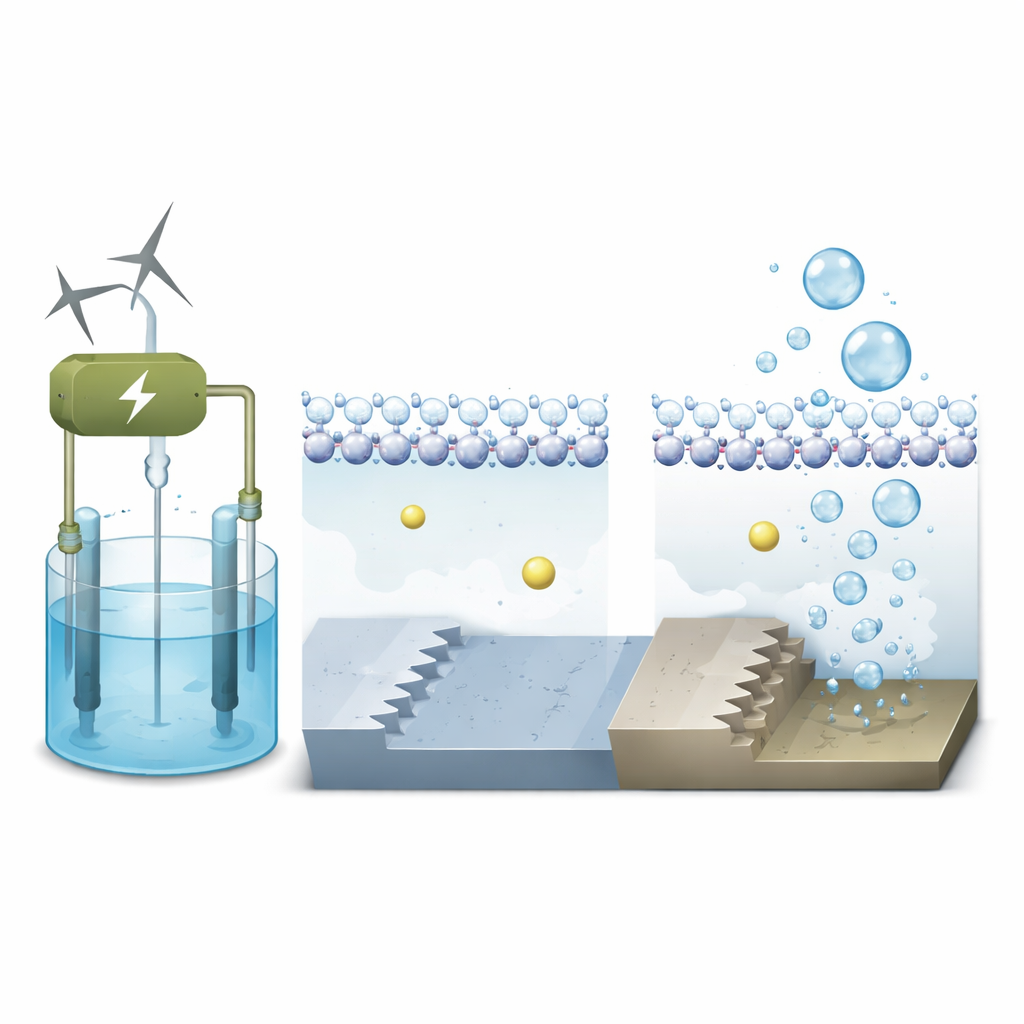
Соляные ионы как скрытые помощники
В щелочных электролизёрах в жидкости присутствуют ионы щелочных металлов, например натрий. Эти положительно заряженные ионы не просто плавают; они могут концентрироваться у электрода и тонко перестраивать электрическое поле на интерфейсе. Моделирования показывают, что на плоской платиновой террасе вода образует плотный упорядоченный слой с направленными вниз к отрицательно заряженной поверхности атомами водорода. Ионы натрия остаются дальше, отделённые от металла этим водным слоем, поэтому их влияние на реакцию невелико. На ступенчатой поверхности, однако, недокоординированные атомы на краю ступени сильнее связывают воду и создают более шероховатую, неупорядоченную локальную структуру воды.
Особый ближний кластер, который притягивает ионы
На этих краях ступеней команда обнаруживает повторяющийся структурный мотив: молекула воды, непосредственно связанная с платиновым шагом, которая, в свою очередь, удерживает рядом ион натрия, окружённый дополнительными молекулами воды. Этот компактный кластер платина–вода–натрий фактически тянет ион примерно на 2,3 ангстрема ближе к металлу, чем на плоской поверхности. Такое приближение существенно усиливает локальное электрическое поле в этом крошечном районе, сильно поляризуя прилегающие молекулы воды. Моделирование показывает, что одна O–H связь в этих молекулах заметно удлиняется, что указывает на её частичное разрывное состояние ещё до формального протекания реакции.
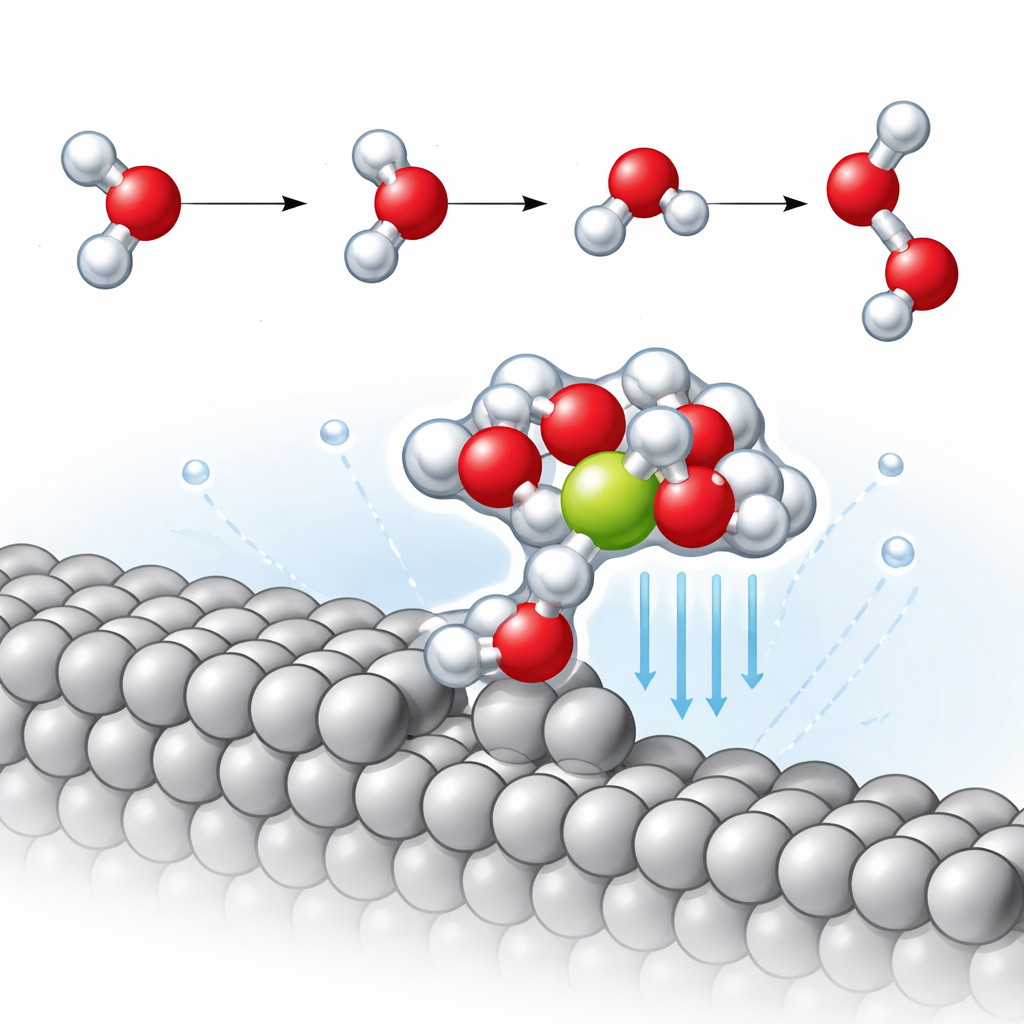
Снижение барьера для образования водорода
Ключевой медленный этап в щелочном образовании водорода известен как шаг Вольмера, когда молекула воды распадается: атом водорода связывается с металлом, а оставшийся гидроксид уходит в жидкость. Проследив путь минимальной энергии реакции, авторы обнаружили, что на плоской платино‑вой поверхности натрий оказывает лишь небольшое влияние на энергетический барьер этого шага. Напротив, на ступенчатой поверхности близко расположенный стабилизированный натрием кластер снижает энергию активации примерно на 0,14 электронвольта — примерно в три раза сильнее, чем улучшение на плоской грани. Детальный анализ колебательных движений показывает, что O–H связь, направленная к поверхности, значительно ослабляется в присутствии близко расположенного иона, что облегчает её разрыв и, таким образом, ускоряет образование водорода.
Правило проектирования для лучших катализаторов водорода
В целом исследование приходит к выводу, что лучшая работа в щелочном производстве водорода достигается не только за счёт самой металлической поверхности или электролита, но их синергии. Ступенчатые сайты платины, способные закреплять особые водно‑ионные кластеры, притягивают щелочные катионы ближе, усиливают локальное электрическое поле, частично «предразрывают» связи в воде и значительно ускоряют важнейший первый шаг выделения водорода. Для неспециалиста основной вывод таков: при аккуратном формировании микроскопической формы поверхностей катализатора и выборе электролитов, которые доставляют нужные ионы в нужные места, инженеры могут преодолеть некоторые фундаментальные замедляющие факторы щелочных устройств и спроектировать более эффективные, энергосберегающие системы для производства чистого водорода.
Цитирование: Zhang, Q., Sun, P., Li, H. et al. Synergistic cation-facet effects boost alkaline hydrogen evolution kinetics on stepped Pt surfaces. Commun Chem 9, 113 (2026). https://doi.org/10.1038/s42004-026-01924-9
Ключевые слова: выделение водорода, щелочной электролиз, катализатор из платины, интерфейсная вода, щелочноземельные катионы