Clear Sky Science · ru
Структурная основа образования филаментов человеческого RegⅢα
Как наш кишечник борется с микробами
Наши кишки постоянно контактируют с миллиардами бактерий, многие из которых безвредны или даже полезны. Но когда появляются опасные микроорганизмы, организму нужны быстрые и точные способы атаковать их, не повреждая собственные ткани. В этом исследовании подробно рассматривается один из таких белков‑защитников, называемый RegIIIα, и показано, как он меняет свою форму, чтобы убивать бактерии, а затем переключается в более безопасное, менее активное состояние. Понимание этого «перевоплощения» помогает ученым лучше понять, как поддерживается баланс микробиоты кишечника и что идет не так при заболеваниях.
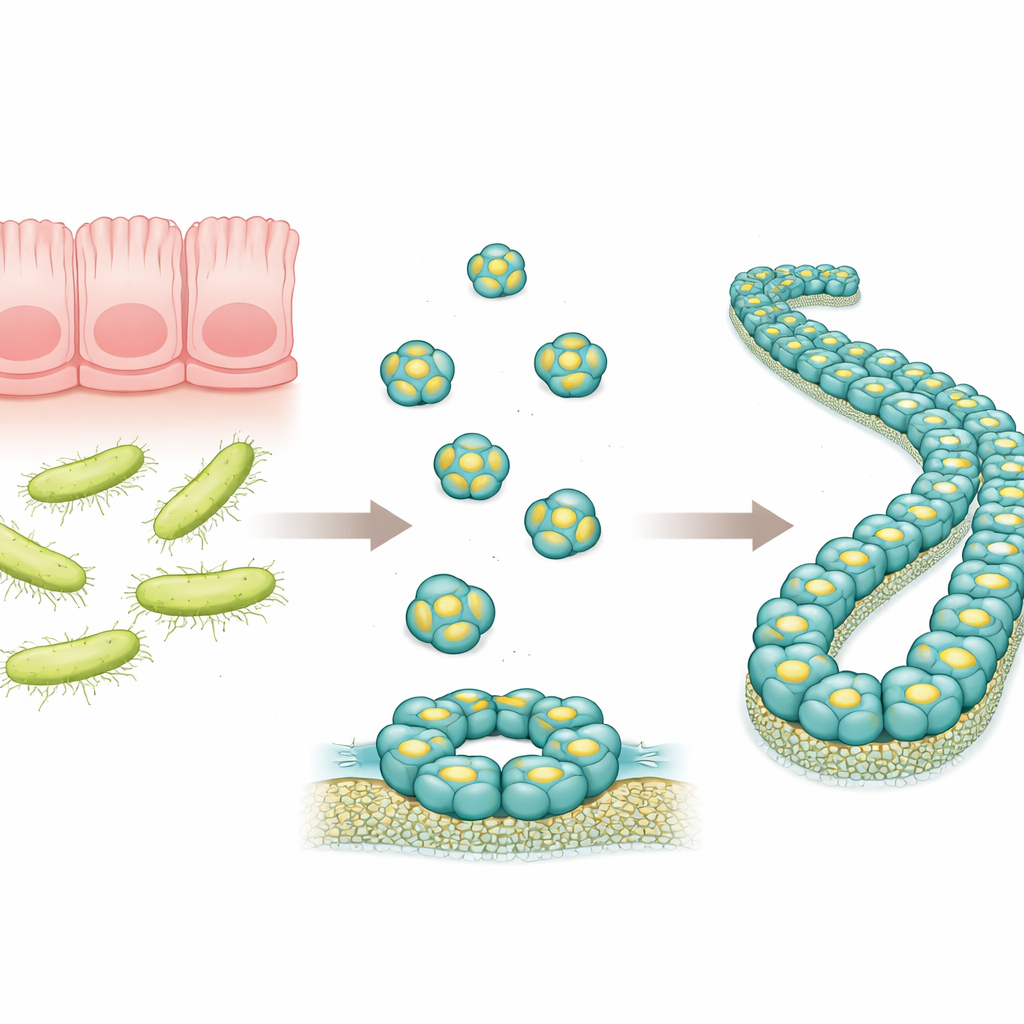
Крошечный защитник в кишечнике
RegIIIα — это белок, вырабатываемый в пищеварительном тракте, который нацелен на определенные бактерии, особенно на грамположительные с толстой внешней стенкой. Ранее предполагали, что RegIIIα может проделывать отверстия в бактериальных мембранах, формируя кольцевые структуры, через которые содержимое микроба вытекает, что приводит к его гибели. Наблюдали также, что со временем эти кольца могут складываться в длинные филаменты, которые, по-видимому, снижают бактерицидную активность белка. Однако точная организация молекул RegIIIα в таких крупных сборках была неизвестна, что затрудняло понимание механизма действия белка и управления его активностью.
Видение филамента на атомном уровне
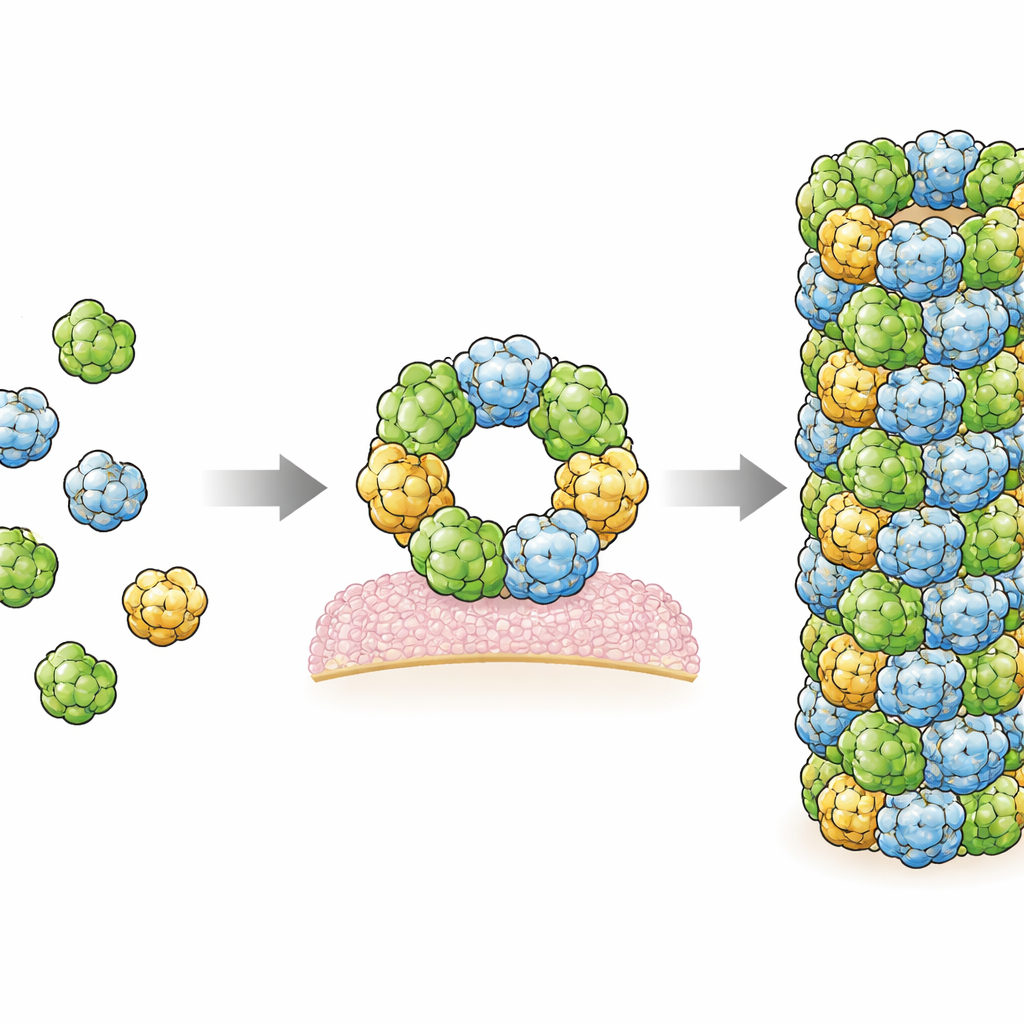
В этом исследовании авторы воспроизвели человеческий RegIIIα в бактериальной системе и затем инициировали его сборку в филаменты в контролируемых условиях. Они использовали мощный метод визуализации — криоэлектронную микроскопию, которая позволяет визуализировать биологические молекулы, замороженные в тонком слое льда, с почти атомным разрешением. Выяснилось, что филаменты состоят из повторяющихся троек идентичных единиц RegIIIα — тримеров, которые укладываются в регулярную спиральную структуру. Каждая отдельная молекула RegIIIα выглядит очень похоже на ранее описанные структуры из кристаллов, но их ориентация внутри филамента отличается от предложенной в более ранней модели с низким разрешением. Эта исправленная ориентация меняет представления о том, как белок взаимодействует с бактериальными мембранами и с собственной регуляторной секцией.
Как белки связываются и почему важны липиды
Тщательно изучив структуру, исследователи выделили две основные контактные области, или интерфейса, где соседние молекулы RegIIIα соприкасаются и удерживают филамент вместе. Они затем модифицировали отдельные аминокислоты в этих интерфейсах и показали, что такие изменения препятствуют образованию филаментов, подтвердив тем самым, что эти контактные участки важны для сборки. Интересно, что в картах крио‑ЭМ в обоих интерфейсах обнаружились дополнительные размытые области, которые, вероятно, представляют собой небольшие вытянутые молекулы, зажатые между белковыми поверхностями. Их форма и химическое окружение указывают на то, что это могут быть липиды — те самые маслянистые молекулы, из которых состоят клеточные мембраны. Это подтверждает ранее высказывавшиеся предположения о том, что липиды способствуют сборке RegIIIα, возможно действуя как молекулярный клей, стабилизирующий взаимодействия между субъединицами.
Переключатель включения–выключения: pH и скрытый фрагмент
Авторы также изучили, что определяет момент, когда RegIIIα способен собираться. До активации белок содержит короткий «про‑фрагмент», который должен быть отрезан пищеварительными ферментами. В их структуре филамента с высоким разрешением в центре сборки нет места для этого дополнительного фрагмента, что подразумевает: про‑сегмент препятствует образованию поровых колец и филаментов. Они обнаружили также, что склонность к формированию филаментов зависит от кислотности: при pH, близком к pH тонкой кишки, филаменты образуются охотно, тогда как в более кислотной среде — плохо. Одна аминокислота, гистидин 50, ведет себя как pH‑чувствительный переключатель; при замене этого остатка чувствительность сборки к pH значительно снижается. В совокупности эти механизмы — расщепление ферментами, связывание липидов и влияние pH — образуют многоуровневую систему контроля, которая настраивает, когда и где RegIIIα активен.
Что это значит для здоровья кишечника
В целом эта работа дает наиболее подробную картину того, как молекулы RegIIIα собираются в более крупные структуры, связанные как с их антибактериальным действием, так и с самоограничивающимся поведением. Те же интерфейсы, которые формируют филаменты, участвуют и в построении гексамерных колец, предположительно образующих поры в бактериальных мембранах, что указывает на тонкий баланс между мощной убивающей формой и более безопасным, «приглушенным» состоянием. Нанесение мутаций, связанных с заболеваниями, на эту структуру показывает, что многие из них расположены в ключевых контактных точках, что предполагает: нарушение сборки может лежать в основе некоторых кишечных или поджелудочных расстройств. Уточнив, как активируется этот природный антибиотик, как липиды направляют сборку и как местный pH формирует его поведение, исследование прокладывает путь для будущих попыток модулировать врожденные защитные механизмы — либо усиливая их против инфекций, либо сдерживая, когда они становятся нарушенными.
Цитирование: Han, J., Cao, Q. Structural basis for human RegⅢα filament formation. Commun Chem 9, 117 (2026). https://doi.org/10.1038/s42004-026-01921-y
Ключевые слова: RegIIIα, кишечный иммунитет, криоэлектронная микроскопия, белковые филаменты, антибактериальные пептиды