Clear Sky Science · ru
Ионно-изменяемые амфифильные янус-гликозиды с азобензольным мостиком для светоуправляемой однокомпонентной и органо-модулируемой доставки pDNA
Свет, раскрывающий более умную доставку генов
Генные терапии обещают лечить заболевания у их корня, доставляя фрагменты генетического кода прямо в наши клетки. Но безопасно провести этот хрупкий груз через кровь, попасть в нужные органы и внутрь целевых клеток — по‑прежнему серьёзная задача. В этом исследовании представлен новый класс мелких сахаросодержащих частиц, поведение которых можно переключать светом до их введения в организм, что позволяет перенаправлять, куда попадёт терапевтический ген и насколько сильно он будет экспрессироваться, при этом клетки в основном остаются невредимыми. 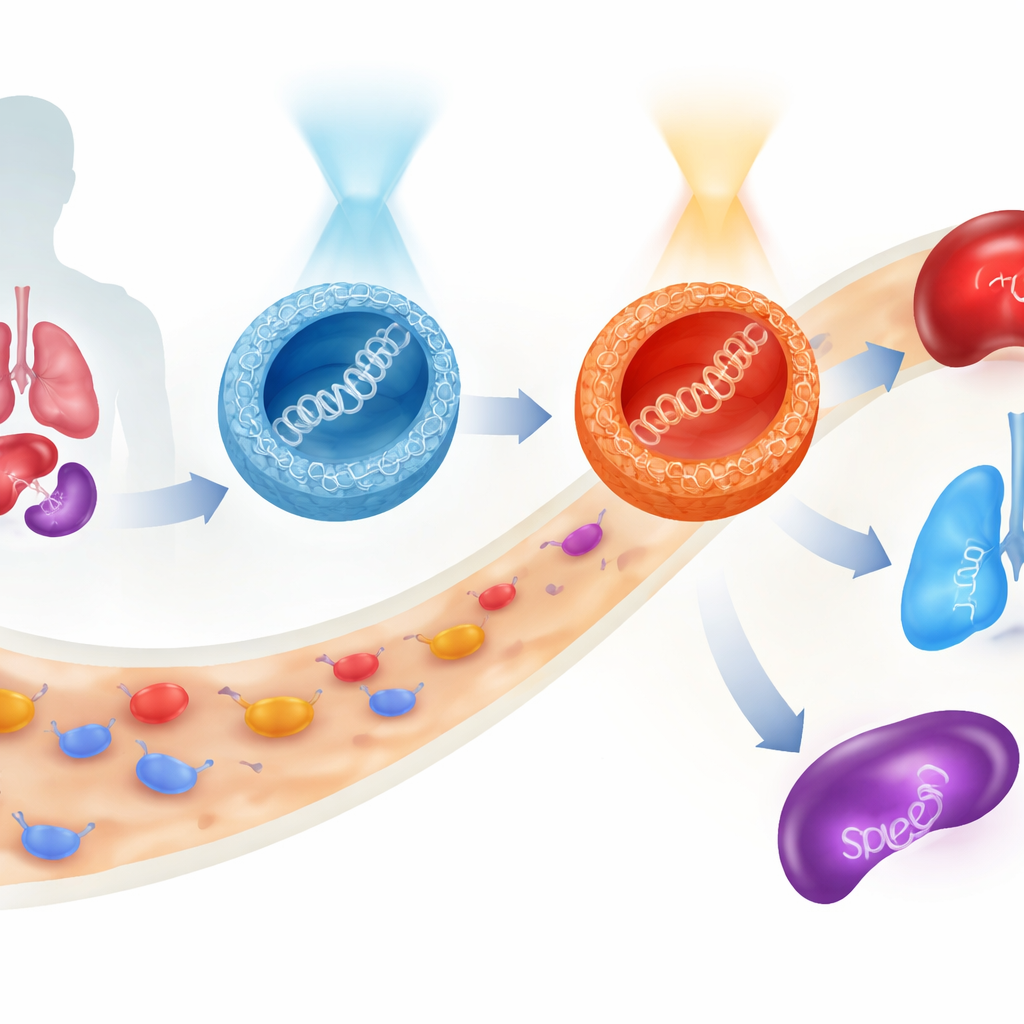
Необходимость точных генетических курьеров
Сегодня наиболее успешными средствами доставки генов являются липидные наночастицы, которые помогли сделать возможными мРНК-вакцины против COVID-19. Эти многокомпонентные капли оборачивают и защищают нуклеиновые кислоты, но они, как правило, накапливаются преимущественно в печени и внутри клеток освобождают лишь малую часть груза. Изменение их состава может сдвинуть предпочтение органов, но смеси сложны и трудно поддаются точному контролю. Авторы статьи решили спроектировать вместо этого отдельные, хорошо определённые молекулы, которые самоассамблируются в наночастицы с предсказуемой формой и поведением — и которые можно активно настраивать извне с помощью простого светового триггера.
Молекулярные качели, управляемые светом
В основе новой системы лежат парные «янусовые» гликозиды: молекулы, построенные из двух глюкозных звеньев, оснащённые гидрофильными заряженными «головами» и липофильными «хвостами», соединённые через центральный азобензольный «шарнир». Азобензол может переключаться между двумя зеркальными формами, называемыми E и Z, при облучении светом разных длин волн. В воде в присутствии ДНК многие копии этих молекул спонтанно собираются в мягкие слоистые частицы, которые обволакивают нити плазмидной ДНК. Исследователи подготовили две версии — с кислородными мостиками и с серными мостиками между сахаром и шарниром — чтобы тонко настроить стабильность и биологическое поведение. Предварительно облучая растворы, они могли обогатить либо форму E, либо форму Z и изучать, как каждое состояние влияет на получающиеся частицы для доставки генов.
Как ведут себя формы-«перекраски» частиц
Измерения размера частиц, поверхностного заряда и внутренней структуры показали, что световое переключение между состояниями E и Z имеет ясные физические последствия. Как правило, форма Z давала более мелкие, более однородные наночастицы с более упорядоченным, слоистым внутренним устройством по сравнению с формой E. Микроскопия показала, что эти внутренние структуры напоминают чередующиеся слои липидоподобного материала и ДНК. Важно, что обе формы защищали ДНК от ферментативного разложения. В культурах клеток почки, печени и иммунной ткани разные изомеры вызывали поразительно разные уровни экспрессии гена, хотя сама ДНК была одинаковой. Повторные световые импульсы, применённые после попадания частиц в клетки, многократно усиливали экспрессию гена, что указывает на то, что механический толчок от переключения помогает частицам раскрыться и освободить груз, а также может способствовать их выходу из внутриклеточных компартментов. 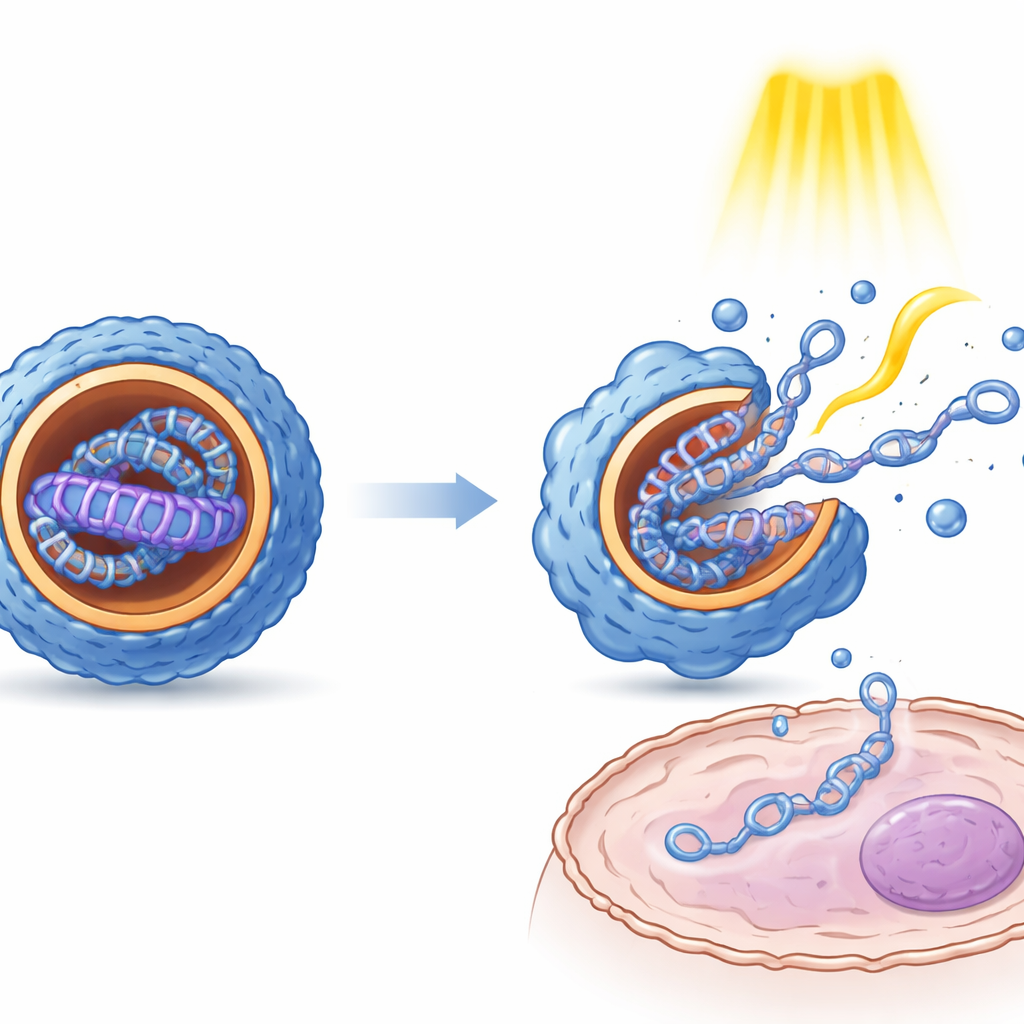
Направление генов к определённым органам
Наиболее неожиданное поведение проявилось у мышей. Когда частицы с кислородным мостиком вводили в форме, обогащённой E, экспрессия маркерного гена происходила преимущественно в печени с некоторой активностью в лёгких. Предварительное переключение их в форму Z до инъекции не только увеличивало суммарную экспрессию, но и сдвигало баланс в сторону лёгких. Частицы с серным мостиком показали другую картину: их форма Z предпочитала селезёнку — ключевой иммунный орган. Таким образом, с той же базовой молекулярной платформы — и без изменения ДНК-груза — исследователи могли направлять активность гена преимущественно в печень, лёгкие или селезёнку просто выбирая связь (кислородную или серную) и светоактивную форму (E или Z) носителя. На протяжении всех испытаний жизнеспособность клеток оставалась высокой, что указывает на относительную мягкость системы.
Светонастраиваемый путь к будущим генным препаратам
Проще говоря, команда создала крошечный светоуправляемый шаттл для ДНК. До инъекции краткое световое воздействие «программирует» шаттлы в одну из двух форм. Каждая форма самоассамблируется в наночастицы с характерным размером и поверхностными свойствами, что, в свою очередь, определяет, насколько прочно они прикрепляются к разным типам клеток и где в организме они окажутся. Поскольку одна и та же химическая основа может быть модифицирована множеством тонких способов, а переключение обратимо и не меняет саму ДНК, эта платформа предлагает гибкий способ тонкой настройки местоположения и механизма действия генотерапий. Хотя до клинического применения ещё далеко, исследование показывает, что тщательно спроектированные одномолекулярные носители, управляемые светом, могут стать мощными инструментами для более безопасных и точных генетических лекарств.
Цитирование: Wang, Z., Rivero-Barbarroja, G., Benito, J.M. et al. Azobenzene-bridged ionizable amphiphilic Janus glycosides for light-controlled, single-component and organ-modulable pDNA delivery. Commun Chem 9, 118 (2026). https://doi.org/10.1038/s42004-026-01920-z
Ключевые слова: доставка генов, светочувствительные наночастицы, азобензольные переключатели, таргетная ДНК-терапия, наномедицина