Clear Sky Science · ru
Сравнительная оценка моделей глубокого обучения для предсказания активности противоопухолевых препаратов (IC50) с практическими выводами для медицинских химиков
Почему это исследование важно для будущих противораковых препаратов
Разработка новых противораковых лекарств медленная и дорогая, поскольку каждую перспективную молекулу нужно тестировать в живых клетках, чтобы выяснить, насколько сильно она подавляет их рост. В этом исследовании поставлен практический вопрос: могут ли современные инструменты искусственного интеллекта надежно предсказывать эти результаты заранее, экономя время и средства в лаборатории? Авторы систематически сравнивают несколько популярных систем глубокого обучения, выясняют, в каких ситуациях они успешны или терпят неудачу, и даже предлагают более реалистичный способ оценить их полезность для практикующих медицинских химиков.
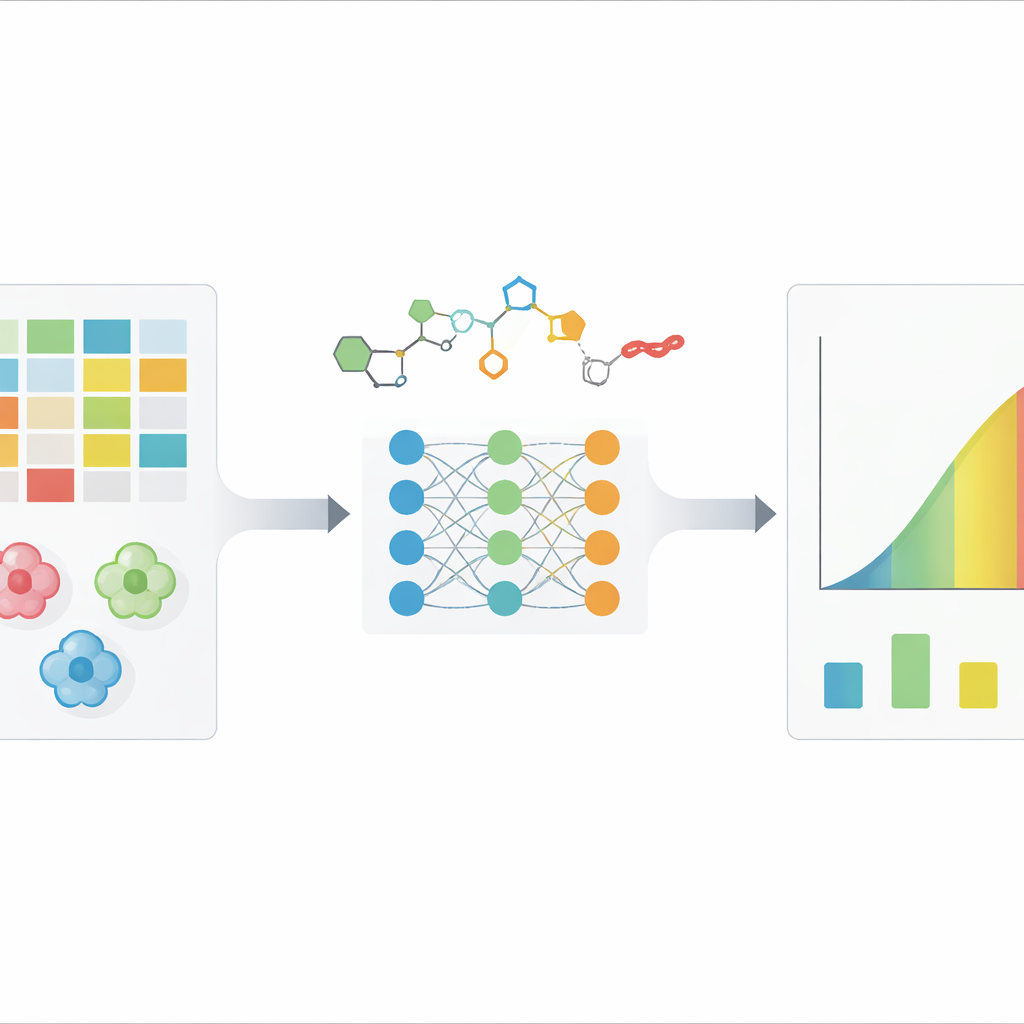
Как измеряют, насколько препарат борется с раковыми клетками
Когда исследователи тестируют потенциальное противоопухолевое соединение, они часто указывают число, называемое IC50: концентрация, при которой препарат снижает рост клеток вдвое. Низкое IC50 означает высокий потенциал препарата. Но одна и та же молекула может иметь очень разные значения IC50 в разных клеточных линиях рака, и даже повторные тесты для одной и той же пары «препарат—клетка» могут отличаться в несколько раз в зависимости от метода и условий. Традиционные методы компьютерного моделирования хорошо отражают взаимодействие молекулы с одним белковым мишенью, но испытывают трудности при учете полной сложности живой клетки. Новые методы глубокого обучения пытаются извлекать закономерности непосредственно из больших наборов данных, связывающих химические структуры и подробную генетическую информацию о клетках с их измеренными значениями IC50.
Испытание пяти инструментов глубокого обучения
Авторы рассмотрели пять ведущих моделей глубокого обучения, каждая из которых использует разную стратегию представления как препаратов, так и клеток рака. Некоторые рассматривают молекулы как графы атомов и связей; другие превращают генетические данные клеток в структурированные сети биологических процессов или выделяют наиболее информативные гены. Все модели были обучены и оценены на одном и том же курированном наборе данных из крупного ресурса GDSC, содержащего десятки тысяч измеренных значений IC50. Команда также разработала намеренно простой метод сравнения: «базовый» подход, который игнорирует биологию и химию и просто предсказывает средние значения IC50 по тренировочным данным. Это позволило задать не только вопрос, какая глубокая модель лучше, но и действительно ли какая-либо из них превосходит очень наивную стратегию.
Более реалистичный способ оценки предсказаний
Обычные метрики машинного обучения, такие как корреляция и среднеквадратичная ошибка, могут выглядеть впечатляюще, но их трудно интерпретировать для экспериментаторов. Чтобы сократить этот разрыв, авторы переписали качество предсказаний в более интуитивных величинах, таких как процентная ошибка и погрешность в логарифмическом масштабе, которая напрямую соответствует разнице в кратностях IC50. Важно, что они также количественно оценили шум в реальных измерениях IC50, проанализировав большую базу данных биологической активности. Показали, что при обычных условиях анализа 90% повторных измерений IC50 для одной и той же пары «препарат—клетка» попадают примерно в семикратный диапазон. Исходя из этого, они определили новую метрику — Точность предсказания с учётом экспериментальной изменчивости (EVAPA): процент предсказаний модели, попадающих в этот реалистичный экспериментальный интервал.
Где модели успешны и где терпят неудачу
При случайном разбиении данных так, чтобы многие препараты и клеточные линии присутствовали и в тренировочной, и в тестовой выборке, все модели глубокого обучения показали хорошие результаты. Они демонстрировали сильную корреляцию с измеренными значениями IC50 и высокие показатели EVAPA, явно превосходя простой базовый подход. Производительность оставалась приемлемой, когда модели проверяли на способность обобщать на полностью новые клеточные линии при условии, что препараты были знакомы; в этом случае даже базовая модель показала удивительно хорошую работу, что говорит о том, что среднее поведение препарата по множеству типов клеток уже содержит полезную информацию. Настоящие проблемы возникали при встрече моделей с новыми химическими структурами: точность резко падала, корреляции приближались к нулю или даже становились отрицательными, и в некоторых тестах простая базовая модель соперничала с глубокими моделями или превосходила их. Команда также проверила, зависят ли ошибки предсказаний от базовых свойств препаратов — таких как размер, полярность или гибкость — или от тканевой принадлежности клеточных линий. Они обнаружили лишь слабые связи, что подразумевает, что модели работают примерно одинаково на разнообразных химиях и типах рака — но по-прежнему дают сбои на по-настоящему новых соединениях.
Проверка действительно новых молекул из недавних исследований
Чтобы выйти за рамки публичных баз данных, авторы собрали более 150 недавно описанных в литературе противораковых соединений и протестировали на этих ранее не встречавшихся молекулах несколько моделей глубокого обучения. Результаты отразили сценарий «нового препарата» из данных GDSC: предсказания были шумными, с большими процентными ошибками и лишь умеренной долей предсказаний, попадающих в реалистичные экспериментальные границы. Тем не менее поведение моделей при разных типах ассайев указывало на то, что они захватывают некоторые типовые, не зависящие от конкретного метода измерения, закономерности влияния препаратов на клетки. Простой веб‑сервер, собранный на базе этих моделей, теперь позволяет химикам ввести структуру и получить предсказанные значения IC50 для сотен клеточных линий рака, с оговоркой, что надежность выше всего, когда новая молекула похожа на те, что были в тренировочном наборе.
Что это значит для разработки лекарств
Эта работа демонстрирует, что современные инструменты глубокого обучения уже полезны для ранжирования и исследования идей по противораковым препаратам, когда они работают в пределах знакомой химической области, но они далеки от того, чтобы быть «кристальным шаром» для по-настоящему новых молекулярных дизайнов. Подчёркивая, что грубая модель на основе среднего иногда может соперничать со сложными нейросетями, и вводя меру точности, основанную на реальной экспериментальной изменчивости, исследование даёт медицинским химикам более ясное представление о том, чего ожидать от программ для предсказания IC50. Вывод сбалансирован: эти модели — перспективные помощники в разработке лекарств, особенно при тщательной бенчмаркинге, но для надёжного руководства в поиске следующего поколения противораковых терапий всё ещё требуются значительные улучшения архитектур и стратегии обучения, особенно для молекул вне распределения тренировочных данных.
Цитирование: Garai, U., Pal, A.S., Ghosh, K. et al. Benchmarking deep learning models for predicting anticancer drug potency (IC50) with insights for medicinal chemists. Commun Chem 9, 106 (2026). https://doi.org/10.1038/s42004-026-01916-9
Ключевые слова: активность противоопухолевых препаратов, предсказание IC50, модели глубокого обучения, клеточные линии рака, вычислительное открытие лекарств