Clear Sky Science · ru
Протеаза S9 WprP2 катализирует равномерное расщепление прекурсорного пептида при биосинтезе RiPP
Почему маленькие режущие инструменты в клетках важны
Внутри бактерий специализированные молекулярные «ножницы» разрезают длинные цепочки аминокислот на меньшие, активные фрагменты, которые часто превращаются в антибиотики или другие полезные натуральные продукты. В этом исследовании обнаружен ранее неизвестный режущий инструмент — протеаза WprP2, которая обрезает свой целевой пептид с необычной точностью. Понимание механизма работы этого фермента может помочь учёным проектировать новые биологически активные пептиды и антибиотики следующего поколения.
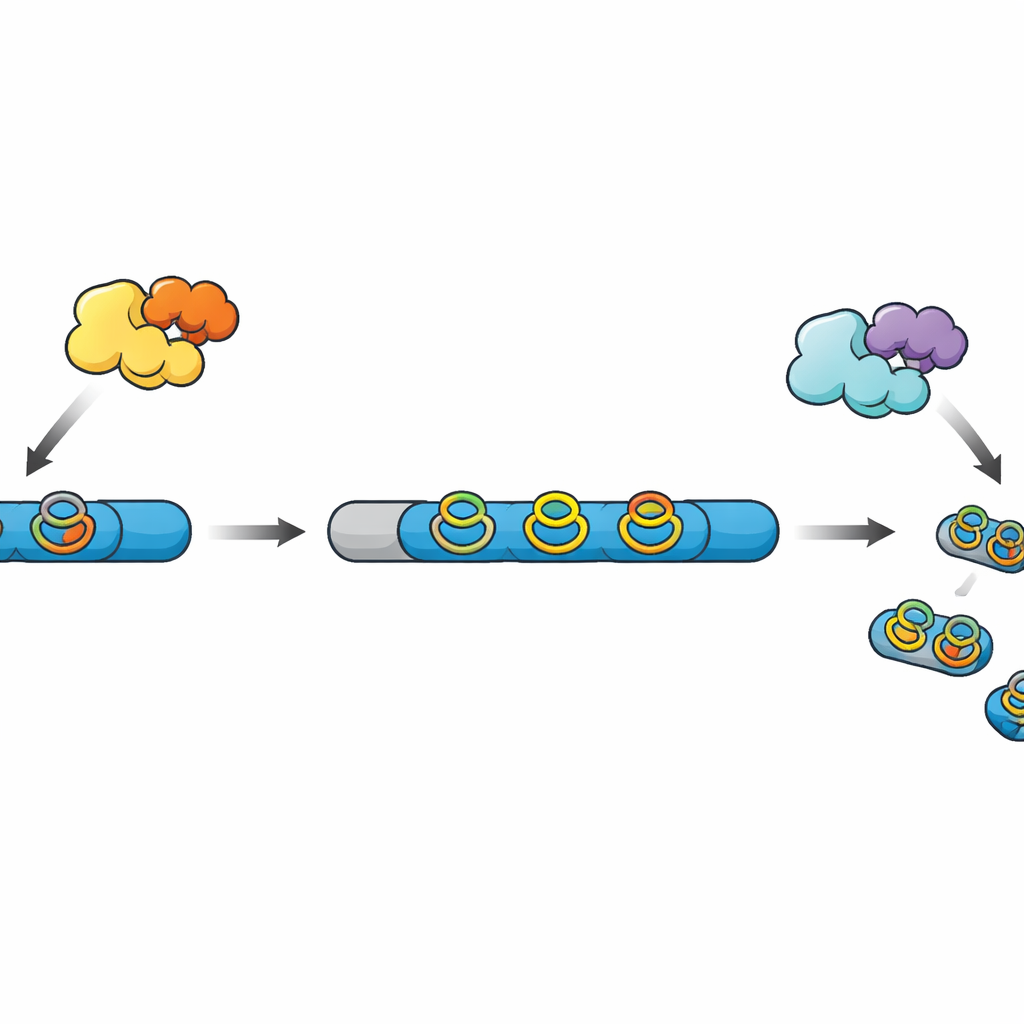
От сырой цепочки до готовых мини‑лекарств
Многие современные пептидные натуральные продукты, объединённые под общим именем RiPP, начинаются как простые цепочки, синтезируемые на рибосоме. Эти цепочки содержат лидирующую область, которая служит «ручкой», и коровую часть, которая после ряда химических модификаций станет финальным продуктом. Другие ферменты вносят поперечные связи и кольца, делающие пептид более устойчивым и активным, а в конце протеаза отрезает лид и освобождает зрелую молекулу. В недавно открытой семье RiPP радикальные SAM‑ферменты формируют компактные «циклофановые» кольца с участием ароматических аминокислот, но в большинстве известных генных кластеров соответствующая протеаза отсутствует, и финальные стадии обработки остаются загадкой.
Поиск пропавшего партнёрного фермента
Авторы ранее изучали радикальную SAM‑фермент WprB1, который встраивал идентичные поперечные связи в трёх повторяющихся сегментах WPR прекурсорного пептида. В новой работе они искали в бактериальных геномах родственников этого фермента и просматривали соседние гены в поисках потенциальной протеазы. В Streptomyces venezuelae они нашли перспективный кластер, содержащий сходный фермент для кросслинкинга, вспомогательный белок, подходящий прекурсорный пептид с тремя повторами WPR и кандидатную сериновую протеазу семейства S9, которую назвали WprP2. Это сделало систему идеальной для исследования того, как пептид окончательно разрезается и высвобождаются активные фрагменты.
Наблюдение за разрезанием пептида
Чтобы изучить WprP2, команда получила прекурсорный пептид в бактериях, как в присутствии, так и в отсутствии фермента для кросслинкинга, очистила его и затем смешала с протеазой в контролируемых in vitro реакциях. Масс‑спектрометрия показала, что WprP2 сначала отрезает цепь сразу после каждого сегмента WPR, а затем выполняет второй разрез на фиксированном расстоянии перед определённой пролиновой остатком дальше по последовательности. Эти два шага создают серию меньших, одинаковых фрагментов. Примечательно, что WprP2 выполнял эту схему разрезов независимо от того, установила ли уже фермента кросслинки‑циклофановые кольца, что показывает: кольца не требуются для распознавания. По сравнению с коммерческим трипсином, который не способен резать в некоторых перекрещённых участках, WprP2 продолжала функционировать, подчёркивая её необычную стойкость.
Расшифровка того, что распознаёт фермент
Исследователи затем выясняли, какие особенности пептида WprP2 «считывает». Систематически меняя отдельные аминокислоты вокруг сайтов разреза, они обнаружили, что замены многих соседних остатков мало влияют на активность, но изменение ключевого аргинина в сегменте WPR или глутамина и пролина во втором сайте разреза может блокировать соответствующий шаг. Эксперименты с родственным прекурсорным пептидом с другими фланкирующими остатками показали, что протеаза всё равно разрезает после повторов WPR, но выполняет второй разрез только при наличии пары глутамин‑пролин. Структурные модели, сгенерированные с помощью AlphaFold3, поддержали эту картину: в предсказанных комплексах участки на основе WPR и участок глутамин‑пролин по очереди выстраиваются в каталитическом центре фермента, что согласуется с поэтапным двухшаговым механизмом.
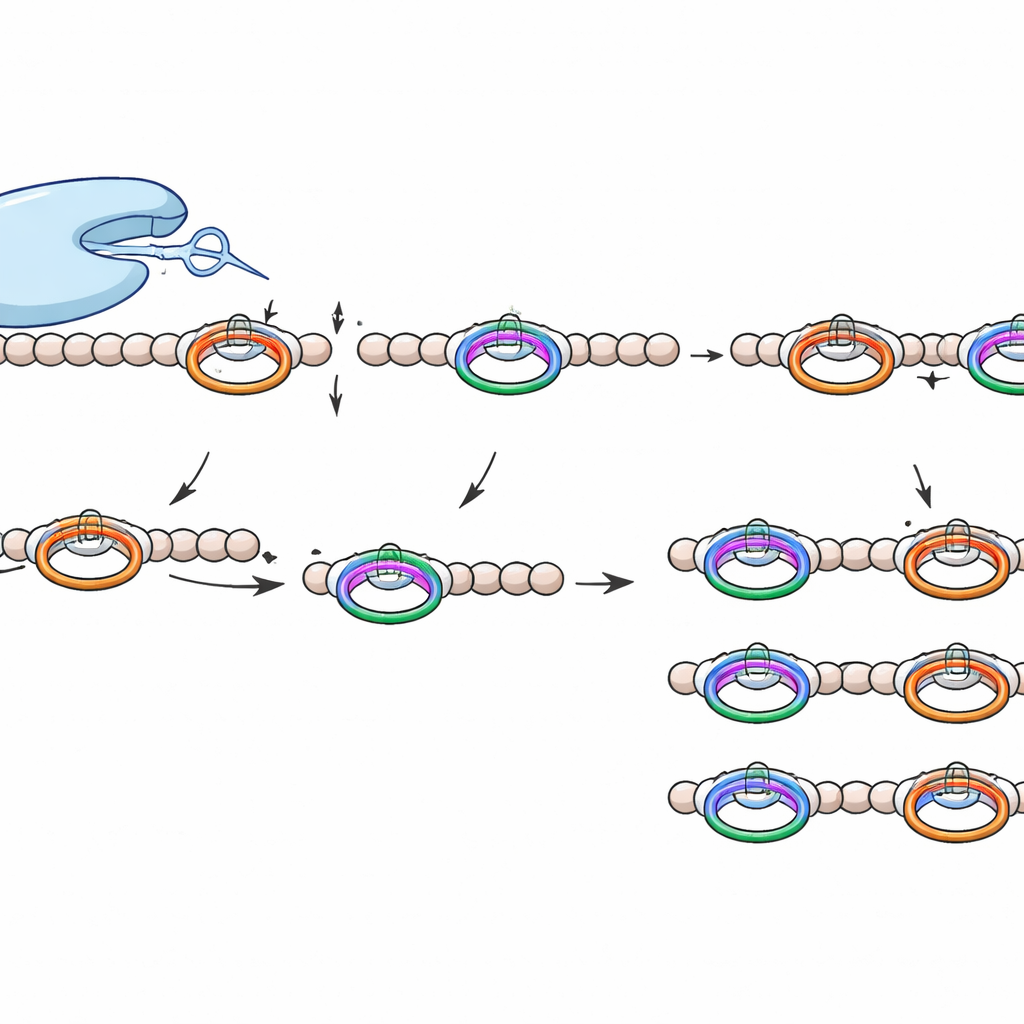
Что делает этот режущий инструмент особенным
WprP2 принадлежит к более широкой семье протеаз S9, в которую уже входят ферменты медицинского значения, но выделяется по нескольким признакам. Она разрезает с N‑терминальной стороны пролина, а не после него, действует на повторяющийся мотив, чтобы генерировать равномерно размеченные фрагменты по всей прекурсорной цепи, и проявляет широкую толерантность к аминокислотам, лежащим между двумя сайтами распознавания. Такое сочетание точности и гибкости ранее не наблюдали у протеаз, связанных с RiPP.
Как можно использовать это открытие
Обнаружив протеазу, которая распознаёт простые последовательностные сигналы и выполняет равномерные повторяющиеся разрезы, исследование добавляет мощный новый инструмент в растущий арсенал для инженерии пептидов. На практике WprP2 можно использовать для высвобождения или переработки дизайнерских пептидов, включая те, что содержат сложные кросслинки и устойчивы к стандартным ферментам, таким как трипсин. Для неспециалистов ключевая мысль такова: учёные обнаружили новый тип молекулярных ножниц, который разрезает длинные пептидные цепи на точные, одинаковые по размеру куски, что открывает путь к более контролируемому производству потенциальных антибиотиков и других биологически активных молекул.
Цитирование: Haedar, J.R., Khan, A.H., Ma, S. et al. S9 protease WprP2 catalyzes uniform cleavage on the precursor peptide in RiPP biosynthesis. Commun Chem 9, 108 (2026). https://doi.org/10.1038/s42004-026-01915-w
Ключевые слова: пептиды RiPP, сериновая протеаза, WprP2, натуральные продукты циклофановой структуры, инженерия пептидов