Clear Sky Science · ru
Зонд эмиссии, вызванной стерическим ограничением, для наблюдения конформаций белков в живых клетках
Наблюдение за преображающимися белками в реальном времени
Внутри каждой живой клетки белки постоянно меняют форму, передавая сигналы, ощущая окружение и выполняя жизненно важные функции. Многие заболевания возникают, когда эти изменения формы идут неправильно, но наблюдать такие движения непосредственно в живых клетках было чрезвычайно трудно, особенно на очень быстрых и очень медленных временных шкалах. В этой работе представлен новый светящийся зонд, названный BIOSCE, который превращает крошечные движения белков в видимые вспышки, позволяя исследователям отслеживать отдельные молекулы белка, когда они изгибаются, крутятся и взаимодействуют в реальном времени внутри живых клеток. 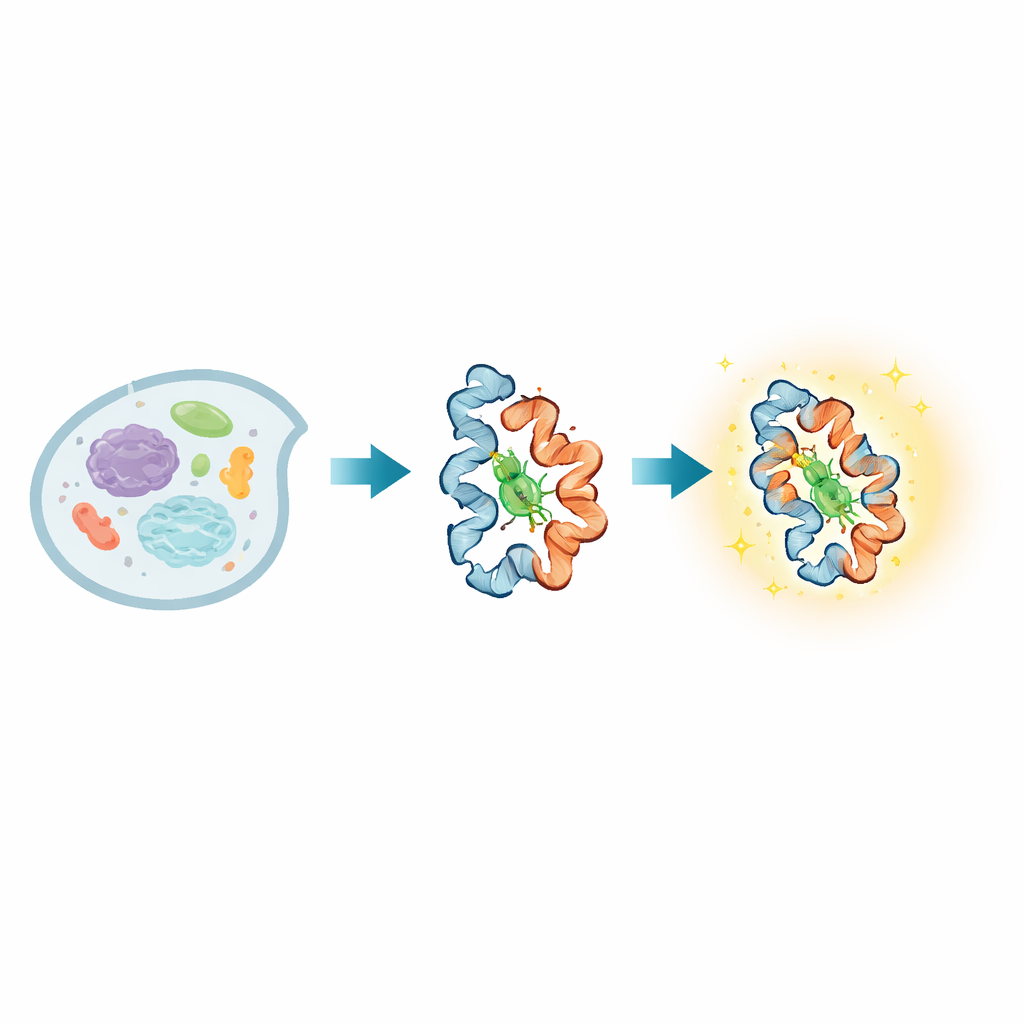
Новый световой переключатель для подвижных белков
В основе BIOSCE лежит маленькая краситель MTPABP-Cl, который становится ярче, когда на него оказывается «сжатие». Исследователи присоединяют этот краситель к широко используемому белковому тегу HaloTag, который может быть генетически слит практически с любым белком интереса. Когда меченый белок меняет форму или плотнее упаковывается с соседями, это изменяет «пространство», в котором краситель может двигаться. В рыхлой среде внутренние части красителя могут свободно вращаться, и большая часть поглощённого света теряется на движение; в более плотном кармане эти движения блокируются, и краситель вместо этого отдает больше этой энергии в виде света. Эта «эмиссия, вызванная стерическим ограничением», превращает тонкие изменения локальной скученности вокруг одного белка в плавное изменение яркости, а не в простую вкл/выкл реакцию, что делает зонд крайне чувствительным к небольшим конформационным изменениям.
Создание и тестирование чувствительного к сжатию красителя
Команда сначала разработала и синтезировала MTPABP-Cl так, чтобы он был тусклым в растворе, но усиливал свечение, когда его фиксирует HaloTag или более компактный белковый фьюжн. Тщательные измерения показали, что краситель поглощает синий свет и испускает дальний красный, что благоприятно для визуализации в глубине клетки и для длительного наблюдения. При связывании только с HaloTag его световой выход увеличивался; когда HaloTag был слит с партнерским белком, который «оборачивался» вокруг красителя, яркость повышалась ещё сильнее. Компьютерные моделирования подтвердили, что в более компактных белковых конфигурациях краситель испытывает более сильную скученность, меньшую открытую поверхность и больше стабилизирующих контактов, все из которых ограничивают движение и усиливают эмиссию. Краситель также связывается быстро и специфично с HaloTag, демонстрирует очень низкий фон в клетках, не несущих этот тег, и остаётся нетоксичным при рабочих концентрациях, что поддерживает его применение в экспериментах с живыми клетками. 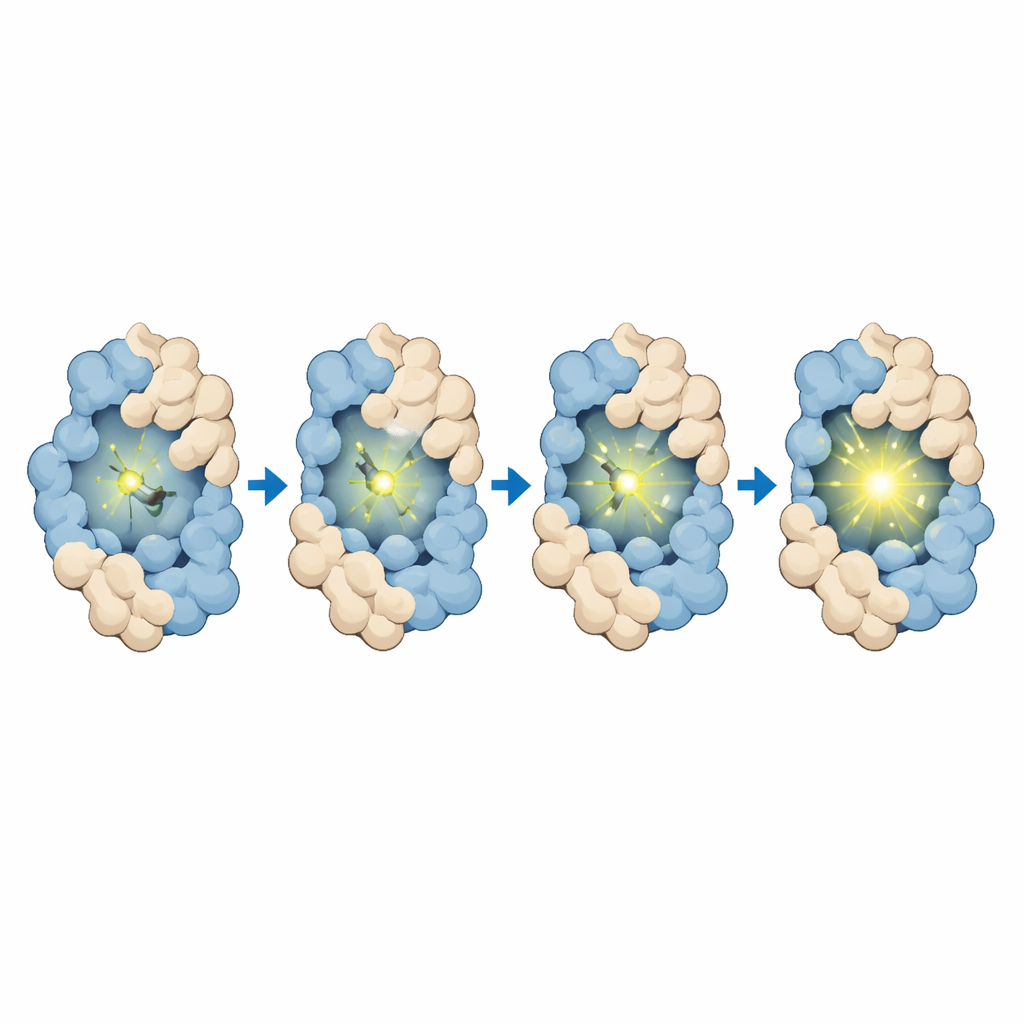
Отслеживание быстрых сигналов и встреч белков
Чтобы продемонстрировать возможности BIOSCE, авторы применили его к нескольким хорошо известным клеточным процессам. Сначала они адаптировали кальциевый сенсор на основе калмодулина — белка, который меняет форму при связывании ионов кальция, центральных в передаче нервных импульсов и многих других клеточных событиях. Слив калмодулин с HaloTag и маркировка MTPABP-Cl позволили создать хемигенетический индикатор под названием SCECaMP. В человеческих клетках и клетках, похожих на нейроны, этот индикатор увеличивал и уменьшал яркость синхронно с пиками кальция, вызванными калиевой стимуляцией, с скоростью отклика, сопоставимой с широко используемыми флуоресцентными белками GCaMP. Поскольку сигнал BIOSCE зависит непосредственно от локальной скученности вокруг красителя, он может верно отражать структурные изменения калмодулина и одновременно предоставлять стабильную, длительную флуоресценцию, подходящую для продолжительной визуализации.
Наблюдение взаимодействий, вызванных лекарствами, и повреждений токсином
Затем исследователи проверили, может ли BIOSCE отслеживать схождение двух белков под действием лекарства. Они использовали классическую систему, в которой рапамицин сводит вместе двух партнеров, FKBP и FRB, в ключевом пути контроля роста. Присоединив HaloTag к FKBP или FRB и маркировав MTPABP-Cl, они наблюдали быстрые, в миллисекундном диапазоне, подъёмы флуоресценции по мере того, как рапамицин вызывал приближение и перестройку этих белков. Увеличение яркости отражало более плотную микросреду вокруг красителя по мере сближения партнеров. В более сложном тесте они изучали SNAP25, белок нервного терминала, важный для высвобождения нейротрансмиттеров и являющийся основной мишенью ботулинического нейротоксина A. Размещая HaloTag по обе стороны от сайта расщепления токсином и маркируя красителем, они могли раздельно отслеживать движения N-концевого и C-концевого фрагментов после разрезания. Отслеживание отдельных частиц показало, что один фрагмент оставался закреплённым рядом с мембраной клетки, тогда как другой свободнее диффундировал по цитоплазме, и что точная картина зависела от того, была ли маркировка выполнена до или после воздействия токсина. Зонд даже фиксировал быстрые, индуцированные цинком конформационные подстройки SNAP25 в процессе.
Что это значит для биологии и медицины
В совокупности эти результаты демонстрируют, что BIOSCE — универсальный новый подход для визуализации того, как отдельные белки движутся, сворачиваются и взаимодействуют внутри живых клеток в широком диапазоне временных масштабов. Поскольку метод основан на общем фьюжне HaloTag и одном маломолекулярном красителе, его, по сути, можно применить к многим различным белкам без необходимости заново проектировать весь сенсор для каждого случая. Непрерывное, зависящее от ограничения изменение яркости позволяет исследователям обнаруживать тонкие структурные сдвиги, а не только крупные бинарные события. В будущем авторы планируют улучшить доставку зонда и глубину визуализации, чтобы BIOSCE можно было применять в тканях и целых организмах. Если эти планы реализуются, подход может стать мощным инструментом для связывания локализации белков, их движений и функций в здоровье и болезни и в конечном итоге будет полезен для детальных компьютерных моделей клеточного поведения.
Цитирование: Jia, H., Yang, L., Yang, Y. et al. Steric confinement-induced emission probe for monitoring protein conformations in live cells. Commun Chem 9, 109 (2026). https://doi.org/10.1038/s42004-026-01914-x
Ключевые слова: динамика конформаций белков, клеточное микроскопирование в живых клетках, флуоресцентные биосенсоры, зонды HaloTag, ботулотоксин