Clear Sky Science · ru
Прямая диазотизация индолов с помощью 2-метоксиэтилнитрита
Преобразование проблемного газа в полезную химию
Оксид азота часто рассматривают как неприятный промышленный газ: он токсичен, с ним трудно работать, и его обычно считают отходом. В то же время он богат азотом — ключевым элементом во многих лекарствах. В этом исследовании показано, как химики могут приручить оксид азота, превратив его в стабильный жидкий реагент, который, в свою очередь, помогает строить сложные молекулы, связанные с кандидатами в лекарства. Работа предлагает способ превратить опасный побочный продукт в инструмент для получения ценных соединений более безопасно и чисто.
Новый вспомогательный молекула для трудных реакций
Химики часто полагаются на «диазо» соединения — молекулы, несущие очень реактивную пару атомов азота — для построения сложных углеродных каркасов. Эти каркасы встречаются во многих фармацевтических препаратах, особенно в тех, что основаны на индолах — циклической системе, распространённой в натуральных продуктах и лекарствах. Традиционные способы получения диазо соединений часто используют взрывоопасные азиды или большие количества сильных кислот и оснований, что создаёт проблемы безопасности и для окружающей среды. Авторы сосредоточились на более безопасной альтернативе: жидкости под названием 2-метоксиэтилнитрит, или MOE-ONO, которую можно получить непосредственно из газа оксида азота, кислорода и простого спирта, образуя в качестве побочного продукта только воду.
Прямое преобразование важного похожего на лекарство кольца
Команда поставила задачу непосредственно прикрепить диазогруппы к индолам, модифицируя их в точном положении на кольце без жёстких условий. Они обнаружили, что комбинация MOE-ONO с распространённым органическим радикалом TEMPO и небольшим количеством солей металла на основе скандия эффективно запускает эту трансформацию. По сравнению с классическими смесями нитрита натрия и кислоты или с другими жидкими донорами оксида азота, такими как трет-бутилнитрит, новая комбинация даёт более высокие выходы, намного меньше побочных продуктов и работает за гораздо более короткое время. Даже индолы, которые сопротивлялись старым методам — например, содержащие объёмные фенильные группы — удалось чисто превратить с помощью этого подхода.
Один метод, много строительных блоков
После оптимизации реакции исследователи проверили её универсальность. Они обнаружили, что широкий набор производных индола выдерживает условия, в том числе молекулы с эфирами, кетонами, амидами и различными заместителями по кольцу — от электронно-щедрых алкильных и метоксигрупп до галогенов и цианогрупп. Метод также распространился за пределы индолов на родственные нафтоловые соединения, формируя диазопроизводные, для получения которых ранее требовались более длительные многоступенчатые процедуры. Примечательно, что реакция работала и в воде, хотя исходные вещества плохо в ней растворяются. Такое «на-воде» поведение указывает на то, что простое перемешивание в воде обеспечивает более зелёную среду, которая помогает реакции протекать, снижая зависимость от органических растворителей.
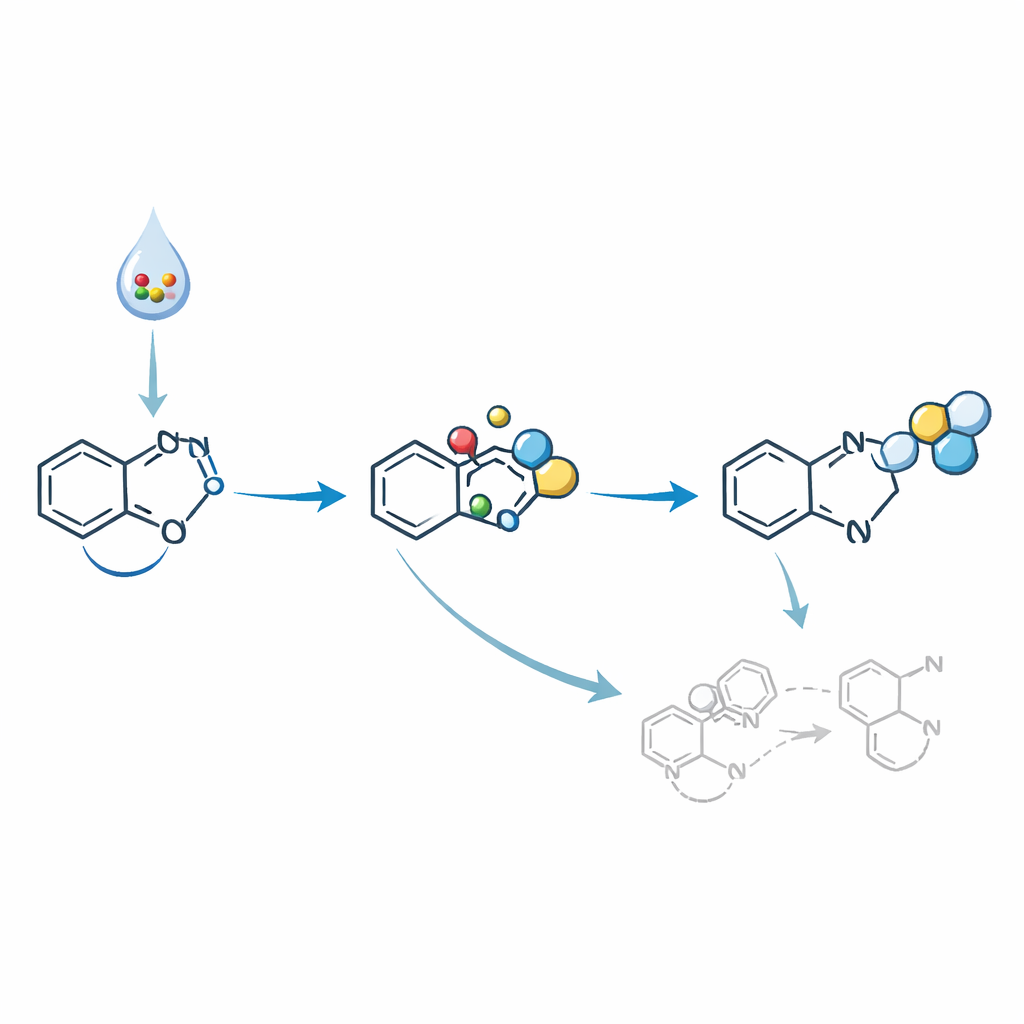
От реактивных интермедиатов к кандидатам в лекарства
Чтобы показать ценность этих диазоиндолов, авторы далее преобразовали их в более сложные молекулы. С помощью родиевого катализатора они превратили диазогруппу в высокореактивный интермедиат — карбен, который затем образовывал новые связи для построения циклопропановых колец в определённых позициях индола. В другой последовательности они собрали кандидат на модулятор рецептора, вовлечённого в контроль уровня сахара в крови, демонстрируя актуальность метода для медицинской химии. Они также показали, что реактивы Гриньяра — классические инструменты для присоединения углерода — могут селективно присоединяться в одну позицию диазоиндола, оставляя диазогруппу нетронутой, что открывает путь к пошаговому построению плотно заместительных структур индолов и индолинов.
Почему реакция идёт в нужном направлении
За кулисами несколько конкурирующих путей могли бы привести к нежелательным нитро- или оксимным продуктам вместо целевых диазо соединений. Механистические эксперименты указывают на то, что TEMPO помогает направлять химию, улавливая вредные радикалы и захватывая мимолётный нитрозный интермедиат прежде, чем тот успеет реаранжироваться. Дополнительные молекулы оксида азота затем присоединяются последовательно, в конечном счёте образуя диазогруппу и выделяя безвредную нитратную соль. Соль скандия, по-видимому, способствует распаду MOE-ONO на реактивные виды и активирует индольное ядро, дополнительно повышая эффективность. Обнаружение нитрата в конечной смеси поддерживает предлагаемую схему от донора оксида азота к диазопродукту.
Безопасный и устойчивый путь к сложным молекулам
В целом эта работа представляет практичный способ установки очень полезных диазогрупп на индольные кольца без использования взрывоопасных реагентов или жёстких условий. Используя стабильную жидкость, полученную из газа оксида азота, метод одновременно «апсайклирует» проблемную промышленную эмиссию и упрощает доступ к сложным лекароподобным молекулам. Для неспециалистов ключевая мысль такова: грамотная химия может превратить токсичный отходный газ в универсальный строительный блок для будущих лекарств, сокращая при этом воздействие на окружающую среду.
Цитирование: Hashidoko, A., Kitanosono, T., Nakao, Y. et al. Direct diazotization of indoles with 2-Methoxyethyl nitrite. Commun Chem 9, 104 (2026). https://doi.org/10.1038/s42004-026-01910-1
Ключевые слова: переработка оксида азота, диазоиндолы, зелёный органический синтез, лекарства на основе индола, донорные реагенты NO