Clear Sky Science · ru
Золото-содержащие полимерные наночастицы с покрытием ионной жидкостью для селективного «попутного» транспорта нейтрофилами при лечении эндометриоза
Переосмысление облегчения при распространённом скрытом заболевании
Эндометриоз — болезненное состояние, при котором ткань, схожая с маточной слизистой, разрастается там, где ей не место, часто вызывая сильные спазмы, хроническую боль и проблемы с фертильностью. Современные методы лечения в основном опираются на гормоны или хирургию, что может сопровождаться побочными эффектами, повторными вмешательствами и отсутствием гарантии длительного облегчения. В этом исследовании рассматривается принципиально иная идея: крошечные частицы, активируемые светом, которые «садятся» на собственные клетки иммунной системы организма, чтобы найти и аккуратно разрушить поражённую ткань — потенциально предлагая в будущем нехирургический вариант, сохраняющий фертильность и уменьшающий побочные эффекты.
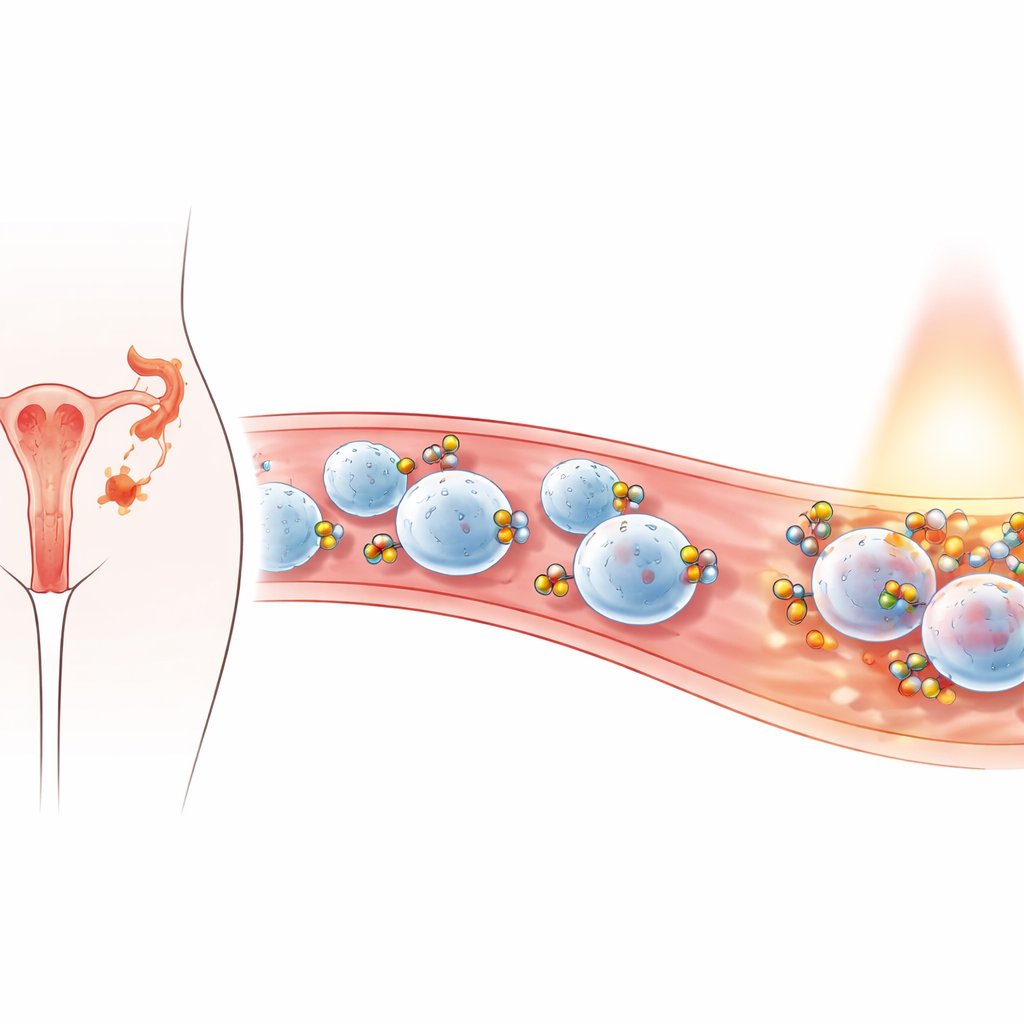
Малые помощники на первом фронте защиты организма
Исследователи сосредоточились на нейтрофилах — типе лейкоцитов, которые быстро стягиваются к очагам воспаления, включая очаги эндометриоза. Их стратегия — «попутать» наночастицы с этими клетками, покрывая частицы так, чтобы нейтрофилы естественным образом захватывали их или несли на своей поверхности. Когда нейтрофилы мигрируют к воспалённой эндометриальной ткани, они приносят наночастицы с собой, концентрируя лечение там, где это наиболее необходимо, и щадя здоровые участки. Важно, что в здоровых тазовых тканях движение нейтрофилов обычно невелико в течение большей части менструального цикла, что может помочь сосредоточить терапию на поражённых зонах, а не на нормальной ткани.
Создание умных наночастиц, реагирующих на свет
Чтобы система работала, команда собрала частицы с тремя ключевыми компонентами. В центре — золото, выбранное за способность поглощать ближний инфракрасный свет и превращать его в тепло контролируемым образом. Вокруг золотого центра они нанесли оболочку из биоразлагаемого полимера PLGA, широко применяемого в медицинских имплантатах и доставке лекарств. Наконец, они покрыли эту оболочку особыми «ионными жидкостями» — солеобразными, маслоподобными молекулами, остающимися жидкими при относительно низких температурах. Тщательно подобрав ионные жидкости, исследователи сумели настроить взаимодействие частиц с клетками крови, особенно с нейтрофилами. Микроскопия и измерения размера подтвердили образование аккуратной «сердцевина‑оболочка», а оптические тесты показали, что покрытия смещают светопоглощение частиц таким образом, что улучшают их нагревательные свойства.
Нагрев поражённых клеток без жёстких лекарств
После разработки стабильной конструкции частицы проверили на человеческих эндометриальных клетках в лаборатории. Когда растворы с частицами облучали ближним инфракрасным светом — аналогичным тому, что может давать медицинский лазер — общая температура повышалась лишь на несколько градусов, тем не менее этого было достаточно, чтобы повредить окружающие клетки. Важно, что без света частицы были по сути безвредны: при контакте с ними жизнеспособность эндометриальных клеток оставалась более 80% в широком диапазоне доз. Под действием света клетки в основном проходили апоптоз — упорядоченную, запрограммированную форму гибели — а не некроз, который может вызвать воспаление. Дополнительные тесты не выявили значительных повреждений ДНК и не показали выброса воспалительных сигнальных молекул из обработанных клеток.
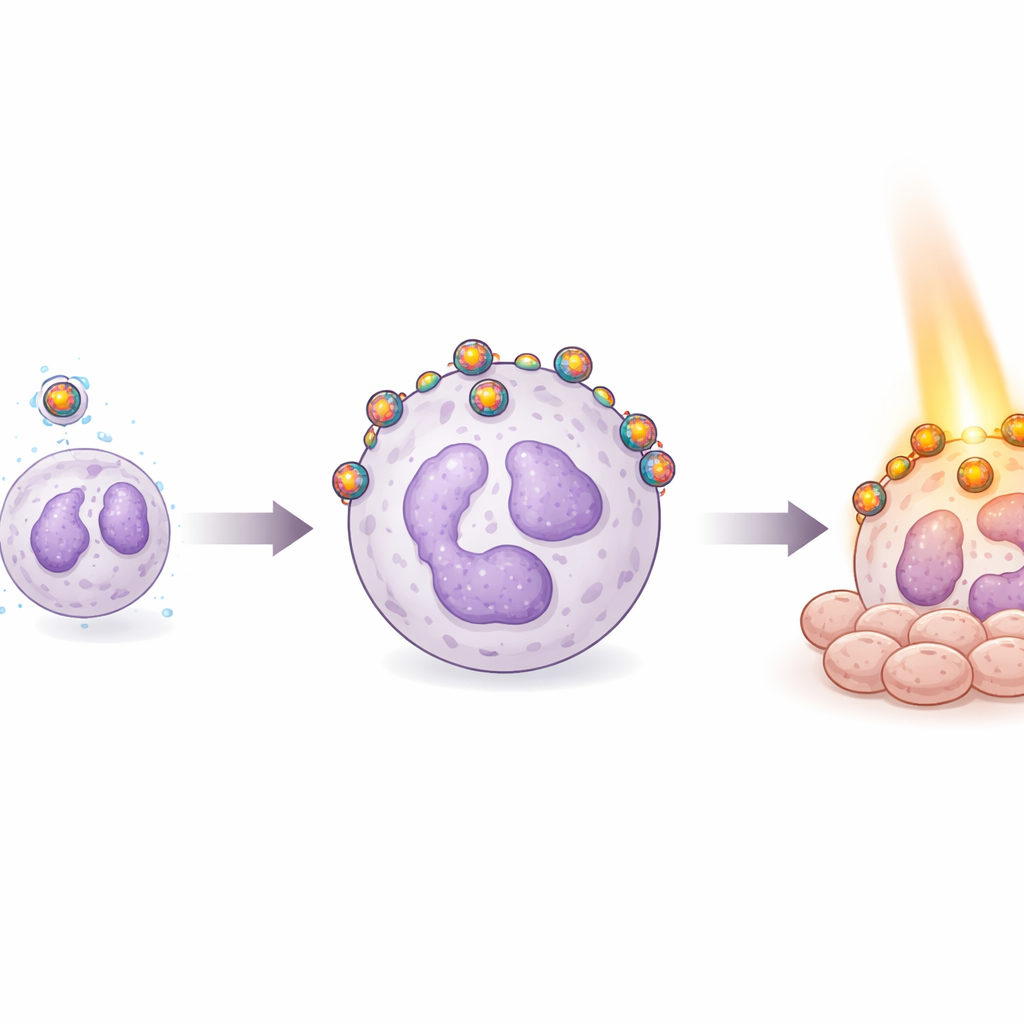
Доказательство безопасности в крови и отслеживание «поездки»
Безопасность в кровотоке жизненно важна для любой внутривенной терапии. Команда подвергала человеческие эритроциты воздействию наночастиц и обнаружила практически отсутствие гемолиза — разрушения красных клеток, что может привести к серьёзным осложнениям — что предполагает, что частицы бережно относятся к крови. Затем они добавили флуоресцентный краситель к частицам и смешали их с образцами человеческой крови, чтобы проследить, каким клеткам частицы предпочитают. По сравнению с непокрытыми частицами версии с покрытием ионной жидкостью показали значительно более сильную ассоциацию с нейтрофилами. Некоторые покрытия поощряли фагоцитоз частиц нейтрофилами, тогда как другие заставляли частицы прилипать к поверхности клетки, как бусинки снаружи шара. Оба типа ассоциации увеличивали количество золота, обнаруженное в нейтрофилах, подтверждая, что покрытия успешно направляют наночастицы на естественных «курьеров» воспаления организма.
Что это может значить для будущего лечения
В целом исследование представляет новый тип «умных» наночастиц, спроектированных для транспортировки нейтрофилами, безопасной циркуляции в крови и, при активации мягким лазерным светом, нагрева и уничтожения эндометриальных клеток преимущественно через контролируемые пути программируемой гибели. Хотя эти эксперименты проведены на клетках и образцах крови, а не на живых пациентах, результаты указывают на возможное будущее, когда очаги эндометриоза можно будет лечить изнутри без масштабной хирургии или интенсивной гормональной терапии. Сочетая таргетированную доставку с точным контролем нагрева светом, этот подход однажды может обеспечить более длительное облегчение, меньше побочных эффектов и лучшее сохранение фертильности для людей, живущих с эндометриозом.
Цитирование: Vashisth, P., Clerc, L.T.D., Hu, D. et al. Ionic liquid-coated gold core polymeric nanoparticles for selective neutrophil hitchhiking towards endometriosis treatment. Commun Chem 9, 119 (2026). https://doi.org/10.1038/s42004-026-01909-8
Ключевые слова: эндометриоз, наночастицы, фототермальная терапия, нейтрофилы, таргетная доставка лекарств