Clear Sky Science · ru
Минимизированное потребление образцов для временной серийной кристаллографии, примененной к редокс‑циклу человеческой NQO1
Наблюдая ферменты в деле с меньшим расходом ценных образцов
Современная биология часто полагается на мощные рентгеновские лазеры, чтобы увидеть, как молекулы жизни двигаются и меняют форму, однако такие эксперименты обычно требуют огромных количеств тщательно приготовленного белка. В этом исследовании предложен новый способ «подачи» крошечных белковых кристаллов в рентгеновский свободно‑электронный лазер гораздо более эффективно, что сокращает необходимый материал до 97%. Также показано, что этот более экономный метод всё равно способен фиксировать ранние этапы активности медицински значимого человеческого фермента, открывая путь к более регулярным «кино» белков в действии. 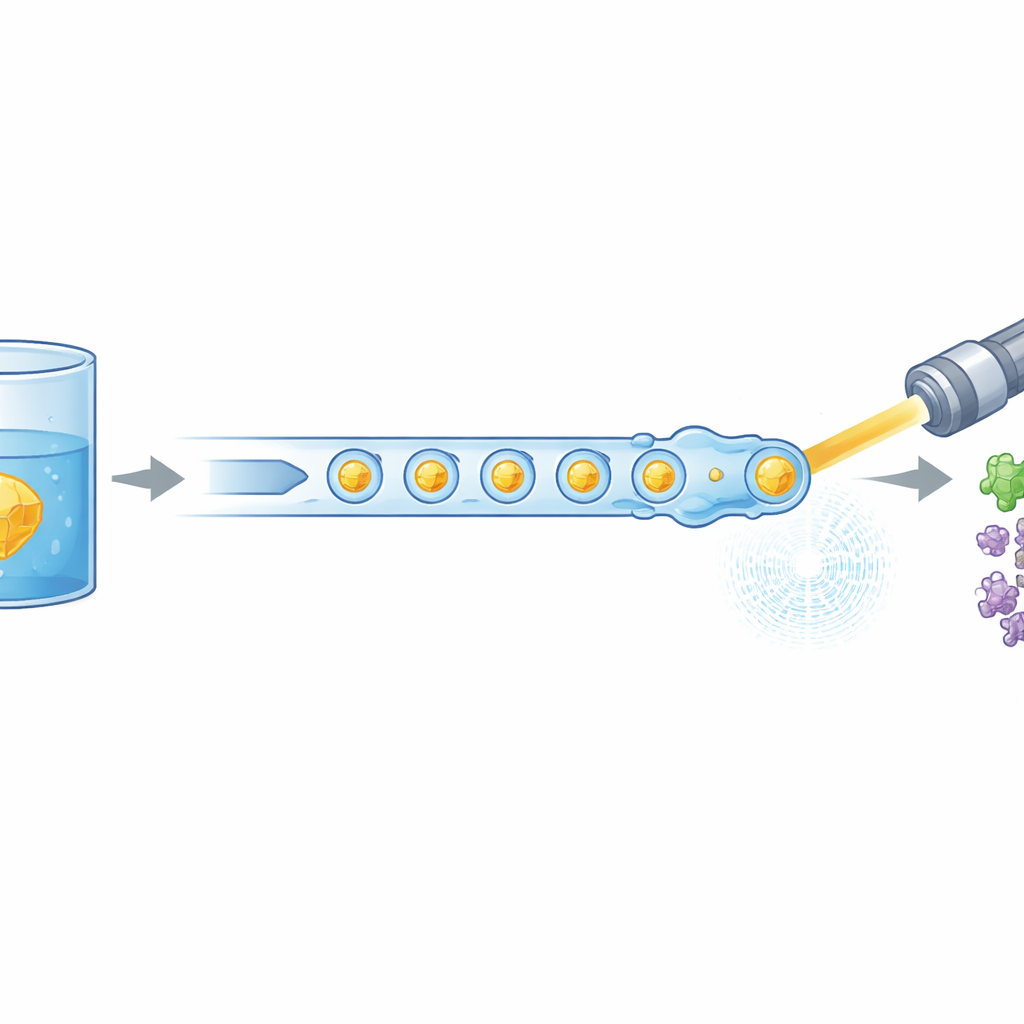
Почему съемка молекулярных «фильмов» так дорога
Чтобы понять, как белки действительно выполняют свои функции, учёные всё чаще переходят от статичных снимков к покадровым «фильмам», отслеживающим реакции в реальном времени. Один из ведущих подходов — временная серийная кристаллография — распыляет миллионы микроскопических кристаллов белка через сверхяркий рентгеновский луч. Каждый кристалл поражается однократно, что даёт снимок без повреждений, и тысячи таких изображений объединяются в полную картину. Загвоздка в том, что каждый момент реакции — десятая доля секунды, целая секунда и т. д. — требует новой порции кристаллов. Поскольку подготовка белка может быть медленной и дорогой, расход образца стал серьёзным узким местом, особенно в передовых центрах вроде European XFEL, где рентгеновские импульсы приходят короткими поездами с мегагерцовыми частотами.
Новый способ доставки крошечных капель по команде
Исследователи решили эту проблему, переработав способ доставки кристаллов в рентгеновский луч. Вместо непрерывного жидкостного потока они генерируют тщательно разнесённый ряд микроскопических капель, каждая из которых содержит кристаллы белка, разделённые масляной фазой. Миниатюрное 3D‑печатаемое устройство объединяет два потока — кристаллы белка и растворённый реагент — в крошечные смешанные объёмы, которые затем отщепляются в виде капель. Эти капли направляются через газо‑фокусированное сопло, формирующее узкую струю, совместимую с вакуумом и скоростью XFEL. Критично, что производство капель электрически синхронизировано со структурой рентгеновских пачек, так что почти каждый полезный импульс попадает в каплю, а не в пустую жидкость. 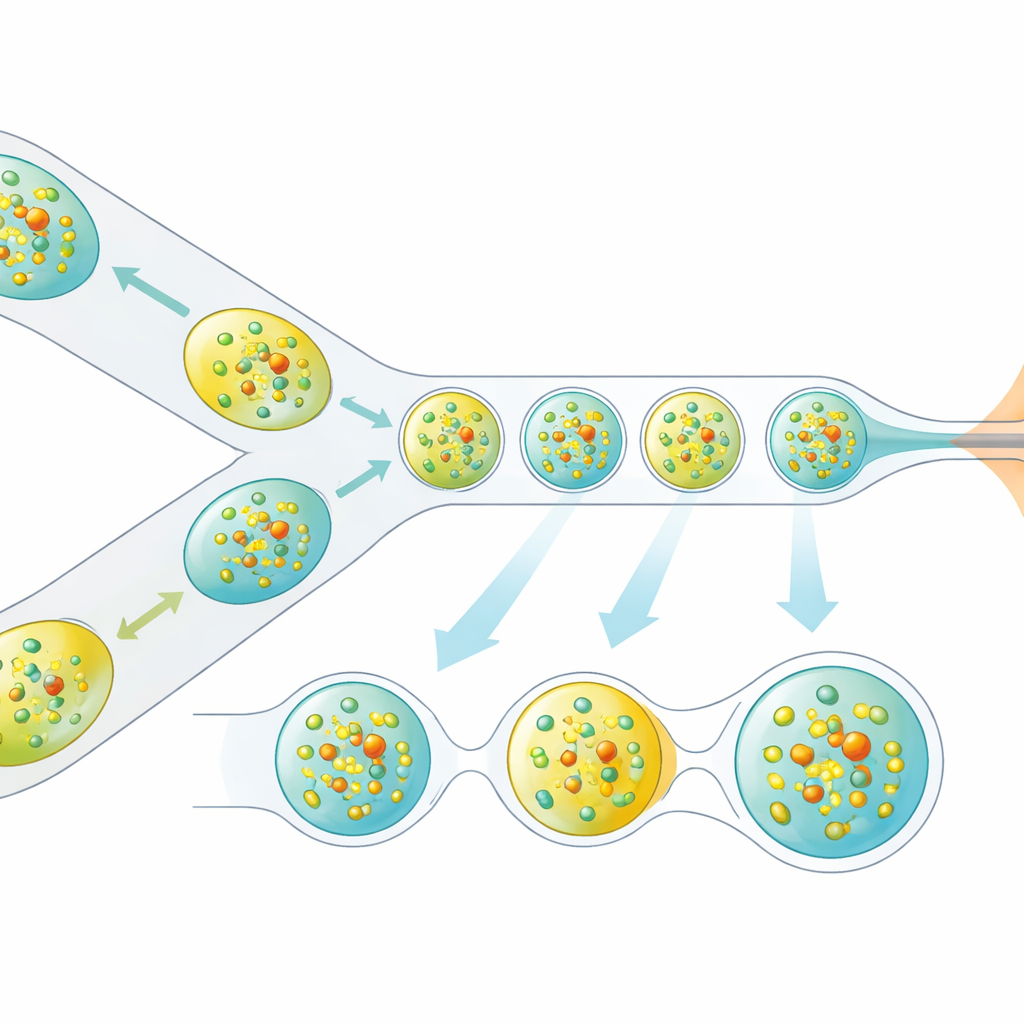
Тест метода на человеческом ферменте
Чтобы доказать применимость капельного подхода к реальным биологическим задачам, команда изучила NAD(P)H:хинонокислородоредуктазу 1 (NQO1), человеческий фермент, участвующий в поддержании редокс‑баланса клетки и связанный с заболеваниями. Они смешали микрокристаллы NQO1 с его природным кофактором NADH и исследовали систему в двух ранних временных точках: 0,3 с и 1,2 с после смешивания. Анализируя полученные дифракционные картины, они реконструировали трёхмерные структуры фермента для каждого запаздывания. Несмотря на использование значительно меньшего количества белка по сравнению с традиционными экспериментами с непрерывным потоком, качество данных позволило выявить тонкие особенности электронной плотности в активных сайтах фермента, что согласуется с начальным связыванием молекул NADH при низкой заполненности.
Что показывают ранние структурные кадры
Структуры показывают, что вскоре после смешивания не все активные сайты в кристалле ведут себя одинаково. При 0,3 с признаки NADH чётко видны в трёх из четырёх активных сайтов в элементарной ячейке и часто в более чем одной конформации, что указывает на то, что кофактор исследует несколько позиций прежде, чем закрепиться. К 1,2 с некоторые из этих особенностей сужаются в доминирующий режим связывания, но общая картина остаётся гибкой и лишь частично заполненной. Такое неоднородное, меняющееся поведение согласуется с более ранними биохимическими данными о том, что два субъединичных партнёра в димере NQO1 не действуют полностью синхронно, а демонстрируют «активность половины сайтов», при которой одна сторона пары включается первой, а другая отстаёт. Временные структурные данные таким образом дают раннее представление о том, как это асимметричное поведение проявляется в реальном пространстве.
Экономия образцов при сохранении науки
С практической точки зрения метод сегментированных капель сократил расход белка примерно в шесть раз для измерений при 0,3 с и до 97% для экспериментов при 1,2 с по сравнению с традиционными непрерывными струями при сопоставимых условиях. При этом метод по‑прежнему обеспечивал надёжную структурную информацию при комнатной температуре и был совместим со строгой структурой импульсов European XFEL. Для неспециалистов главный вывод таков: исследователи теперь могут наблюдать, как ферменты вроде NQO1 начинают свою работу в почти реальном времени, потребляя при этом лишь миллиграммы ценного образца на каждую временную точку. Это делает гораздо более реалистичным обследование множества времён реакции и разных белков, что в конечном счёте поможет раскрыть, как важные для медицины ферменты движутся, сгибаются и взаимодействуют, выполняя химию жизни.
Цитирование: Doppler, D., Grieco, A., Koh, D. et al. Minimized sample consumption for time-resolved serial crystallography applied to the redox cycle of human NQO1. Commun Chem 9, 107 (2026). https://doi.org/10.1038/s42004-026-01908-9
Ключевые слова: серийная кристаллография, свободно‑электронный рентгеновский лазер, микрофлюидика капель, динамика ферментов, NQO1