Clear Sky Science · ru
Онкогенные варианты PI3Kα выявляют градуированный спектр конформаций с мутационно-специфическими скрытыми карманами
Когда одной замены в ДНК недостаточно
Рак часто описывают как болезнь мутаций, но это исследование показывает, что не все мутации действуют в одиночку. Авторы изучили ключевой фермент, контролирующий рост — PI3Kα — и обнаружили, что две определённые замены в ДНК, происходящие вместе в одной копии гена, могут сдвинуть белок в более активные конформации, чем любая из этих замен по отдельности. Это важно, потому что гиперактивный PI3Kα не только стимулирует развитие рака, но также участвует в доброкачественных синдромах гиперроста и расстройствах развития мозга — и помогает объяснить, почему некоторые опухоли плохо реагируют на существующие препараты.
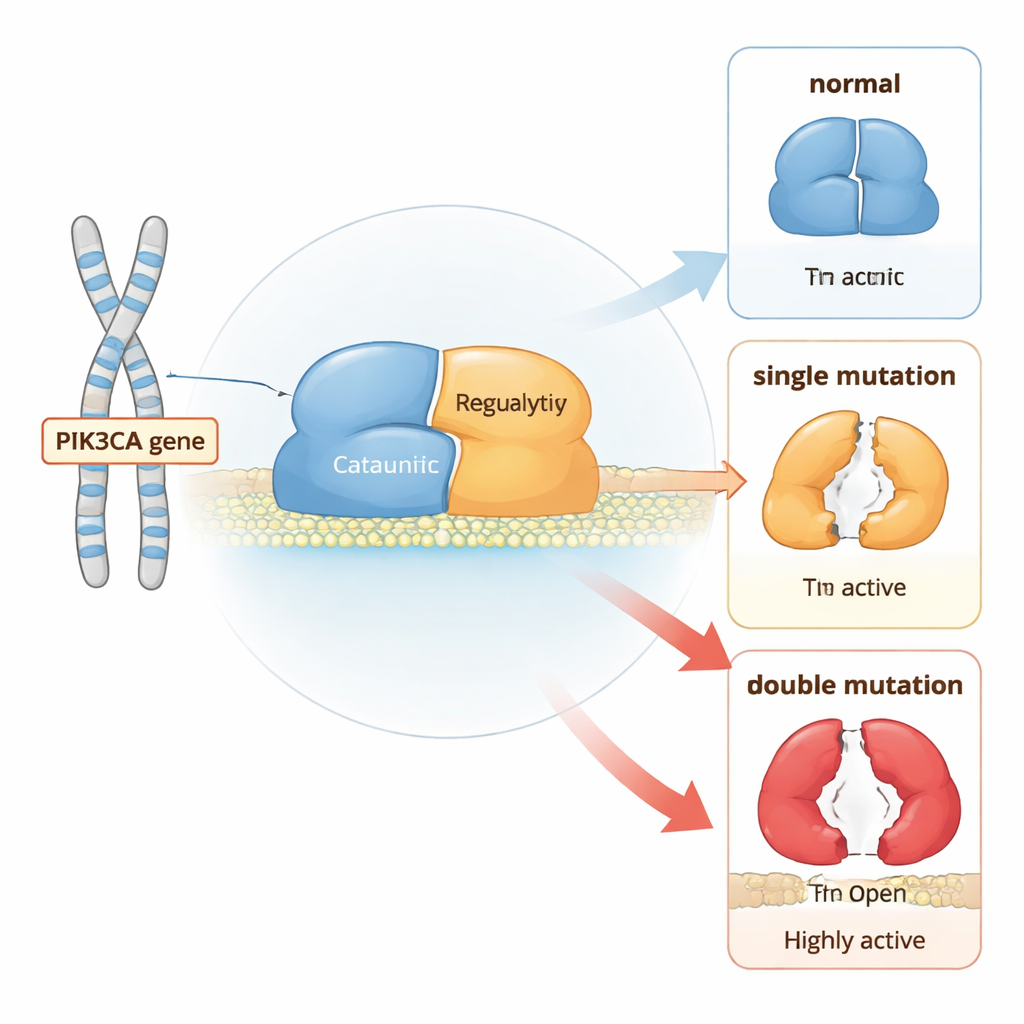
Молекулярный переключатель клеточного роста
PI3Kα — это белок из двух частей, находящийся у мембраны клетки и передающий сигналы роста. В норме он преимущественно находится в «выключенном» состоянии до тех пор, пока рецепторы на поверхности клетки не будут активированы. Затем PI3Kα перемещается к мембране и превращает липид PIP2 в PIP3, который сигнализирует клетке о росте и делении. Чтобы предотвратить неконтролируемый рост, в белке есть несколько встроенных «тормозов»: одна область зажимает каталитическое ядро, другая удерживает гибкую петлю активации близко, а партнёрная субъединица помогает сдерживать весь комплекс.
Как одиночные и двойные мутации сдвигают равновесие
С помощью длительных атомистических компьютерных симуляций авторы сравнили нормальный PI3Kα с вариантами, несущими либо одиночные «горячие» онкогенные мутации, либо комбинации горячей мутации с более слабой в той же молекуле. Они обнаружили, что каждая мутация изменяет частоту появления более открытых, активных конформаций, но двойные мутации смещают это равновесие значительно дальше, чем одиночные. В частности, некоторые пары мутаций работают совместно, ослабляя контакты, удерживающие регуляторный фрагмент (называемый nSH2), и сдвигая другой сегмент (iSH2) от его места докинга. Такая скоординированная подвижность отпирает каталитическое ядро, облегчая переход белка к мембране и запуск сигналинга.
Помощь субстрату на пути к реакционному центру
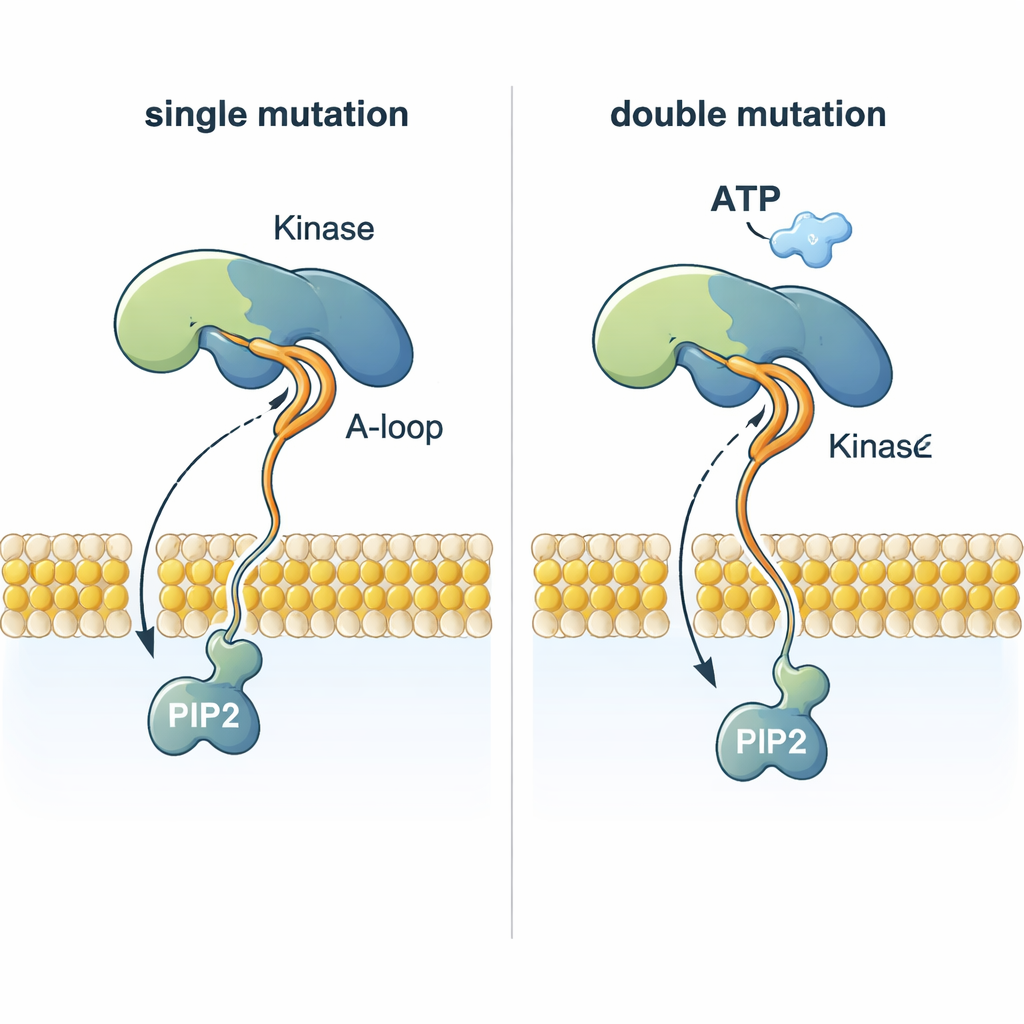
Одна из загадок — как PI3Kα переносит фосфат от ATP, находящегося почти на 2 нанометра выше мембраны, на PIP2, встроенный в мембрану. Симуляции показывают, что определённые мутации перестраивают гибкую петлю активации так, что сильно положительно заряженный участок выпрямляется и тянется к мембране. Эта петля может захватить отрицательно заряженную головку PIP2, вытащить её из липидного слоя и направить вверх к ATP. Двойные мутанты, объединяющие мутацию, закрепляющую белок у мембраны, с мутацией, меняющей эту петлю, координируют захват PIP2 значительно эффективнее по сравнению с нормальным PI3Kα или одиночными мутантами, что даёт структурное объяснение тому, почему опухоли с двумя мутациями PI3Kα могут быть особенно агрессивными.
Скрытые сайты для препаратов, выявляемые движением
Поскольку PI3Kα велик и гибок, препарат, направленный только на активный центр, часто с трудом действует на все мутантные формы и может вызывать побочные эффекты, например серьёзные нарушения сахарного обмена. Наблюдая, как белок «дышит» и изгибается со временем, исследователи обнаружили «криптические» карманы — временные борозды, которые открываются лишь в определённых мутантных конформациях и невидимы в статических кристаллических структурах. Эти карманы появляются в мутационно-специфичных местах, например рядом с регионами, которые наиболее сильно смещаются в конкретных двойных мутантах. Это указывает на то, что тщательно спроектированные аллостерические препараты, связывающиеся вне активного центра, можно адаптировать, чтобы «запереть» отдельные мутантные варианты в более безопасных, менее активных конформациях.
К более разумным комбинированным лечениям
В целом работа поддерживает представление о «двойном ударе» в генетике рака: сильная горячая мутация плюс более слабый партнёр в той же молекуле PI3Kα могут создавать градуированный спектр более активных конформаций, часто связанный с более тяжёлыми клиническими исходами. Для терапии авторы утверждают, что вместо опоры на один ингибитор эффективнее сочетать препараты, нацеленные на разные карманы — один в активном центре и один или несколько аллостерических сайтов, которые существуют только в специфичных мутациях. Такие коктейли могли бы, по сути, точнее снизить активность PI3Kα, уменьшить токсические побочные эффекты и лучше согласовать лечение с точным паттерном мутаций в опухоли пациента.
Цитирование: Jang, H., Yavuz, B.R., Zhang, M. et al. Oncogenic PI3Kα variants reveal graded conformational spectrum with mutation-specific cryptic pockets. Commun Chem 9, 100 (2026). https://doi.org/10.1038/s42004-026-01906-x
Ключевые слова: PI3K альфа, онкогенные мутации, аллостерические ингибиторы, молекулярная динамика, сигнальная трансдукция