Clear Sky Science · ru
Динамика фотоокисления CO до CO2 на рутиле (110)
Почему важно наблюдать молекулы за триллионную долю секунды
Современная жизнь опирается на химические реакции, которые очищают наш воздух и воду и преобразуют солнечный свет в полезную энергию. Многие из этих реакций происходят на поверхностях твердых материалов — фотокатализаторов, которые приводятся в действие светом. В этом исследовании рассматривается одна из таких реакций — превращение ядовитого оксида углерода (CO) в углекислый газ (CO2) на поверхности диоксида титана — на шкалах времени в считанные квадриллионные доли секунды. Понимание этих ультрабыстрых стадий поможет ученым разрабатывать более продуманные материалы для борьбы с загрязнением, самоочищающиеся покрытия и солнечные энергетические технологии.
Светозапускная бригада по очистке
Диоксид титана — универсальный материал, который используется в самоочищающихся окнах, покрытиях для очистки воздуха и экспериментальных устройствах для получения солнечных топлив. Он дешев, стабилен и может использовать свет, чтобы запускать мощные очищающие реакции на своей поверхности. Но не все формы диоксида титана ведут себя одинаково. Две распространенные формы — анатаз и рутил — различаются по эффективности в реакциях, таких как превращение CO в CO2. Хотя анатаз обычно более активен в целом, детальная временная картина отдельных этапов реакции — особенно того, как активируется кислород из воздуха — оставалась неясной. Это исследование сосредоточено на форме рутил с определенной ориентацией поверхности, обозначаемой как (110), чтобы выяснить, как быстро окисляется CO после воздействия света.
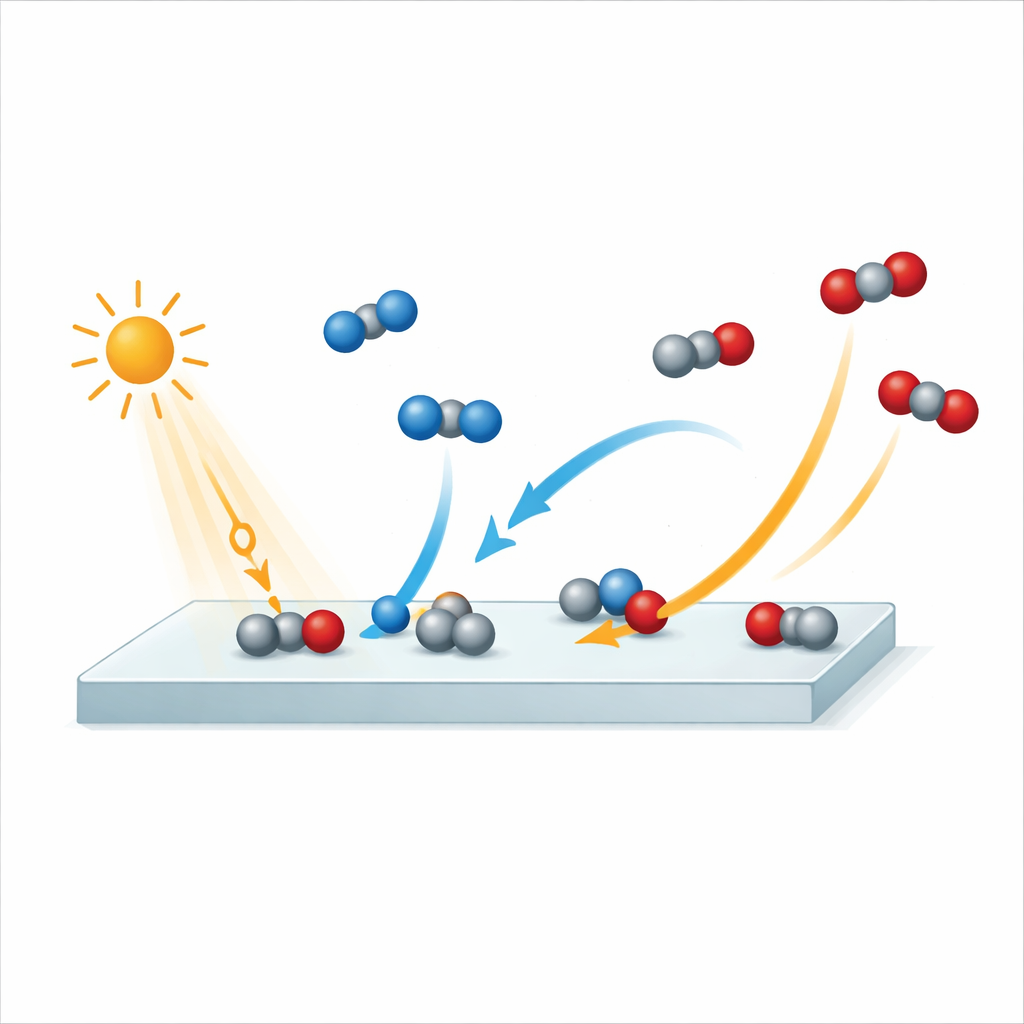
Съемка реакции на экстремальной скорости
Для захвата этого процесса исследователи использовали источник свободных электронов в Гамбурге, который генерирует исключительно короткие вспышки рентгеновского излучения. Сначала они облучали поверхность рутила импульсом инфракрасного света, выполняющим роль крошечной «вспышки», запускающей реакцию. Тщательно синхронизированный рентгеновский импульс затем зондировал, как изменяются атомы и электроны на поверхности. Повторяя эту последовательность с разными задержками между световым и рентгеновским импульсами, они собрали своего рода «молекулярный фильм» реакции с временным разрешением около 250 фемтосекунд — одна фемтосекунда равна миллионной доле миллиардной доли секунды. Команда отслеживала сигналы от атомов кислорода в поверхности и в газовой фазе, что позволяло отличать CO, CO2, воду и сам оксид по мере развития реакции.
Фиксация CO2 менее чем за триллионную долю секунды
Ключевое наблюдение состоит в том, что новый CO2 появляется на поверхности рутила уже через 200–800 фемтосекунд после светового импульса. Это означает, что кислород из соседних молекул O2 активируется, связи разрываются, и CO превращается в CO2 за меньшее время, чем одна триллионная доля секунды. Примерно через 0,8 пикосекунды свежий сигнал CO2 ослабляетcя по мере десорбции продукта с поверхности. Примечательно, что вся эта последовательность происходит быстрее на рутиле, чем на анатазе, где ранние исследования обнаруживали появление первого CO2 лишь через примерно 1,2–2,8 пикосекунд при прочих равных условиях. Хотя анатаз в целом производит больше CO2 и считается более сильным фотокатализатором, рутил выполняет ключевой этап окисления быстрее.
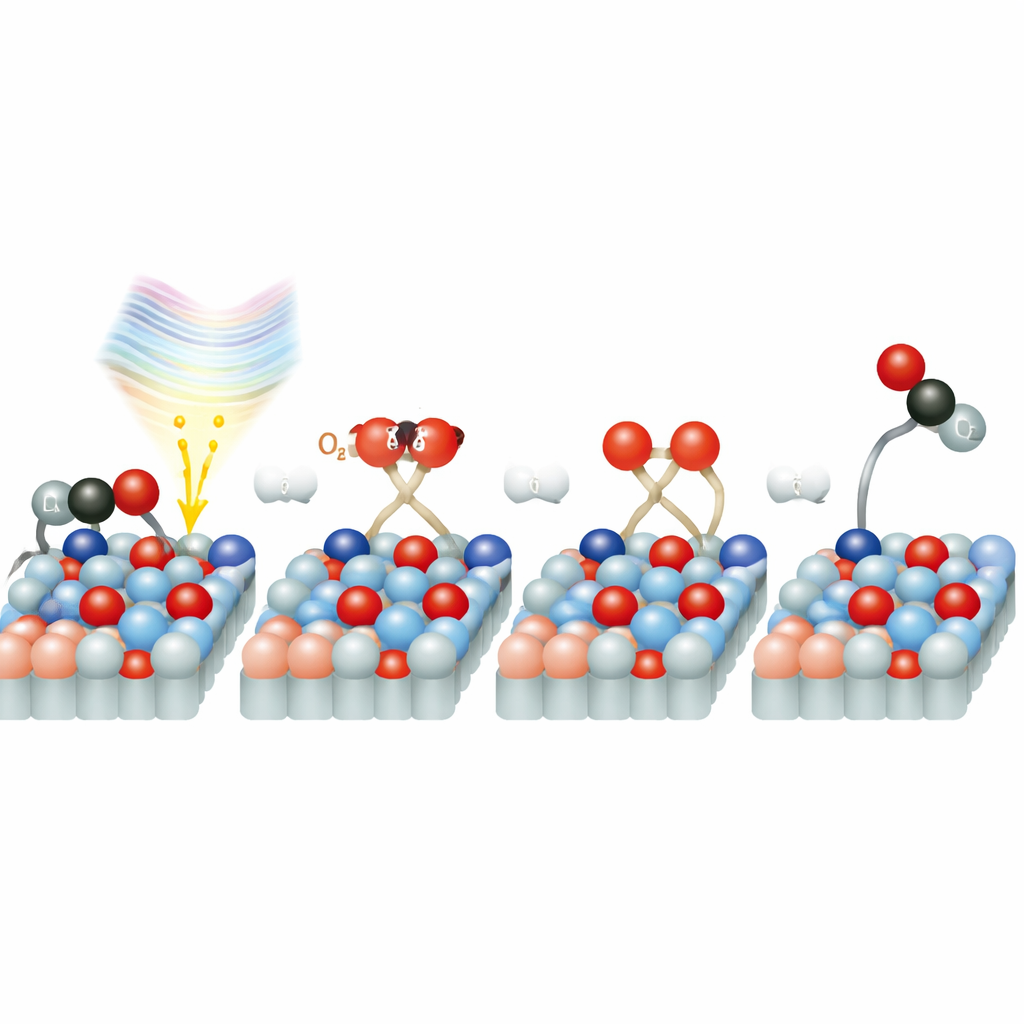
Короткая путь для кислорода
Почему реакция так быстра на рутиле? Подробные компьютерные моделирования указывают, что молекулы кислорода, адсорбированные на поверхности, создают особые электронные состояния, которые служат мостом между твердым телом и O2. При поглощении лазерного света с длиной волны 770 нм электрон может напрямую перейти из диоксида титана в молекулу кислорода, формируя заряженную, активированную форму кислорода. Этот «короткий путь» избегает более медленного маршрута, при котором электроны сначала перемещаются через объем твердого тела, а затем дрейфуют к поверхности. Как только кислород активирован, он быстро распадается, и один атом кислорода соединяется с CO, образуя CO2. Исследование также показывает, что следы воды на поверхности могут как блокировать реакционные участки, так и при низких концентрациях потенциально способствовать переносу заряда и активации кислорода, добавляя еще один уровень сложности.
Связь электронной структуры с реальной эффективностью
В целом работа демонстрирует, что крошечные детали в том, как электроны перетекают между поверхностью и соседними молекулами, могут существенно менять скорость реакции, даже между двумя близкородственными материалами. Хотя анатаз по-прежнему выигрывает по суммарной фотокаталитической отдаче, рутил показывает более быстрый этап активации кислорода, связанный с этим специальным маршрутом переноса заряда. Объединяя ультрабыстрые измерения и современные моделирования, исследование предоставляет дорожную карту для настройки поверхностей так, чтобы светозапускаемые реакции проходили эффективнее. В долгосрочной перспективе такие знания могут помочь инженерам разрабатывать лучшие покрытия для очистки воздуха, более эффективные антибактериальные поверхности и усовершенствованные материалы для солнечного получения топлива и разложения воды.
Цитирование: Gleissner, H., Wagstaffe, M., Wenthaus, L. et al. Dynamics of CO photooxidation to CO2 on rutile (110). Commun Chem 9, 127 (2026). https://doi.org/10.1038/s42004-026-01901-2
Ключевые слова: фотокатализ, диоксид титана, ультрабыстрая спектроскопия, химия поверхности, окисление угарного газа