Clear Sky Science · ru
Разработка квадрупльно-конъюгированной наномодели на основе углеродных точек для таргетной терапии глиомы
Новая надежда для упорных опухолей мозга
Опухоли мозга высокой степени злокачественности, такие как глиобластома, относятся к самым труднолечимым ракам. Многие препараты, эффективные в других частях тела, либо не могут преодолеть защитный гематоэнцефалический барьер, либо повреждают здоровую ткань по пути. В этом исследовании описана лабораторная «умная» наночастица, призванная точнее проникать в опухоли мозга, нести мощный коктейль лекарств и высвобождать его непосредственно внутри ядер опухолевых клеток, где воздействие на рак будет максимальным при минимальном вреде для нормальных клеток.
Крошечный грузовичок из углерода
В основе нового подхода лежат углеродные точки — наночастицы размером в нанометры, сделанные из углерода; они недороги в производстве, хорошо смешиваются с водой и светятся при определённом типе освещения. Их поверхности богаты химическими «крючками», что позволяет одновременно прикреплять разные биологические компоненты. В этой работе исследователи создали «квадрупльно-конъюгированную» наномодель: каждая углеродная точка была химически связана в одномодовой реакции с двумя различными пептидами-таргетами и двумя противоопухолевыми грузами. Такая модульная конструкция превращает каждую точку в крошечный грузовик, который распознаёт опухолевые клетки, проходит клеточные барьеры и доставляет препараты по нужному внутриклеточному адресу.
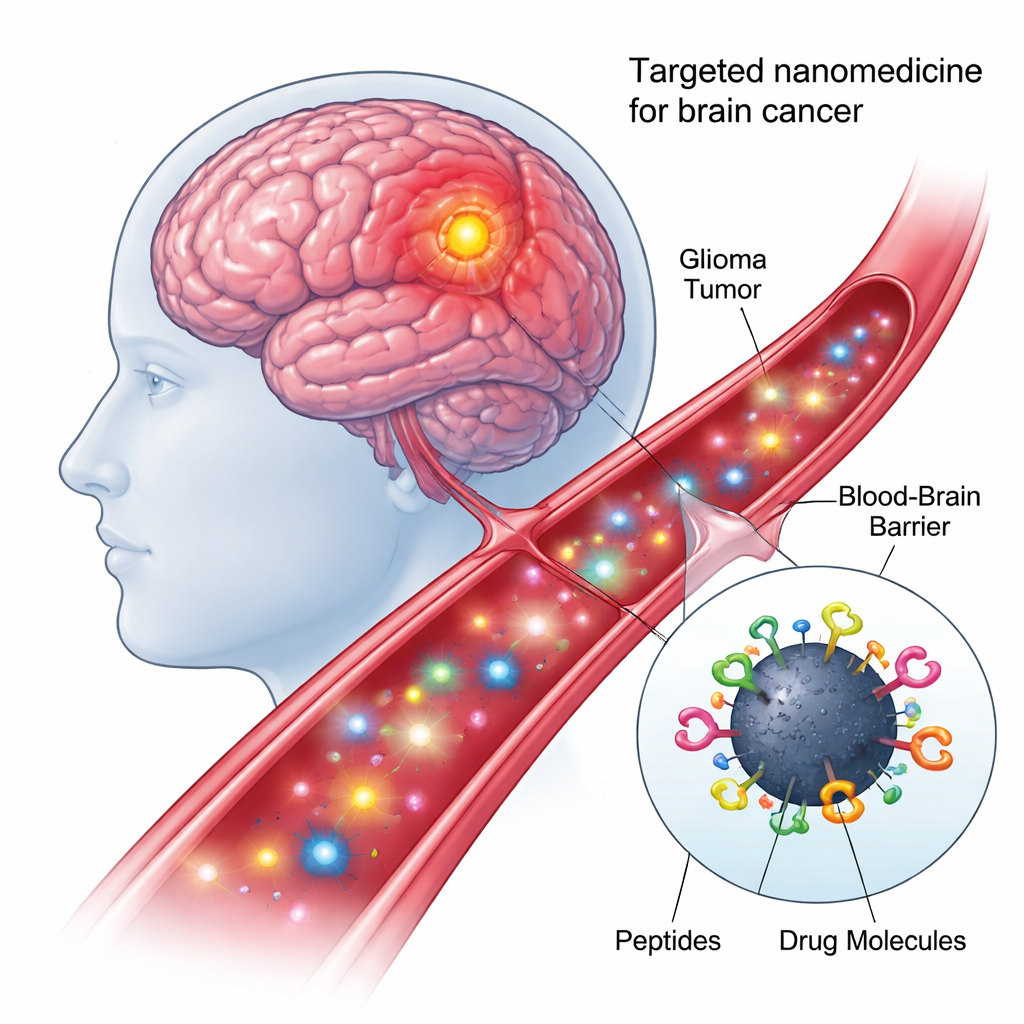
Поиск и проникновение в нужные клетки мозга
Первый пептид на наночастице, названный shPep-1, разработан для распознавания рецептора IL13Rα2. Этот рецептор обнаруживается в больших количествах во многих агрессивных опухолях мозга — включая взрослую и детскую глиобластому и диффузную интринсивную понтинную глиому — но практически не выражен в нормальных мозговых клетках. Связываясь с IL13Rα2, shPep-1 помогает углеродным точкам нацеливаться на опухолевые клетки и проникать в них посредством рецептор-опосредованного эндоцитоза. Второй, более длинный пептид lnPep-1, содержит сигнал ядерной локализации: короткую последовательность, помогающую грузу пройти через ядерную мембрану и достичь «контрольного центра» клетки, где хранится ДНК. Вместе эти два пептида обеспечивают наночастице и предпочтение к опухоли, и способность достигать ядра после попадания внутрь клетки.
Координированная атака препаратов
Терапевтический груз состоит из двух малых молекул. Первая — эпирубицин, хорошо известный химиотерапевтический препарат, который убивает раковые клетки, встраиваясь в ДНК и блокируя ферменты, необходимые для восстановления двухцепочечных разрывов. Вторая — метаболит 5-аминоимидазол-4-карбоксамид (AIC), образующийся из противоопухолевого препарата темозоломида при физиологическом pH. В предыдущих работах та же группа показала, что сочетание эпирубицина и AIC на углеродной точке усиливало гибель раковых клеток по сравнению с каждым препаратом по отдельности. В новой конструкции оба вещества совместно доставляются на наночастице с двумя пептидами, с целью добиться синергетического эффекта непосредственно в ядре опухолевой клетки.
Сильное действие в опухолевых клетках и более мягкое — в нормальных
Чтобы проверить эффективность наномодели, команда подвергла воздействию несколько линий клеток глиомы высокой степени — взрослую глиобластому, детскую глиобластому и модель диффузной интринсивной понтинной глиомы — квадрупльно-конъюгированными углеродными точками. Даже при очень низких концентрациях (всего 50 наномоляр) жизнеспособность опухолевых клеток падала примерно вдвое по сравнению с необработанными контролями, а при более высоких дозах все протестированные конъюгаты уничтожали большинство опухолевых клеток. Важно, что квадрупльная наномодель превосходила более простые «с одной пептидной» версии, хотя содержала в целом меньше эпирубицина. При тестировании на неконечных клетках сосудистых гладких мышц она была значительно менее токсична: для достижения схожего снижения жизнеспособности требовалось примерно в 25–40 раз больше наночастиц, что указывает на полезное окно безопасности, обусловленное таргетированием опухоли, а не грубым увеличением дозы.
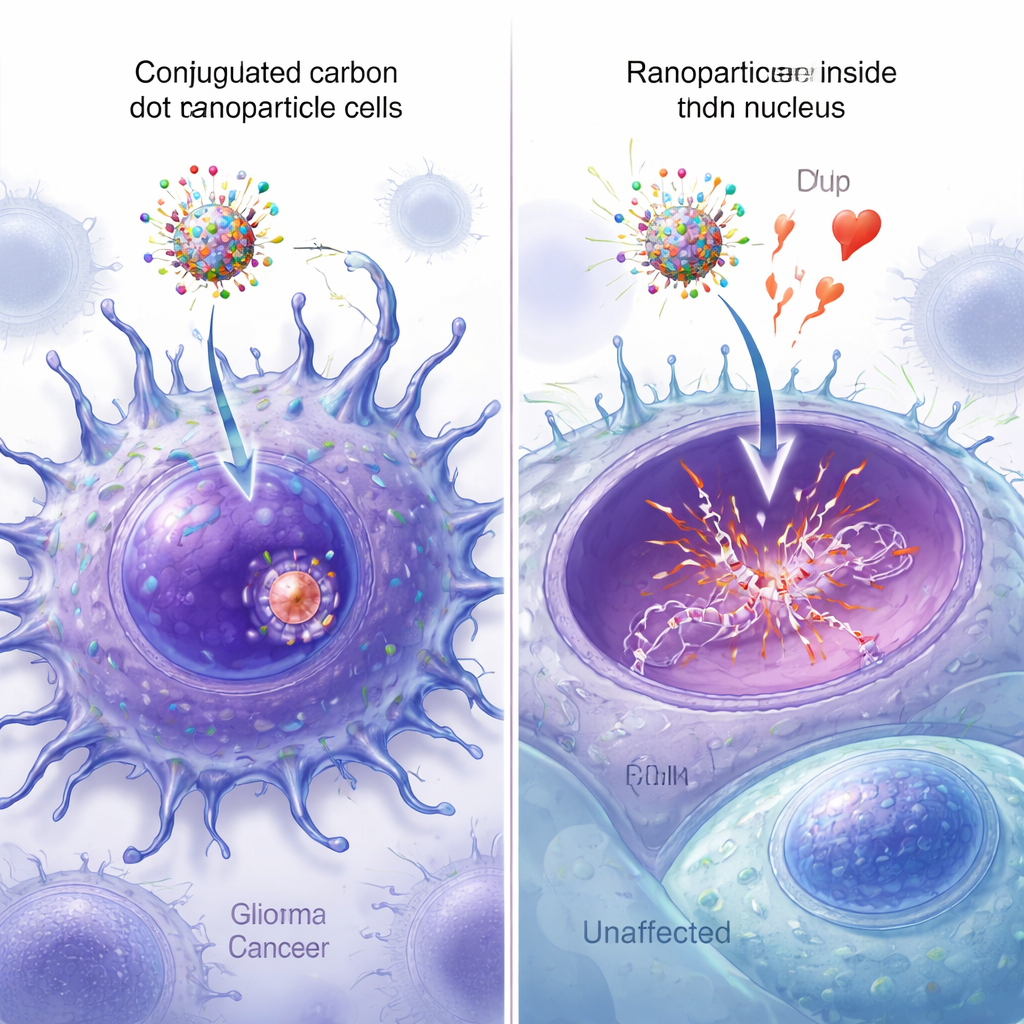
Визуализация проникновения наночастиц в ядро
Флуоресцентные версии наночастиц позволили исследователям наблюдать, насколько каждая конструкция проникает в клетки и достигает ядра. Под микроскопом углеродные точки, оснащённые обоими пептидами, давали самое яркое распределённое по раковым клеткам свечение, с сильным совпадением зелёной флуоресценции наночастиц и синего окрашивания ядер. Количественный анализ изображений подтвердил, что частицы с двумя пептидами имели наивысшую ядерную колокализацию, значительно превышая показатели частиц с одним пептидом или без пептидов. Дополнительные спектроскопические, масс-спектрометрические и измерения с помощью атомно-силовой микроскопии верифицировали, что все четыре компонента успешно прикреплены к углеродным точкам и умеренно увеличивают их размер, не нарушая ключевой способности эпирубицина связываться с ДНК.
Что это может значить для будущего лечения рака мозга
Для пациентов эти результаты пока остаются демонстрацией на клеточных линиях на ранней стадии, а не готовой терапией. Тем не менее они демонстрируют многообещающую концепцию: небольшую, стабильную и относительно простую в изготовлении углеродную наночастицу, которую быстро можно настроить с помощью пептидов-таргетов и комбинаций препаратов. Направляя препараты специфически в опухолевые клетки, сверхэкспрессирующие IL13Rα2, и концентрируя их в ядре, такие нанопрепараты потенциально позволят применять более низкие дозы, снижать побочные эффекты и развивать более персонализированные стратегии лечения для высоко летальных опухолей мозга, таких как глиобластома и диффузная интринсивная понтинная глиома.
Цитирование: Cilingir, E.K., Hettiarachchi, S.D., Rathee, P. et al. Development of a quadruple-conjugated carbon dot nanomodel for targeted glioma therapy. Commun Chem 9, 96 (2026). https://doi.org/10.1038/s42004-026-01900-3
Ключевые слова: глиобластома, наномедицина, углеродные точки, таргетная доставка препаратов, опухоли мозга