Clear Sky Science · ru
Контролируемый сферулитный рост кристаллов из смесей солей
Почему сольные кристаллы могут выглядеть как цветы
Большинство из нас представляет кристаллы как острые, фасеточные формы, но в природе они часто растут в впечатляющие сферы, напоминающие цветы или снежные шары. Эти «сферулиты» встречаются в вулканических породах, почечных камнях и даже при некоторых заболеваниях, связанных с неправильно свернувшимися белками. В этой статье рассматривается, как обычный минерал — сульфат натрия, та же соль, что в моющих средствах и некоторых строительных материалах — может быть направлен к образованию таких замысловатых сферических кристаллов и что это говорит о том, как сложные структуры самособираются из простых компонентов.
От простых солей к вылепленным сферам
Исследователи стремились понять, когда и как сульфат натрия образует сферулиты вместо обычных блочных кристаллов. Они готовили крошечные капли воды, содержащие смеси сульфата натрия и других сульфатных солей с двухвалентными катионами, такими как магний или железо. По мере того как эти пиколитровые до микролитровые капли медленно испарялись на стеклянных предметных стёклах при комнатной температуре, растворённые соли становились всё более концентрированными, пока не началось образование кристаллов. Систематически варьируя соотношение компонентов, авторы обнаружили особые композиционные «сладкие точки», при которых сульфат натрия стабильно давал сферические, радиально текстурированные кристаллы. Вне этих диапазонов тот же раствор приводил либо к обычным фасеточным зернам, либо к бесформенному гелеобразному осадку — это показывает, что образование сфер требует точно настроенных условий.
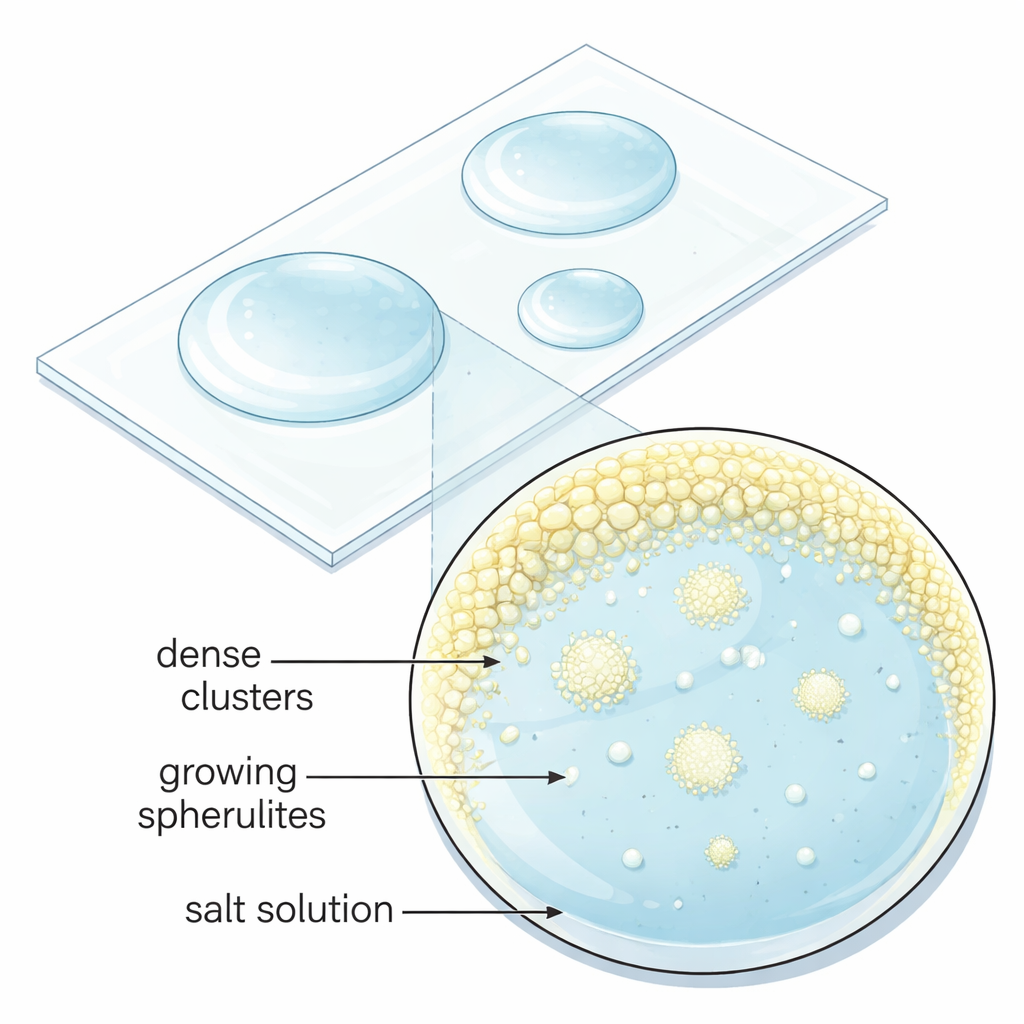
Крошечные жидкие карманы, служащие зародышами кристаллических сфер
Под микроскопом команда заметила, что сферулиты не появляются напрямую из прозрачного раствора. Сначала испарение образовывало небольшие плотные жидкие скопления, обогащённые растворёнными ионами, у края капли. Эти микронные капсулы задерживались в течение минут, а затем внезапно одновременно порождали множество сферулитов. Кадры с высоким разрешением электронного микроскопа высушенных структур показали, что каждый сферулит состоит из бесчисленных нанометровых кристалликов сульфата натрия, ориентированных примерно наружу и позже сплавляющихся друг с другом. Это поведение противоречит классической картине роста кристаллов, где один стабильный ядро растёт равномерно, и указывает на многоступенчатый «неклассический» путь, при котором плотные капли и наночастицы собираются и реорганизуются по пути к окончательному твёрдому состоянию.
Когда солёная вода становится похожей на арахисовую пасту
Ключевая часть истории — то, насколько густым, или вязким, становится раствор по мере потери воды. Отслеживая скорость расширения сферулитов и напрямую измеряя реологические свойства родственных солевых растворов, авторы показали, что смешанные растворы натрий–магний или натрий–железо становятся исключительно вязкими — вплоть до примерно 100 раз гуще мёда — как раз в момент, когда начинают формироваться сферулиты. Такая «пастообразная» консистенция замедляет движение ионов настолько, что именно диффузия, а не поверхностная химия, ограничивает скорость роста кристаллов. В этой медленной среде образуются бесчисленные крошечные кластеры и нанокристаллы, которые успевают слипаться в сферические агрегаты, вместо того чтобы вырастать в несколько крупных, хорошо оформленных кристаллов. Двухвалентные ионы металлов здесь играют ключевую роль: они сильно связывают воду и образуют короткие цепочки или сети, что и повышает вязкость, и способствует образованию аморфной гелеобразной среды вокруг растущих сферулитов.
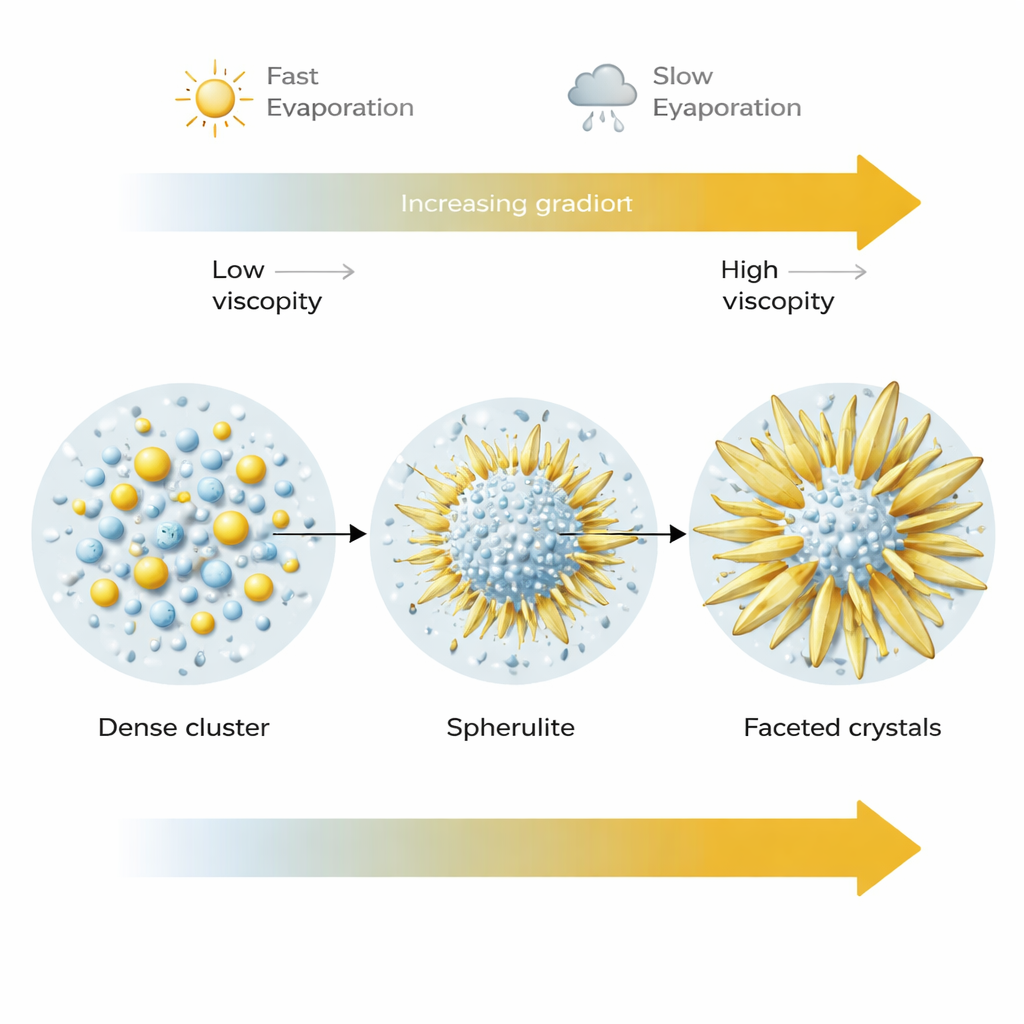
Как скорость высыхания перекраивает окончательные кристаллы
Скорость испарения оказалась ещё одним мощным регулятором. При более быстром высыхании (ниже влажности) множество сферулитов нуклеировалось, но оставалось относительно мелким, «замороженным» в своей метастабильной сферической форме, по мере того как окружающая жидкость быстро загустевала. При медленном высыхании (более высокая влажность) те же начальные сферы имели больше времени и доступа к растворённым ионам. Их крошечные строительные блоки могли реорганизовываться и сливаться в большие, более гладкие и фасеточные кристаллы, часто порождая лопастные отростки, которые в итоге превращались в термодинамически стабильную форму сульфата натрия. Иными словами, сферические структуры служат переходной стадией в пути роста, который при разной скорости сушки и подвижности материала может завершиться очень различными формами.
Почему это важно помимо красивых кристаллов
Проще говоря, исследование показывает: красивые, похожие на цветы сольные сферы возникают тогда, когда концентрированные смеси простых солей становятся достаточно вязкими, чтобы всё замедлить, но не настолько, чтобы рост полностью остановился. При этих «в самый раз» условиях плотные жидкие карманы и рои крошечных кристалликов самоорганизуются в сферические кластеры, которые впоследствии могут превратиться в более стабильные фасеточные зерна. Понимание и управление этим тонким балансом между составом, вязкостью и испарением открывает путь к проектированию пользовательских кристаллических текстур для приложений от более прочных строительных материалов и улучшенных фармацевтических препаратов до лучших моделей геологических и биологических процессов образования кристаллов.
Цитирование: Heeremans, T., Lépinay, S., Le Dizès Castell, R. et al. Controlled spherulitic crystal growth from salt mixtures. Commun Chem 9, 90 (2026). https://doi.org/10.1038/s42004-026-01892-0
Ключевые слова: сферулиты, сульфат натрия, рост кристаллов, неклассическая нуклеация, соляные растворы