Clear Sky Science · ru
Первая кристаллическая структура аддукта, образующегося при реакции ванадиевого соединения с трансферрином человека
Почему имеет значение белок крови и металлический препарат
Множество экспериментальных лекарств содержат атомы металлов, которые могут помогать в лечении таких заболеваний, как диабет и рак. Но как только эти металлооснованные лекарства попадают в кровоток, им приходится «путешествовать» при помощи природных транспортных белков организма. В этом исследовании рассматривается, как один из таких белков — трансферрин сыворотки человека, основной переносчик железа в крови — взаимодействует с перспективным ванадиевым соединением, что проясняет, как металлические лекарства перемещаются по организму и как их можно было бы оптимизировать для более безопасной и эффективной терапии.
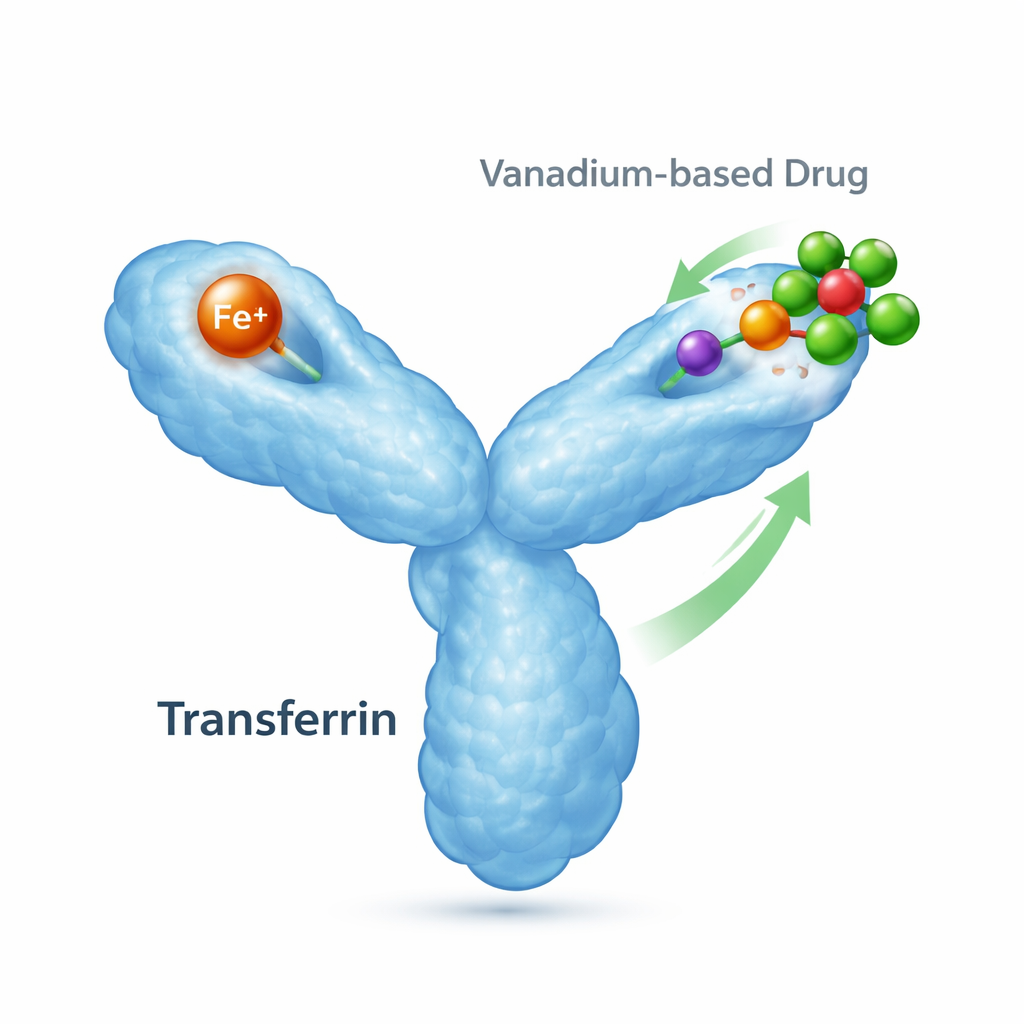
Курьер железа в организме и его второстепенные роли
Трансферрин — это белок молекулярной массы около 80 килодальтон, основная функция которого — захватывать железо и доставлять его в клетки, где оно необходимо. Он состоит из двух «долей», каждая из которых способна связать один ион железа, и меняет свою форму в зависимости от наличия железа. При связывании железа доля «закрывается»; без железа она остается открытой. Специальные рецепторы на поверхности клеток распознают железонагруженные формы и захватывают их внутрь, поэтому трансферрин играет ключевую роль в балансе железа и здоровье клеток. Однако трансферрин также может связывать другие металлы, в том числе используемые в медицинских препаратах, что означает — он может влиять на то, куда попадают металлооснованные лекарства и как они действуют.
Снимок формы: ванадий на трансферрине
Исследователи сосредоточились на хорошо изученном ванадиевом кандидате в лекарства — бис(ацетилацетонато)оксованадии (IV), часто записываемом как [VIVO(acac)₂]. Ранние работы показали, что это соединение или виды, образующиеся из него в воде, могут присоединяться к трансферрину, но точная природа связывания оставалась неизвестной. С помощью рентгеновской кристаллографии команда получила структуры трансферрина высокого разрешения, несущего железо только в его С-концевой доле (форма «FeC»), как до, так и после воздействия ванадиевого препарата. В кристаллах, обработанных ванадием, они обнаружили не исходный препарат, а преобразованный ванадиево-кислородный кластер, связанный в железонезанятой N-концевой доле. Таким образом получили первое прямое структурное изображение фрагмента ванадия, прикреплённого к человеческому трансферрину.
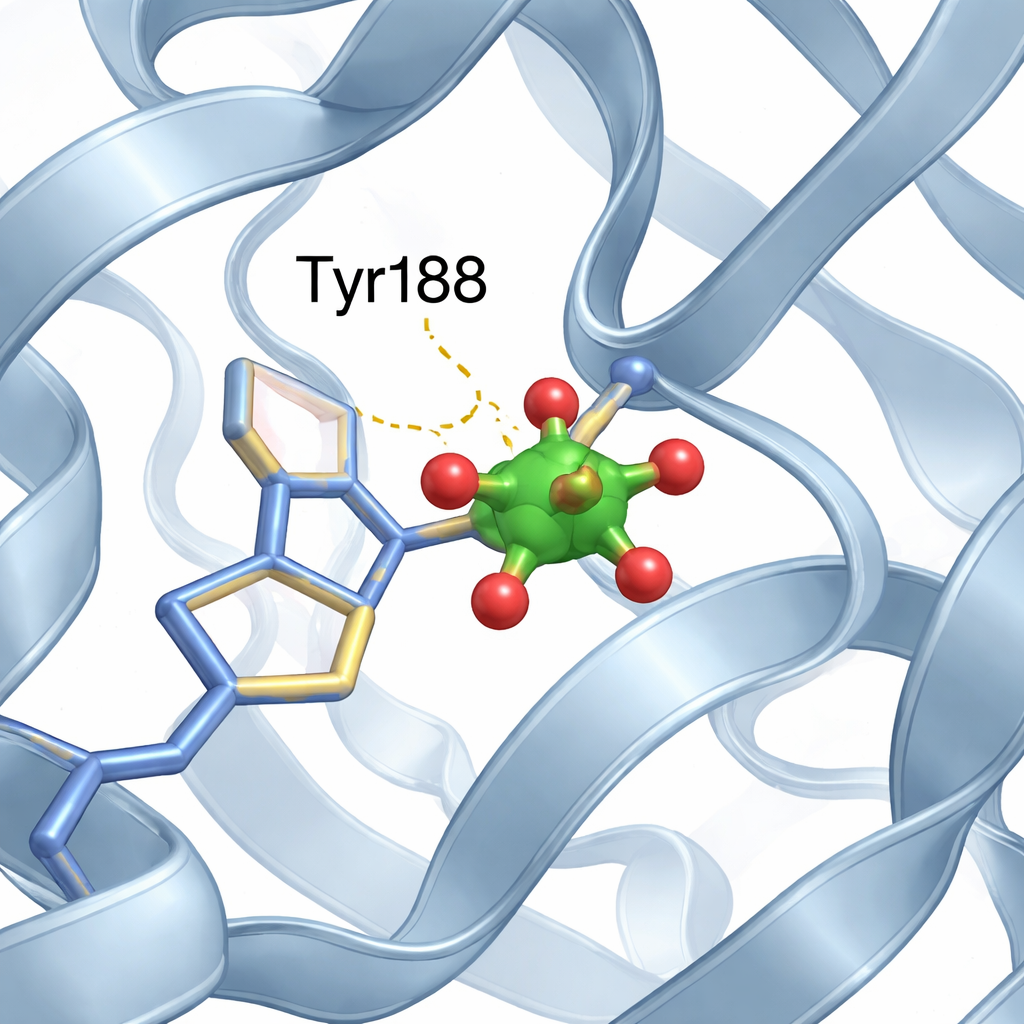
Небольшой ванадиевый кластер находит нишу
Внутри сайта связывания железа в N-доле команда идентифицировала небольшой кластер, состоящий из двух атомов ванадия и кислорода, который лучше всего описывается как модифицированный «диванадат». Одну из кислородных позиций кластера занимает кислород от специфической аминокислоты — тирозина 188 (Tyr188), образуя прямую связь между белком и металлическим кластером. Дополнительные мягкие взаимодействия, такие как водородные связи с соседними сегментами белка, дополнительно стабилизируют кластер на месте. Важно, что несмотря на появление этого металлического гостя в кармане для железа, общая конформация белка сохраняет привычное открытое положение N-доли и закрытое положение C-доли, практически не отличаясь от структуры без ванадия.
Как трансферрин переопределяет химию ванадия
В растворе при pH и концентрации, использованных для кристаллизации, видимая в кристалле двухванадиевая форма обычно является лишь малой долей; в растворе, как правило, доминируют более крупные ванадиево-кислородные кластеры. Спектроскопические измерения и расчёты теоретической специации указывают на то, что исходный ванадиевый препарат медленно окисляется и распадается в воде, образуя простые ионы ванадата, которые затем собираются в разнообразные кластеры. Кристаллическая структура свидетельствует, что трансферрин избирательно стабилизирует именно этот небольшой диванадатоподобный фрагмент в ущерб большим кластерам, по сути «выбирая» одну химическую форму из сложной смеси в растворе, предоставляя удобное место связывания на Tyr188 и поддерживающую сеть водородных связей.
Сохраняется ли рукопожатие с клеточным рецептором
Поскольку трансферрин должен связываться с рецептором на поверхности клеток, чтобы доставлять железо, исследователи проверили, нарушит ли присоединение этого ванадиевого кластера это важное «рукопожатие». С помощью нативного гель‑электрофореза и чувствительного метода биолэйерной интерферометрии они измерили, как ванадием обработанный трансферрин связывается с рецептором по сравнению с необработанной формой, содержащей только железо. Оба варианта вели себя практически одинаково, демонстрируя очень сильное связывание в низком наномолярном диапазоне. Это подтверждает, что ванадиевый кластер, хоть и размещённый в N-доле, существенно не изменяет ту часть трансферрина, где происходит взаимодействие с рецептором, и поэтому не должен препятствовать распознаванию белка клетками.
Что это значит для металлооснованных лекарств
Для неспециалистов главное: это исследование даёт молекулярный снимок того, как производное ванадиевого препарата присоединяется к основному переносчику железа в организме, не нарушая его обычной функции. Трансферрин способен захватить специфический маленький ванадиево-кислородный кластер в сайте для железа, при этом общая форма белка и его способность связываться с рецептором остаются по сути неизменными. Это помогает объяснить, как ванадиевые препараты могут циркулировать, будучи связанными с трансферрином, и подчёркивает, что разные белки могут предпочитать кластерам разного размера. Такие сведения важны для разработки более продуманных металлооснованных терапий, поведение которых в кровотоке — какие формы они принимают, куда направляются и как долго сохраняются — можно предсказывать и контролировать.
Цитирование: Banneville, AS., Lucignano, R., Paolillo, M. et al. First crystal structure of an adduct formed upon reaction of a vanadium compound with human serum transferrin. Commun Chem 9, 89 (2026). https://doi.org/10.1038/s42004-026-01891-1
Ключевые слова: ванадиевые препараты, трансферрин сыворотки человека, металлооснованные терапевтические средства, связывание белок–металл, структурная биология