Clear Sky Science · ru
Лактам обеспечивает удалённые перебалансировки боронатов к C═N‑связям
Новый кратчайший путь к созданию лекарственных молекул
Химики постоянно ищут более быстрые и чистые способы собирать сложные молекулы, встречающиеся в лекарствах и современных материалах. В этой работе предложён изящный приём: обычная кольцевая структура — лактам — временно направляет реакцию, а затем «отступает», что позволяет превращать простые доступные ингредиенты в ценные строительные блоки для фармацевтики без использования дорогих металлов или сложной предварительной подготовки.
Преобразование тихого помощника во временный направитель
Многие современные лекарства и функциональные материалы зависят от реакций бороновых кислот — семейства соединений на основе бора, ценимых за надёжность и мягкие условия. Традиционно для того, чтобы стимулировать бороновые кислоты к образованию новых связей с углеродно‑азотными двойными связями (C=N), химикам приходилось заранее вводить специальные «направляющие группы» в реагенты. Эти группы служат ручками, которые управляют реакцией, но добавляют время, затраты и этапы и часто работают только с очень реактивными партнёрами. Авторы заметили, что лактамы, кольцевые родственники привычной амидной связи, могут выступать в роли встроенных временных направителей. Координируя бор с кислородом лактама, они формируют упорядоченный четырёхкоординированный центр бора, который может перераспределить присоединённую фрагментную группу к удалённой позиции вдоль молекулы, обеспечивая образование новых C–N‑связей без постоянной направляющей группы.
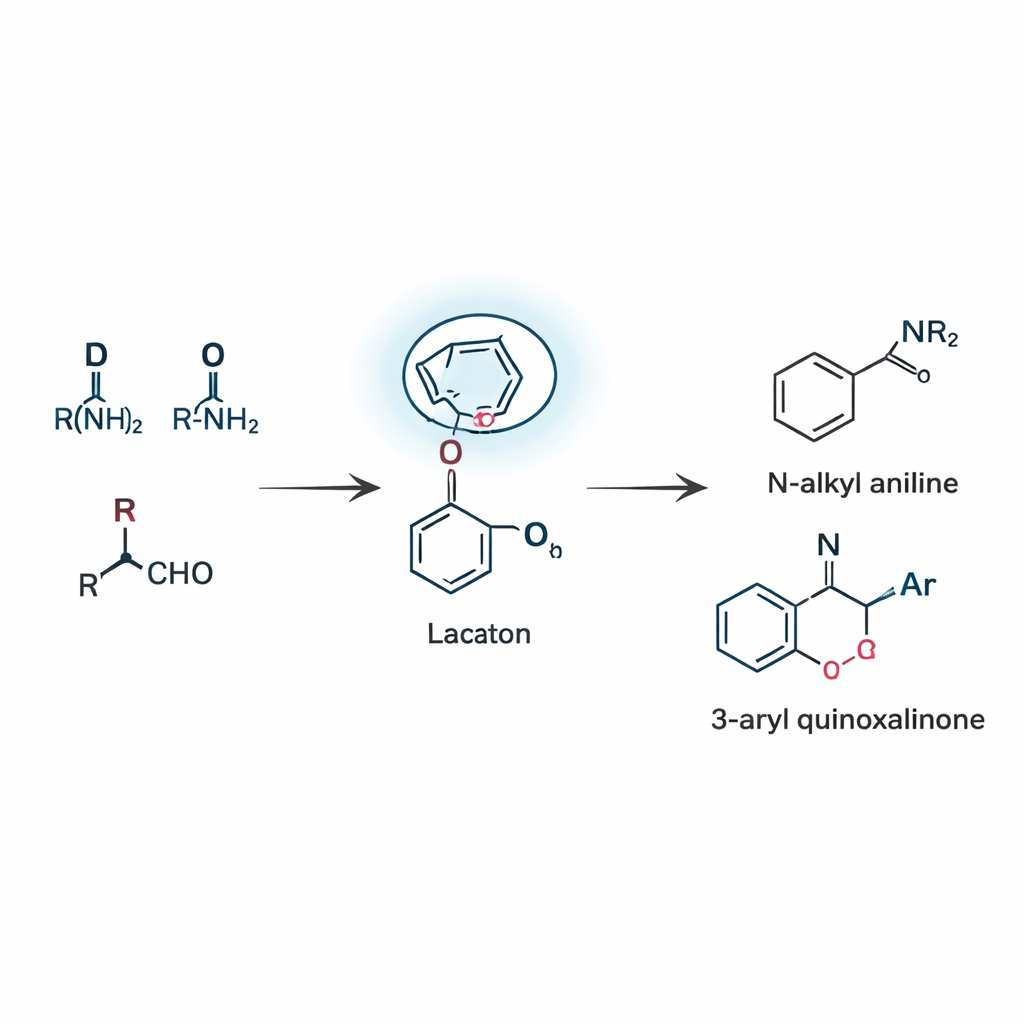
Создание двух семейств полезных продуктов в одной стратегии
Опираясь на эту идею, группа разработала два родственных типа реакций, оба основанные на лактам‑направляемом перераспределении бороната, известном как удалённая перебалансировка бороната. В первом варианте три простых компонента — альдегид, амин и бороновая кислота — объединяются, образуя N‑алкиларилиамины, ключевой мотив, встречающийся во множестве кандидатов в лекарственные средства и красителей. Реакция идёт через редкий 1,5‑перенос, при котором арильная группа на боре перепрыгивает через пять атомов, чтобы достичь C=N. Тщательная настройка катализатора, растворителя и температуры позволила добиться достойных выходов и показать, что многие разные заместители — включая галогены, алкильные группы и гетероциклы — переносятся. Во втором режиме та же направляющая идея применяется к хиноксалинонам, классу азотсодержащих колец, распространённых в медицинской химии. Здесь реакция проходит вообще без добавления металлического катализатора и тем не менее эффективно даёт 3‑ариловые хиноксалиноны благодаря способности лактама вступать в связь с бором и стабилизировать ключевой интермедиат.
Экологичные условия и позднее редактирование лекарств
Помимо демонстрации широкого охвата, авторы показывают, что стратегия практична для реальных молекул. Поскольку 1,4‑перестановка в хиноксалинонах проходит в безметалльных условиях в специализированном спиртовом растворителе, это исключает необходимость в дорогих или токсичных переходных металлах. Группа применила метод к сложным фрагментам, полученным из зарегистрированных лекарств, таких как ибупрофен, и других терапевтических соединений с каркасом хиноксалинона. В каждом случае реакция вводила новые арильные группы в заданную позицию, не затрагивая другие чувствительные участки. Такой подход «поздней стадии функционализации» позволяет химикам быстро украшать существующие лекарственные ядра новыми боковыми цепями, ускоряя поиск более высокой эффективности, безопасности или улучшенных физических свойств.
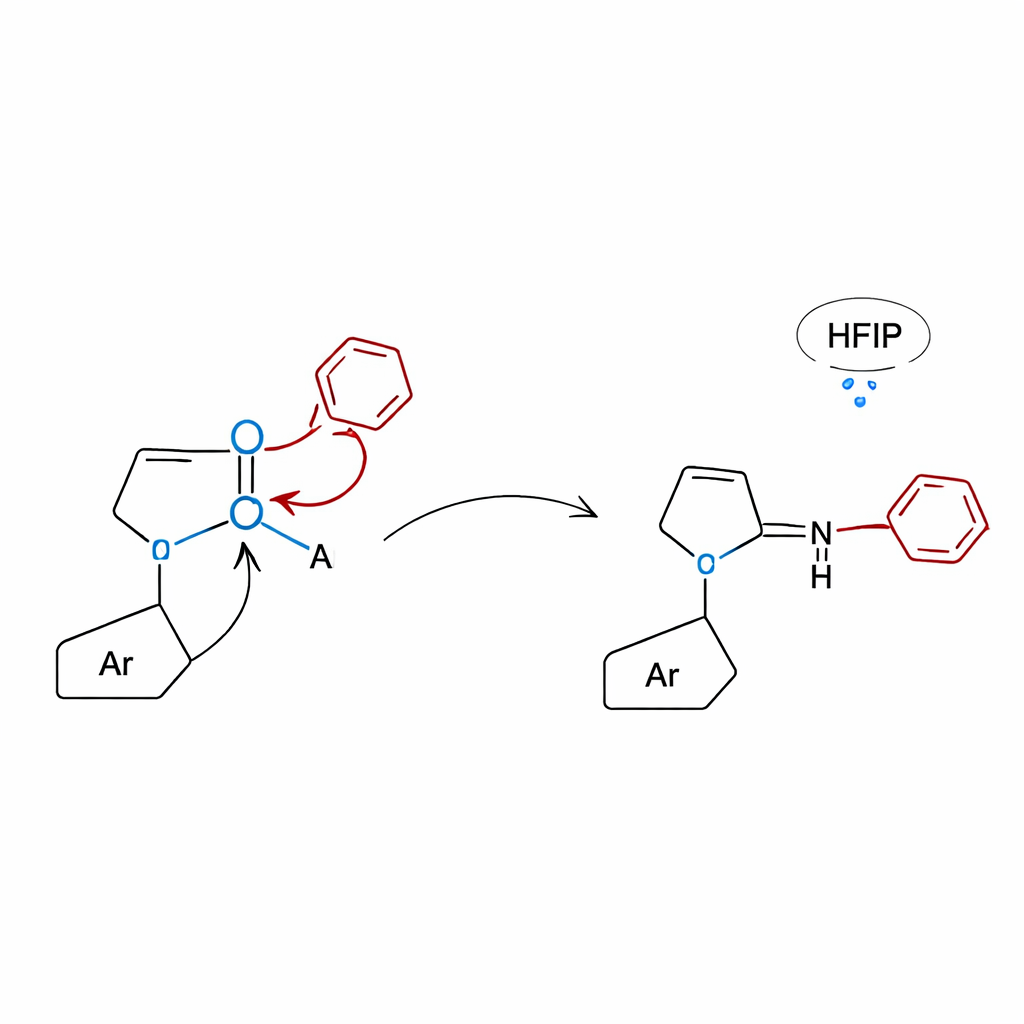
Заглядывая под капот: теория и контрольные эксперименты
Чтобы понять, почему лактамный подход работает так хорошо, исследователи объединили продуманно спроектированные контрольные опыты с компьютерным моделированием. При испытании молекул без лактамной группы реакции практически останавливались, что подтверждает необходимость лактама для активации бороновой кислоты и направления перестановки. Квантово‑химические расчёты показали, что кислород лактама связывается с бором, формируя компактную четырёхкоординированную структуру, из которой арильная группа может мигрировать либо через пять атомов (1,5‑перенос), давая N‑алкилариламины, либо через четыре атома (1,4‑перенос), давая 3‑арил‑хиноксалиноны. В случае хиноксалинонов сеть водородных связей, обеспечиваемая растворителем HFIP, дополнительно понижает энергетический барьер, помогая реакции проходить при относительно мягких термических условиях без добавления катализатора.
Почему это важно для будущих лекарств
В целом работа показывает, что простой лактамный цикл может выступать в роли динамичного, перерабатываемого направителя, который открывает ранее недоступные схемы образования связей в химии бороновых кислот. Для неспециалистов главный вывод таков: у химиков теперь есть более прямой и эффективный способ превращать базовые строительные блоки в два важных класса азотсодержащих молекул, лежащих в основе многих лекарств. Поскольку метод избегает благородных металлов, терпим к широкому набору функциональных групп и пригоден для сложных лекареподобных структур, он способен упростить проектирование и оптимизацию будущих фармацевтических соединений и, возможно, новых агрохимикатов.
Цитирование: Lei, J., Xu, J., Li, X. et al. Lactam enables remote boronate rearrangements to C═N bonds. Commun Chem 9, 88 (2026). https://doi.org/10.1038/s42004-026-01890-2
Ключевые слова: бороновые кислоты, химия лактамов, образование C–N‑связей, хиноксалиноны, медицинская химия