Clear Sky Science · ru
Поиск ферментов на основе инференции орфологов для диверсификации антиракового скелета эводиамина
Превращение растительных химикатов в лучшие лекарства
Многие современные лекарства зародились как защитные вещества в растениях. Эти природные молекулы часто обладают мощными эффектами против рака, инфекций или боли, но редко являются «идеальными» препаратами. Химикам хотелось бы точечно модифицировать их структуры, чтобы сделать их безопаснее и эффективнее, однако эти молекулы часто настолько сложны, что даже небольшие изменения даются тяжело. В этом исследовании показано, как учёные могут использовать растительные ферменты как маленькие молекулярные инструменты для целевых изменений антиракового соединения эводиамина, что потенциально открывает новые пути к улучшенным терапиям.
Почему эта растительная молекула важна
Эводиамин — природное соединение, обнаруженное в плодах дерева, используемого в традиционной китайской медицине. Оно принадлежит к семейству кольцевых молекул, на которых уже основаны важные препараты от рака, высокого кровяного давления и инфекций. Сам эводиамин демонстрировал антираковые, противовоспалительные, болеутоляющие и антимикробные свойства, а некоторые его модифицированные версии выглядят особенно перспективно как многоцелевые кандидаты против рака. Проблема состоит в том, как прикрепить новые химические «ручки», например содержащие кислород группы, в очень конкретные позиции на этом загруженном скелете без использования жёстких химикатов или многоступенчатых синтезов.
Дать ферментам делать тяжёлую химию
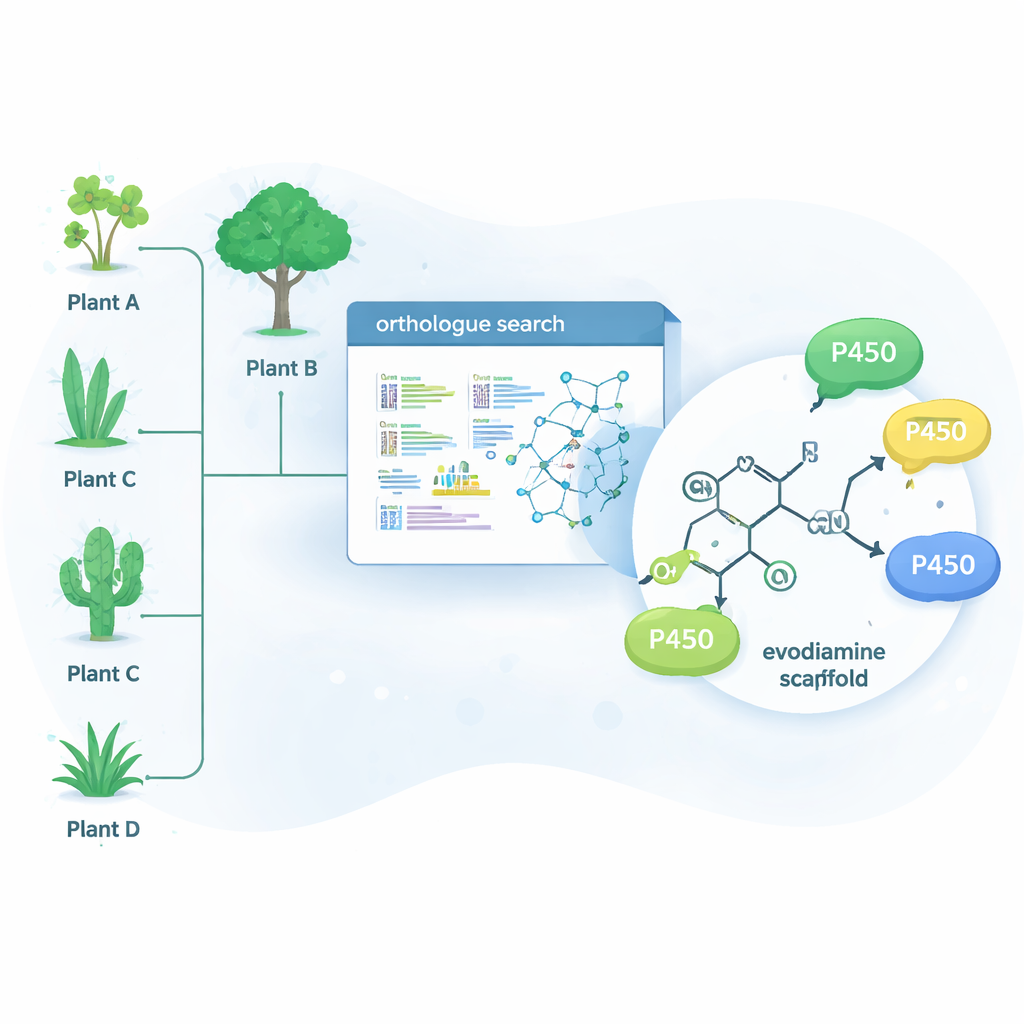
Природа уже решила многие из этих трудных химических задач с помощью ферментов — белков, катализирующих специфические реакции. Одно крупное семейство ферментов, называемое цитохромами P450, отлично справляется с добавлением кислорода к относительно неактивным углеродно–водородным связям. Этот единственный шаг может кардинально изменить поведение молекулы в организме и также создать отправную точку для дальнейшей химической модификации. Вместо того чтобы искать только в растениях, которые естественно синтезируют эводиамин, исследователи использовали биоинформационный инструмент OrthoFinder для сканирования генетических данных 15 различных алкалоидпродуцирующих растений. Они искали P450-ферменты, являющиеся близкими «орфологами» известных алкалоид-модифицирующих ферментов, полагая, что родственники этих белков также могут тонко модифицировать родственные молекулы, похожие на лекарства.
Нахождение новых ферментов в неожиданных растениях
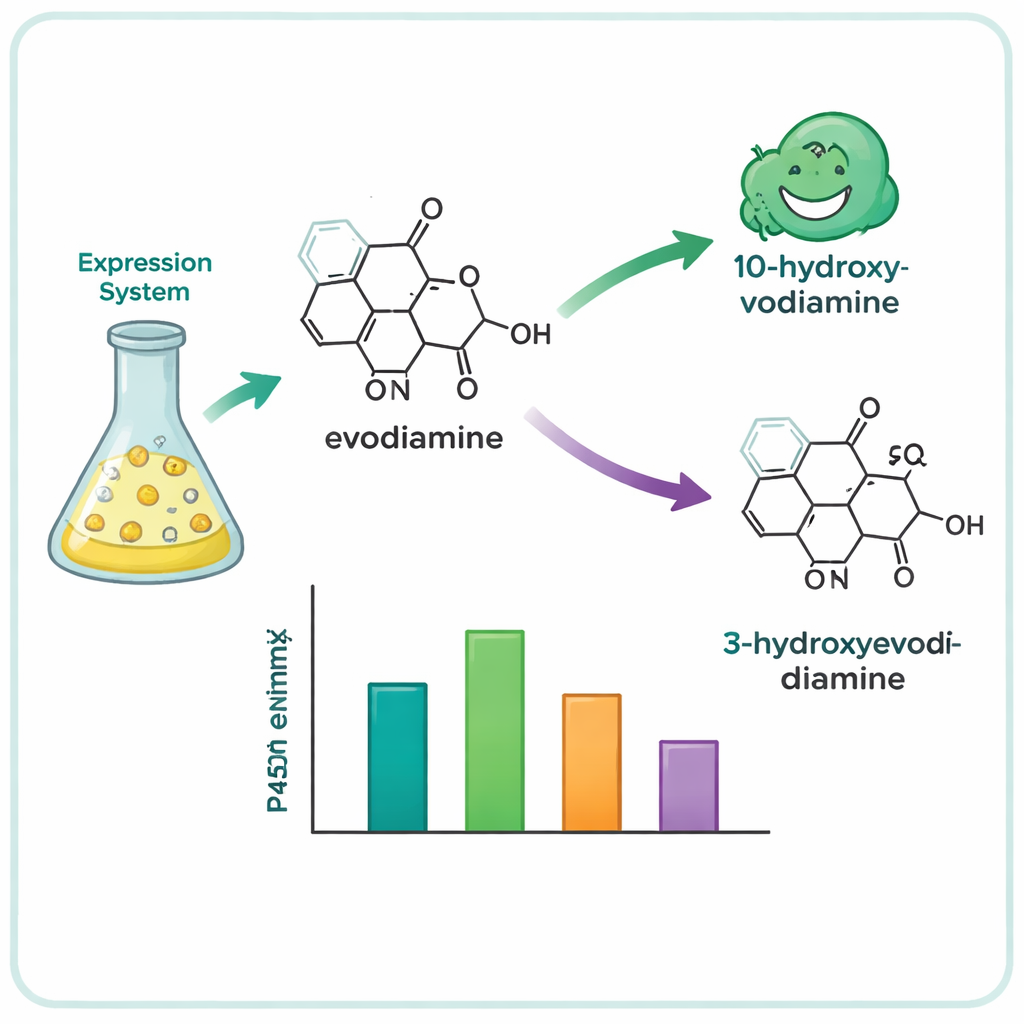
Из сотен кандидатов команда сузила список до 15 перспективных P450 и экспрессировала их в дрожжевых клетках, которые служили миниатюрными ферментативными фабриками. Затем эти дрожжи кормили коллекцией сложных растительных молекул и анализировали, какие из них подверглись химическим изменениям. Четыре фермента — три из дерева Camptotheca acuminata и один из куста Tabernaemontana elegans — оказались активны в отношении эводиамина, хотя ни одно из этих растений не известно как его продуцент. Эти ферменты селективно вставляли атом кислорода в одну из двух позиций на кольцевой системе эводиамина, порождая два основных продукта: 10‑гидроксиэводиамин и 3‑гидроксиэводиамин. Такие окисленные версии проще далее трансформировать в водорастворимые или более активные лекарственные кандидаты, используя более мягкую химию по сравнению с традиционными синтетическими маршрутами.
Заглядывая в набор молекулярных инструментов
Чтобы понять, почему эти близкородственные ферменты вели себя по-разному, исследователи построили трёхмерные модели наиболее активного фермента и его родичей с помощью современных инструментов предсказания структуры белка. Затем они использовали компьютерный докинг, чтобы увидеть, как эводиамин может располагаться внутри активного кармана ферментов, рядом с железосодержащим центром P450, где происходит реакция. Модели выделили несколько объёмных, гидрофобных аминокислот — особенно остатки фенилаланина — расположенных рядом с ароматическими кольцами эводиамина. Путём аккуратного мутирования этих позиций команда показала, что изменение размера и формы этого кармана может ослабить активность, изменить соответствие субстрата или даже переключить предпочтительное место окисления с одного кольца молекулы на другое. В одном случае одна единственная мутация изменила предпочтение фермента с образования 10‑гидроксипродукта на образование 3‑гидроксипродукта.
Что это означает для будущих лекарств
Для неспециалистов ключевая идея в том, что авторы продемонстрировали практическую дорожную карту для обнаружения и настройки растительных ферментов, способных выполнять точечные, «хирургические» правки сложных молекул, похожих на лекарства. Комбинируя масштабный генетический поиск с тестированием ферментов и структурным моделированием, они обнаружили набор биокатализаторов, способных селективно перестраивать скелет эводиамина в позициях, недоступных стандартной химии. Это не только предлагает более чистый и устойчивый способ получения усовершенствованных версий эводиамина — например, водорастворимых антираковых кандидатов — но и показывает, что полезные ферменты можно найти в растениях, которые сами не синтезируют целевое соединение. Ту же стратегию теперь можно применить к множеству других природных продуктов, ускоряя разработку следующего поколения растительных лекарств.
Цитирование: Kwan, B.D., Kim, T., Nguyen, H.H. et al. Orthologue inference-based enzyme mining for diversification of the anti-cancer evodiamine scaffold. Commun Chem 9, 73 (2026). https://doi.org/10.1038/s42004-025-01876-6
Ключевые слова: эводиамин, растительные ферменты, цитохром P450, биокатализ, поиск лекарств