Clear Sky Science · ru
Мутация при синдроме PACS1 нарушает транспортировку грузов, опосредованную динеином, через HDAC6 и BICD2
Почему это важно для развития мозга
Синдром PACS1 — редкое генетическое состояние, которое вызывает интеллектуальную недостаточность, судороги и характерные черты лица. Семьям и врачам известны симптомы, но до недавнего времени было неясно, что именно идет не так внутри клеток пациентов. В этом исследовании раскрывается эта тайна: показано, как одно буквенное изменение в гене PACS1 нарушает внутриклеточную систему транспорта, особенно в нейронах, и как это связывает синдром PACS1 с более широкой семьей «транспортных» болезней нервной системы. 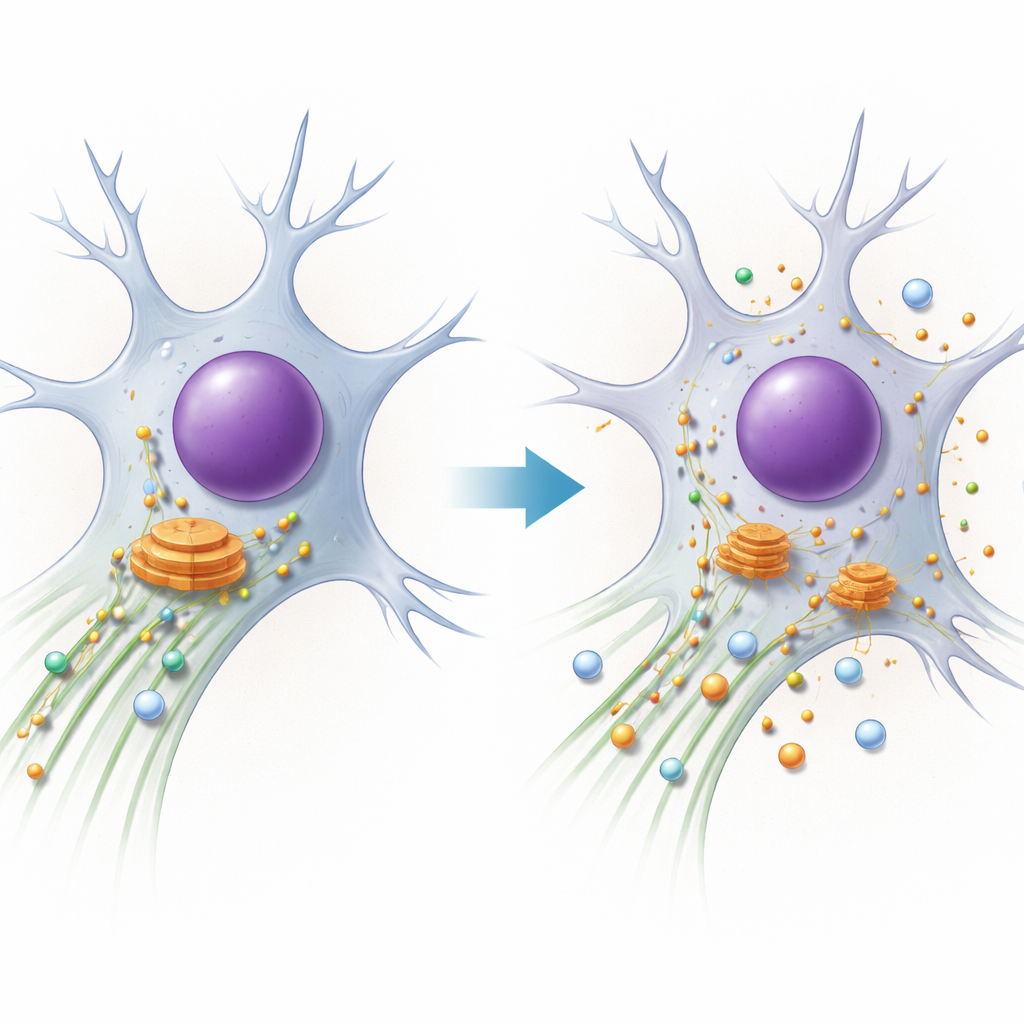
Транспортные магистрали клетки
Каждая клетка опирается на микроскопические магистрали из белковых трубочек — микротрубочек. По этим путям ходят молекулярные моторы, перевозящие грузы, такие как ферменты и мембранные компартменты, туда, где они нужны. Один из моторов, динеин, отвечает за дальние «обратные рейсы», перетягивая грузы с периферии клетки обратно к центру, где находится крупная сортировочная станция — аппарат Гольджи. Авторы сосредотачиваются на PACS1, белке, который помогает выбирать, какой груз должен ехать с динеином, и также регулирует состояние путей через другой белок, HDAC6, управляющий химической меткой (ацетилированием) на микротрубочках. Нейроны, с их очень длинными отростками, особенно чувствительны к даже небольшим сбоям в этой системе.
Мутантный координатор, который хватается слишком крепко
Синдром PACS1 вызывается повторяющейся мутацией R203W в PACS1. Исследователи обнаружили, что как нормальный, так и мутантный PACS1 физически связываются с тяжелой цепью динеина, но мутантная форма сцепляется сильнее. На клетках кожи пациентов и в инженерных клеточных линиях они показали, что такое чрезмерное «захватывание» дает тот же исход, что и частичная утрата функции динеина: аппарат Гольджи распадается на рассеянные мини‑стопки, а важный фермент фурин, обычно локализованный на транс‑стороне Гольджи, неправильно маршрутизируется в другие компартменты. Разбирая структуру PACS1, они выделили короткий бета‑штриховой «пятно», которое конкретно контактирует с динеином. Когда этот участок изменяли, не затрагивая другие функции PACS1, фурин снова терял правильное местоположение, что подтвердило: рукопожатие динеин–PACS1 критично для корректного размещения грузов. 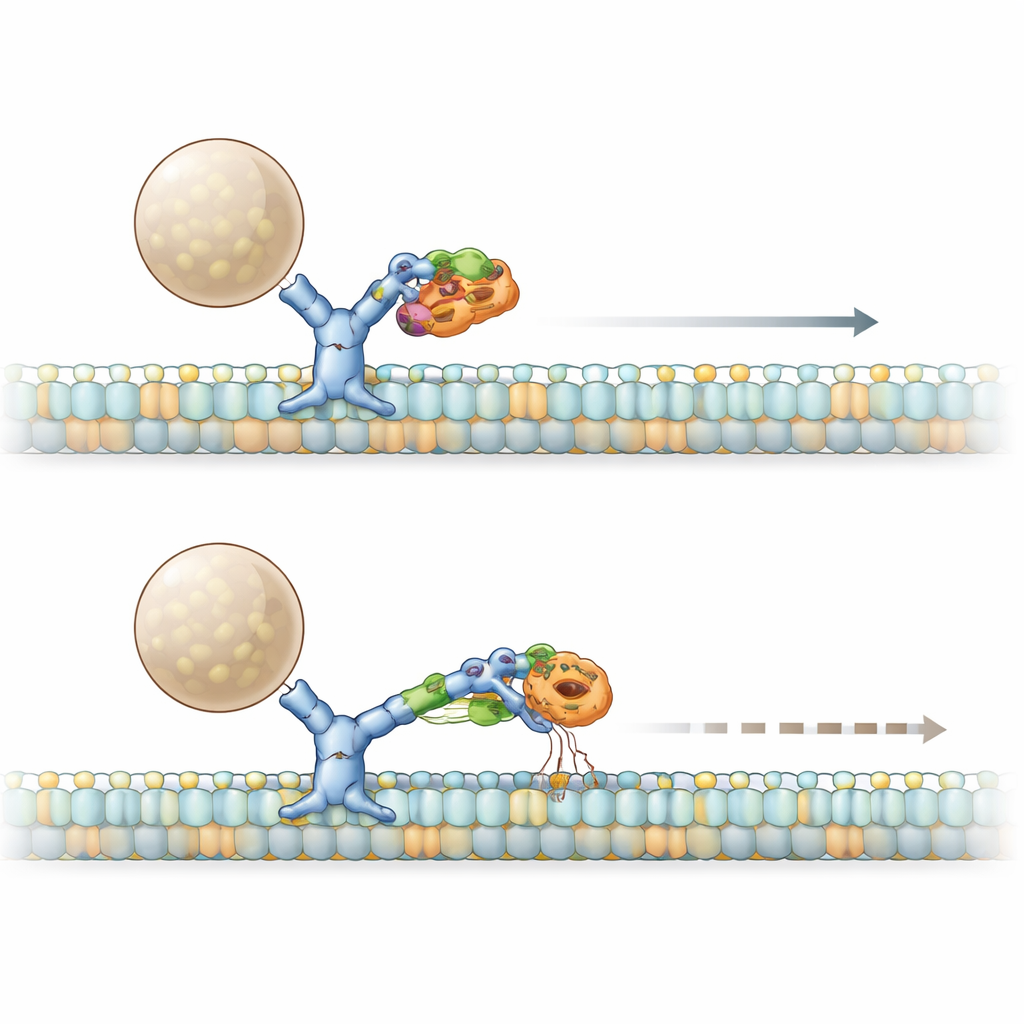
Как тройной альянс блокирует мотор
Сюжет усложняется двумя дополнительными участниками: HDAC6 и адаптером BICD2, который помогает собирать активные комплексы динеина. Мутантный PACS1 не только повышает активность HDAC6, снижая ацетилирование микротрубочек, но и образует увеличенный комплекс с HDAC6 и BICD2. Биохимические тесты показали, что вместе мутантный PACS1 и HDAC6 оттесняют BICD2 от динеина, при этом его взаимодействие с мотором, двигающимся вперед (киназином), сохраняется. В живых клетках искусственный груз, который обычно быстро перемещается по динеину, замедлялся, и число движущихся грузов уменьшалось в присутствии мутантного PACS1. Блокирование активности HDAC6 восстанавливало как скорость, так и количество движущихся частиц, показывая, что комплекс мутантный PACS1–HDAC6–BICD2 действует как тормоз на способность динеина запускать и поддерживать транспорт.
Восстановление трафика с помощью природного помощника динеина
Далее исследователи проверили, можно ли «реактивировать» динеин несмотря на мутантный комплекс. Они обратились к Lis1, известному помощнику динеина, который стабилизирует активные моторные ансамбли. В клетках пациентов уровни Lis1 были несколько снижены. При добавлении избытка Lis1 улучшились две вещи: Гольджи снова сгруппировался ближе к центру клетки, а лизосомы, другой класс органелл, сместившихся к периферии, вернулись на место. В том же эксперименте по подвижности Lis1 увеличивал частоту и скорость перемещения грузов, приводимых динеином, в присутствии мутантного PACS1. Эти результаты показывают, что дело не в отсутствии динеина, а в том, что он оказывается пойман в слабоактивном состоянии — состоянии, которое можно частично исправить либо ослаблением HDAC6, либо усилением активации динеина.
Связывание редкого синдрома с более широким кругом расстройств
Объединяя структурный анализ, клеточную биологию и живую визуализацию, авторы предлагают ясную модель: PACS1 обычно связывает отобранные грузы с динеином и тонко настраивает работу мотора через HDAC6 и ацетилирование микротрубочек. Мутация R203W открывает поверхность взаимодействия PACS1, чрезмерно рекрутируя HDAC6 и BICD2 в комплекс, который подрывает способность динеина захватывать микротрубочки и эффективно двигаться. В результате широко нарушается размещение Гольджи, лизосом и других грузов, особенно в нейронах, где критичен дальний транспорт. Этот механизм помогает объяснить, почему снижение PACS1 или HDAC6 с помощью антисенс‑терапий корректирует дефекты мозга в модельных мышах и сейчас изучается у пациентов. Более широко, это помещает синдром PACS1 в растущий спектр расстройств трафика по микротрубочкам, наряду с состояниями, вызванными мутациями в динеине, BICD2 и связанных факторах транспорта.
Цитирование: Yang, Y., Thomas, L., Chen, K. et al. PACS1 syndrome mutation disrupts dynein-mediated cargo transport via HDAC6 and BICD2. Commun Biol 9, 450 (2026). https://doi.org/10.1038/s42003-026-09924-0
Ключевые слова: синдром PACS1, транспорт динеином, трафик по микротрубочкам, организация аппарата Гольджи, развитие нейронов