Clear Sky Science · ru
Секретируемый белок CLCF1 улучшает течение холестатического заболевания печени, подавляя синтез желчных кислот в печени и способствуя их выведению
Почему это исследование важно для здоровья печени
Холестатические заболевания печени — состояния, при которых желчь, пищеварительная жидкость, вырабатываемая печенью, перестаёт должным образом оттекать и вместо этого накапливается, постепенно отравляя ткань печени изнутри. Существующие лекарства помогают лишь части пациентов, и многим в конечном счёте требуется пересадка печени. В этом исследовании выявлён естественно вырабатываемый белок, называемый CLCF1, который организм, по-видимому, включает как защитный механизм при холестатическом поражении печени. Понимание того, как действует этот белок, может указать путь к новым терапиям, защищающим печень и за счёт снижения образования вредных компонентов желчи, и за счёт более эффективного их выведения.
Скрытый помощник в больной печени
Исследователи начали с изучения ткани печени у пациентов с первичным билиарным холангитом и первичным склерозирующим холангитом, двумя основными формами хронического холестатического поражения печени. Они сравнили людей с ранней стадией болезни и с более выраженным холестазом, а также проанализировали доступные публичные геномные наборы данных. Во всех этих независимых человеческих источниках один секретируемый белок выделялся особенно ярко: CLCF1 последовательно входил в число наиболее резко повышенных генов в холестатических печенях. Повышенные уровни CLCF1 коррелировали с худшими показателями крови, отражающими тяжесть заболевания, что наводит на мысль, что печень усиливает выработку этого белка по мере нарастания стресса и накопления желчи. У пациентов на ранней стадии, лечившихся стандартным препаратом урсодезоксихолевой кислотой, у тех, кто хорошо отвечал на терапию, в печёнах обычно обнаруживали больше CLCF1, что указывает на то, что этот белок может быть маркером более адаптивной, чувствительной к лечению печени.
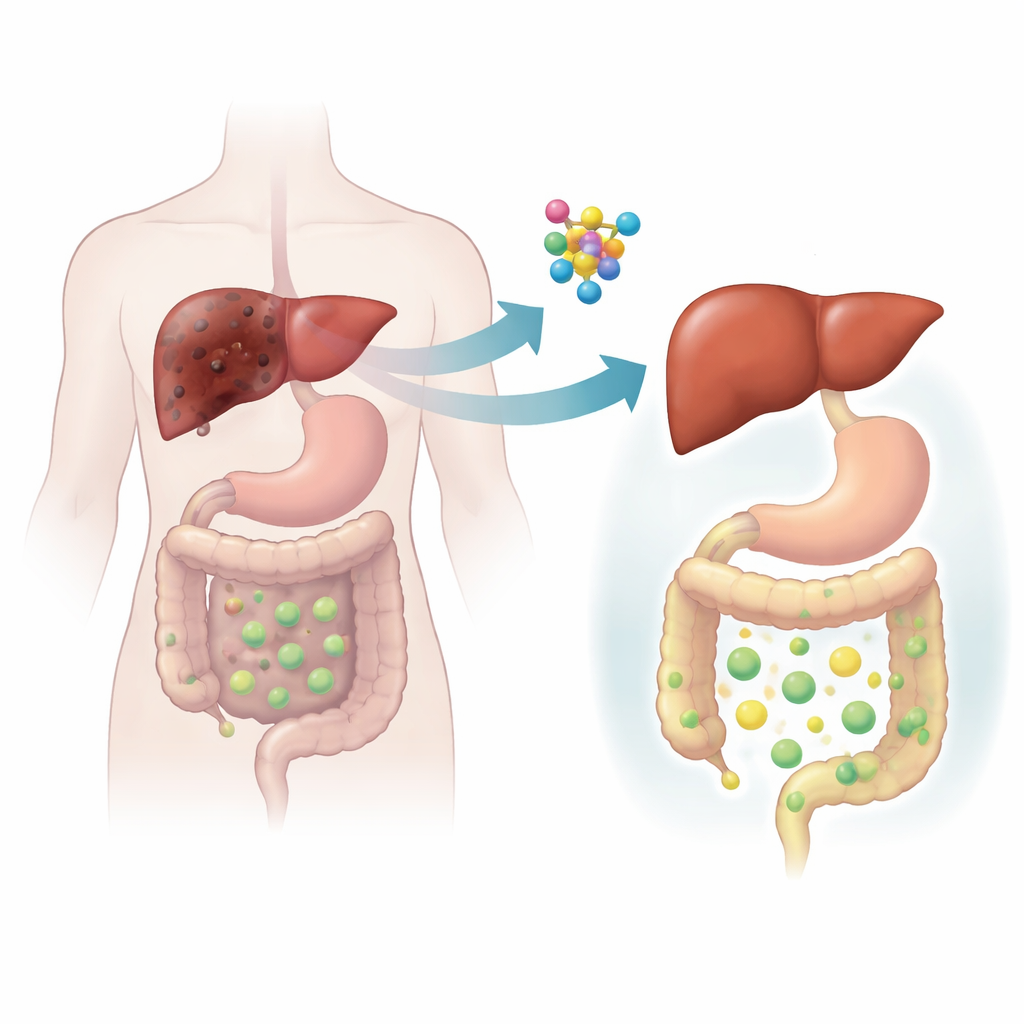
Испытания CLCF1 в моделях на животных
Чтобы выйти за рамки человеческих корреляций, команда обратилась к мышам и с помощью генетических и диетических приёмов воссоздала холестатическое поражение печени. В двух различных мышиных моделях холестаз сильно усиливал синтез Clcf1 в печени, повторяя результаты у людей. Когда учёные специфически удалили рецептор CLCF1 в клетках печени, холестатическое повреждение стало значительно сильнее: наблюдался разрастание желчных протоков, некроз печёночной ткани, усиление воспаления, образование рубцовой ткани и накопление токсичных желчных кислот. Обратный эксперимент дал более обнадёживающий результат. Когда команда использовала безвредный вирус для повышения уровня Clcf1 исключительно в печени, мыши получили защиту: печень выглядела здоровее, показатели крови улучшились, фиброз уменьшился, а количество желчных кислот, задержанных в печени, заметно снизилось.
Перекрытие крана и открытие стока
Как CLCF1 так эффективно снижает перегрузку желчными кислотами? Исследователи обнаружили два дополняющих друг друга механизма. Во-первых, CLCF1 прямо подавлял печёночный механизм синтеза желчи. В нескольких мышиных моделях и в культурах печёночных клеток дополнительный CLCF1 последовательно выключал ключевые ферменты, превращающие холестерин в желчные кислоты, фактически перекрывая поток нового образования желчи. Это происходило без активации обычного печёночного регулятора контроля желчи — ядерного рецептора FXR, что указывает на то, что CLCF1 использует альтернативный внутриклеточный путь для замедления синтеза желчных кислот. Во-вторых, CLCF1 влиял на дальнейшую утилизацию желчи в организме. Он изменял состав микробного сообщества кишечника в сторону бактерий, особенно эффективных в переработке желчных кислот, и увеличивал количество желчных кислот, выводимых с калом, действуя как усиленный сток.
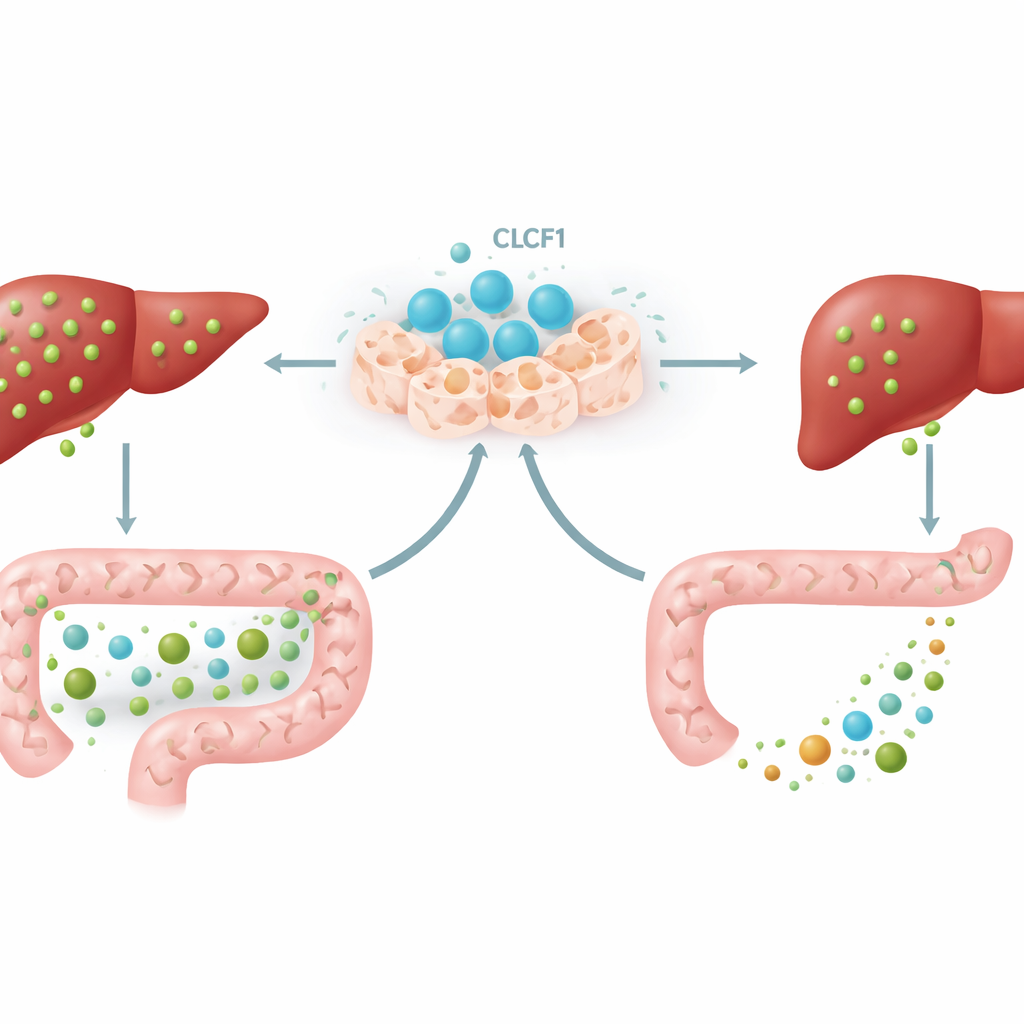
Диалог кишечника и печени
Ключевой элемент механизма связал в обратную связь кишечник и печень. Некоторые желчные кислоты в кишечнике активируют сенсор FXR в клетках кишечной стенки, которые затем выделяют гормон-переносчик, известный у мышей как FGF15. Этот гормон по кровотоку попадает в печень и сигнализирует ей снизить производство желчных кислот. При дополнительном CLCF1 у мышей в кишечнике накапливались специфические типы желчных кислот — особенно те формы, которые являются сильными активаторами FXR. В результате кишечный FXR включался, уровни FGF15 возрастали в кишечнике и печени, и печень дополнительно снижала синтез желчных кислот. Когда учёные блокировали кишечный FXR с помощью препарата, действующего только в кишечнике, большая часть защитного эффекта CLCF1 исчезала, показывая, что этот диалог кишечник–печень является важной составляющей действия белка.
Что это может значить для будущих лечений
В совокупности результаты представляют CLCF1 как встроенный предохранительный клапан при холестатическом заболевании печени. Белок снижает уровень желчных кислот с двух сторон: он замедляет их образование в печени и поощряет их выведение через кишечник, в чём помогают благоприятные кишечные микробы и гормональная обратная связь. В отличие от существующих препаратов, активирующих FXR по всему организму и потенциально вызывающих побочные эффекты, такие как зуд и нарушение липидного профиля, CLCF1, по-видимому, регулирует желчевыделение более мягко и выборочно, особенно через кишечник. Хотя эти результаты получены на мышах и в лабораторных образцах, они позволяют предположить, что усиление активности CLCF1 или имитация его путей может лечь в основу новых терапий, а также что измерение этого белка или тех желчных кислот, которые он обогащает в кишечнике, может помочь выявлять пациентов, наиболее вероятно ответивших на такую стратегию.
Цитирование: Liu, M., Su, Y., Hu, Y. et al. The secretory protein, CLCF1, improves cholestatic liver disease by inhibiting hepatic bile acid synthesis and promoting bile acid excretion. Commun Biol 9, 370 (2026). https://doi.org/10.1038/s42003-026-09847-w
Ключевые слова: холестатическое заболевание печени, желчные кислоты, ось кишечник–печень, CLCF1, микробиота кишечника